科室介绍 查看全部
科室医生 查看全部
科普·直播义诊专区 查看全部
- 精选 术中冰冻病理良性,切片报告为恶性,这算医疗事故吗?
我们有时会听到一些患者家属说: “我们手术当中做切片,医生说肿瘤是良性的,等到正式的病理报告出来一看,变成恶性了!你说是不是医生水平不行?这算是医疗事故吗?” 许多人都想知道答案,却也完全不了解——快速冰冻病理是干什么的?有什么用?为什么会出现误诊? 今天,我们就来聊聊这个话题。 1.什么是术中快速病理 “术中快速病理”是为了给外科医生提供手术决策而进行的病理检查。目前较常用到的术中快速病理包括:快速冰冻病理、印片细胞学病理、快速免疫组化、快速PCR等。但目前国内最常用的还是“快速冰冻病理”。 冰冻病理要求病理医生在手术过程中,利用很短的时间(一般30分钟)内向手术医生提供病理诊断意见。 假设一名女士在洗澡时摸到自己左侧乳腺长了一个不痛不痒的小肿块,她立即到医院就诊。医生在检查后,建议她手术。在手术过程中,医生先把肿块局部切下来,送到病理科,并在手术中等待病理诊断的结果。病理科医生拿到肿块后,用手术刀片仔细地把肿块切开,寻找到可疑的病变之处,切成薄片。再由病理技师将切下的组织放入特殊的冰冻切片机,将组织迅速冻成硬块,制成切片后供病理医师在显微镜下检查,寻找肿瘤的蛛丝马迹,再写出病理报告。手术医生根据这张报告决定手术范围,比如:切除乳房、实施根治术或者仅切除肿块。 2.术中快速病理的临床价值 快速冰冻切片病理学检查可以诊断肿瘤类型、进行病理学分级、确定病变的性质、明确手术切除的肿瘤组织边缘是否有残留等。可以这样说,术中快速病理可以帮助手术医生在手术过程中进一步决定或更改手术方案。 3.术中快速病理准确率有多高? 据国内文献报道,术中冰冻切片诊断总确诊率为93%-99%,延迟诊断率为0.4%~3.5%,误诊率在0.5%~1.0%[1]。与常规石蜡切片相比,冰冻病理存在假阴性更高的可能性(误诊率)。 4.出现误诊的原因 既然病理检查是疾病诊断的“金标准”,为什么快速冰冻病理还会发生误诊?这是因为目前临床上确实存在许多无法避免的因素,导致快速冰冻病理的“假阴性”判断。 (1).疾病发生、发展的因素 虽然临床上把肿瘤分为良性的和恶性的,但疾病在发展过程中会有许多过渡性阶段。以结直肠癌为例,从正常的结直肠粘膜变为晚期恶性肿瘤,需要经历“肠道息肉—腺瘤—上皮内瘤变—早期癌变”。在有些情况下,肿瘤很可能处于良性变为恶性的阶段,也就是医学上所说的“交界性肿瘤”,而交界性肿瘤一直是病理诊断的难点,因其复杂的腺样结构排列使间质浸润更难判断。 早期癌变要通过冰冻切片来确诊是很困难的,甚至在石蜡切片中确诊也非常困难,为了慎重期间,医生会做出延迟诊断的决定。 (2).技术局限的因素 在做冰冻病理时,切片组织会因快速制冷出现冰晶、细胞肿胀等变化,而温度过低或过热、或是温度由冷变热,都会使细胞变形导致胞核肿胀、异型,呈现巢状、条索状分布,容易被误诊为肿瘤细胞。 冰冻切片的诊断困难有其客观性。举例而言,甲状腺嗜酸性髓样癌和嗜酸性细胞癌的冷冻切片在显微镜下的形态非常相似,要通过快速冰冻做出诊断非常困难[1]。而甲状腺微小乳头状癌由于体积小,本身极易误诊、漏诊,而该病的诊断依据为核是否出现异型堆砌、毛玻璃核、核沟等,但毛玻璃核很难在冰冻切片中体现出来,因此通过冰冻切片诊断更加困难。 5.良/恶性无法诊断时怎么办 当使用冰冻病理无法判断疾病是良性还是恶性时,病理医生会暂时给出“良性”的判断。因为在这种情况下,即便得出的是假阴性的判断,之后还是可以通过其他治疗手段予以补救,但如果贸然判断为“阳性”,切除了病人的某个重要器官,以后就无法补救了,这种过度医疗的伤害对病人更大。冰冻病理的“假阴性”还是要靠石蜡切片来诊断,因为石蜡切片的可靠性更高。 虽然目前医学的发展日新月异,但它仍旧是一门不确定的科学。由于技术上的现实制约,快速冰冻病理的误诊率难以避免,因此,我们更要相信每一位病理医生。 冰冻诊断医师的资格要求非常高,需从事病理诊断工作十几年高年资主治以上医师诊断,大部分医院要求有两名高年资医师签名。他们的丰富经验可以帮助我们规避这些技术上的缺憾。 [1].阙金莲,廖旭慧.1585例甲状腺术中冰冻切片与术后石蜡切片诊断对比分析[J].现代实用医学.2016,28(7):890-892.
张玉洁 副主任医师 天津市第一中心医院 病理科4.6万人已读 - 精选 做免疫组化是医生骗你钱?
免疫组化对肿瘤治疗来说是非常重要的!如果没有免疫组化这一步,很难准确判断病情,也不能做出适合患者的最佳治疗方法;对患者负责,科学诊断,积极治疗才是医生们的初衷。 很多患友一定也有过类似疑问:为什么手术都做了,也看到癌细胞,还要做那么多的检查作甚?问医生吧,医生时间有限往往一句话解释不清楚。 为什么增加这个“神秘”的检查——免疫组化?真是为了增收些检查费用吗? NO NO NO,完全不是,这样说真的是太冤枉医生了! 那么,免疫组化到底有哪些作用呢? 一、鉴别肿瘤类型 通常,医生在治疗肿瘤前,都必须清楚它是哪种类型的肿瘤。因为不同类型肿瘤的治疗方法是不一样的。一般在肿瘤病检中,“苏木精-伊红染色(HE染色)”可以鉴定出大多数的肿瘤类型。但是,仍有5%-10%的肿瘤HE染色难以辨别,无法看清肿瘤的真面目,这时候就需要免疫组化等辅助技术来“帮忙”辨别。 举个栗子,像淋巴瘤、胚胎性横纹肌肉瘤等软组织肉瘤在HE染色“看来”,长得跟多胞胎一样,分不清谁是谁。根据一些蛛丝马迹,推测可能是淋巴瘤,这时候再做一下免疫组化,真相顿显。 另外,对于有的肿瘤来说,只知道它是哪个肿瘤还不够。这些肿瘤又细分为好几个亚型,每种亚型的治疗方法还是不一样的,所以有必要弄清楚这种肿瘤的亚型是哪个,还是需要免疫组化“出山”。 比如,确诊胆囊癌了,是腺癌还是鳞癌或者未分化癌等?确诊乳腺癌了,是ER+、PR+、HER2+还是三阴性乳腺癌(ER-、PR-、HER2-)呢等等。通过免疫组化检查3种受体:雌激素受体(ER)、孕激素受体(PR)、HER2受体的表达状态就可以知道答案。 二、发现微小转移灶 免疫组化能发现更早的微小转移灶。用常规病理检测方法HE染色有时候难以发现微小的转移灶。一方面某些肿瘤的早期转移灶与淋巴结内窦性组织细胞增生“长得”比较像,这使得它难以被发现;另一方面是因为早期转移灶都很小,尤其是只有一个转移性细胞或几个细胞的时候,用HE染色的方法在一个组织中认出它们,就好比在茫茫人海中找到一个人或几个人,海底捞针,难以实现。而免疫组化就不一样了,免疫组化识别精确度较高,自带“火眼金睛”,即使是十分微小的肿瘤转移灶,也难逃“法眼”。要知道,出现转移的肿瘤和完全没有转移的肿瘤,在治疗方法以及预后上可能会有很大差别的。免疫组化真是帮了大忙了。 三、确定肿瘤原发部位 免疫组化不仅能发现微小的转移灶,还能分辨出这些转移灶的“身份”,即它们是身体哪个部分的肿瘤派来的。比如,骨组织内有前列腺特异性抗原阳性细胞,就说明可能是前列腺癌派的“兵”转移到骨组织。知道这些转移灶来自哪里对治疗方法的选择意义重大。 四、确定肿瘤分期,预测患者预后 免疫组化能通过确定肿瘤分期来预测患者预后,分期越靠后,患者预后就越差。比如运用免疫组化判断肿瘤是原位癌还是浸润癌,浸润癌有没有侵袭到血管或淋巴管等,可以判断肿瘤的分期。如果发现上皮性癌突破了基底膜,就说明不是原位癌,而是浸润癌了,肿瘤发生了转移,那么患者预后是完全不一样的。而这个“本领”对HE染色来说,实现起来十分困难,但免疫组化却“游刃有余”。 五、确定肿瘤分化程度 免疫组化也能通过确定肿瘤的分化程度来预测患者预后。比如,确诊是胆囊癌,通过免疫组化检测PCNA、MMP9等的表达水平可以确定胆囊癌的分化程度,分化程度越低,患者预后就越差。 言而总之,免疫组化对肿瘤治疗来说是非常重要的!如果没有免疫组化这一步,很难准确判断病情,也不能做出适合患者的最佳治疗方法。对患者负责,科学诊断,积极治疗才是医生们的初衷。随着现代医学的进步,越来越讲究个体化精准治疗,这就要求患者不仅仅要做免疫组化,甚至还可能需要做个基因检测,才能找到最合适自己的个性化治疗方案,获得最佳治疗效果。
张玉洁 副主任医师 天津市第一中心医院 病理科4519人已读 - 常见病毒性肺炎的病理鉴别诊断
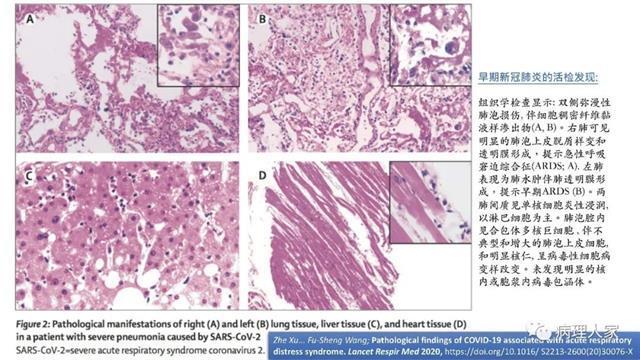
2019-nCoV新型冠状病毒引起的肺炎(NCP)在今年春天肆虐全球,目前已导致全球上百万人感染,几十万人死亡。该病毒传染性极强,来源、宿主、传染途径和潜伏期等尚不完全清楚。此前经相关病理学家对死亡病例进行解剖研究,初步对其病理改变和特征等有了初步的认识,并与SARS ,流感以及其他病毒感染所致肺炎的临床和病理特征进行鉴别诊断研究,加强病理医生对新冠肺炎病理性改变的进一步认识。 当前最常见的病毒性肺炎的种类有新型冠状病毒性肺炎(NCP,COVID-19),严重急性呼吸综合征(SARS),流感肺炎(H1N1,H7N9),呼吸道合胞病毒肺炎和腺病毒肺炎等。 新型冠状病毒性肺炎(NCP,COVID-19)的病原体是冠状病毒科的新成员,2020年初爆发,目前全球累计感染上百万,死亡几十万,极具传染性,主要通过呼吸道传播。影像学表现为单灶/多灶斑状/点状影,至后期全白肺表现。病毒的自然史、传播途径、中间宿主、潜伏期和病理特征尚不完全清楚,诊断标准依据临床表现、影像学表现以及核酸检测是否阳性等。 病理特征包括早期表现和急性期表现。早期表现有弥漫性肺泡损伤(DAD),透明膜形成;细胞纤维粘液样渗出,肺水肿,ARDS;间质单核细胞、淋巴细胞浸润;以及病毒性细胞病变样改变。急性期表现有弥漫性肺泡内出血;下呼吸道管腔内浓稠粘液和纤维素渗出和聚集;广泛肺血管病变包括血管纤维素炎,血管周围炎;炎细胞为单核细胞为主,其他淋巴细胞、浆细胞、巨噬细胞、组织细胞也可见。 严重急性呼吸综合征(SARS)也是由冠状病毒科的一种新成员引起,2002-2003年在全球爆发,8000多发病病例,750多例死亡,一般通过呼吸道分泌物传播。 病理学特征中弥漫性肺泡损伤(DAD)是其典型病变。弥漫性肺泡损伤急性期通常11天——主要表现有间质和肺泡腔成纤维母细胞增生,细支气管和肺泡腔纤维粘液样栓形成,肺泡间隔增厚和机化性肺炎。 此外,还出现小气道损伤包括支气管和细支气管上皮纤毛丢失,上皮细胞脱落,纤维素沉积在细支气管管腔和沉积在暴露的基底膜上。以及其他非特异性发现如肺血栓栓塞、鳞状细胞化生、多核巨细胞等。可伴有CMV、曲霉菌病等共感染。 用RT-PCR、分子检测和电镜检查可明确诊断。
 张玉洁 副主任医师 天津市第一中心医院 病理科2402人已读
张玉洁 副主任医师 天津市第一中心医院 病理科2402人已读




