科室介绍 查看全部
科室医生 查看全部
-
肝胆外科

杜成友
主任医师 教授
肝胆外科主任
肝胆外科
陈勇
主任医师 副教授
4.3
肝胆外科
罗放
主任医师 教授
4.1
肝胆外科
吴忠均
主任医师 教授
3.9
肝胆外科
黄平
副主任医师 副教授
3.8
肝胆外科
孔宪炳
主任医师 副教授
3.7
肝胆外科
廖锐
副主任医师 副教授
3.8
肝胆外科
王济明
主任医师 教授
3.7
肝胆外科
郑军
副主任医师 副教授
3.7
肝胆外科
罗诗樵
副主任医师 副教授
3.7
-
肝胆外科

王洪林
主任医师 教授
3.7
肝胆外科
李明
副主任医师 讲师
3.7
肝胆外科
吴晓健
副主任医师
3.7
肝胆外科
史政荣
主任医师
3.6
肝胆外科
杨祖奎
副主任医师 副教授
3.6
肝胆外科
阎雄
副主任医师
3.6
肝胆外科
贺强
主治医师
3.5
肝胆外科
刘强
主治医师
3.5
肝胆外科
吴乔
副主任医师
3.5
肝胆外科
邱建国
主治医师 讲师
3.5
-
肝胆外科

凌康
主治医师 讲师
3.5
肝胆外科
肖衡
主治医师
3.5
肝胆外科
潘龙
医师
3.4
肝胆外科
闫雄
3.4
肝胆外科
周宝勇
3.4

蓝翔
副主任医师

魏续福
副主任医师
科普·直播义诊专区 查看全部
- 精选 浅谈胰腺导管内乳头状黏液性肿瘤(IPMN)
胰腺导管内乳头状黏液性肿瘤(IPMN)指源于主胰管或胰管主要分支有大量黏液分泌的乳头状肿瘤。IPMN具有恶变潜能,早期确定并采取适当手术方式或随访方案处理,对于获得良好预后十分关键。一、分型根据胰管受累情况,IPMN可分为3种类型:(1)主胰管型(mainduct-IPMN,MD-IPMN):恶变率较高,60%~70%(2)分支胰管型(branchduct-IPMN,BD-IPMN):恶变率略低,15%~-25%(3)混合型(mixedtype-IPMN,MT-IPMN):恶变率认为与主胰管型相似二、组织病理学2019版WHO胰腺肿瘤分类将IPMN分为:IPMN伴低级别异型增生(lowgradedyplasia,LGD)、IPMN伴高级别异型增生(highgradedyplasia,HGD)、IPMN伴浸润性癌;后两者通常被认为是恶性病变在切除的MD-IPMN中,HGD和浸润性癌的比例分别高达61.6%、41.3%;而切除的BD-IPMN标本中,HGD和浸润性癌的比例分别为31%、18.5%。三、诊断1.临床表现:整个胰腺均可受累,胰头及钩突部最为常见,因肿瘤生长缓慢,大多数患者仅在健康体检时发现而无任何症状。部分出现上腹部疼痛,恶心、呕吐,腰背部疼痛,梗阻性黄疸,反复发作的胰腺炎2.实验室检查:血清CA19-9升高与恶性IPMN相关,敏感度为79%~100%,但在正常范围内的CA19-9水平并不排除恶性可能。3.囊液分析:对超声内镜引导下细针穿刺活检获取的囊液进行综合分析,可能提高诊断的准确性。二代测序技术(NGS)测定囊液中的KRAS和GNAS突变可区分黏液性与非黏液性肿瘤,KRAS/GNAS突变见于73%的黏液性肿瘤,而GNAS突变被认为仅存在于IPMN中,因而可作为鉴别IPMN与MCN的指标。然而,不管囊液CEA水平还是KRAS和GNAS突变均无法鉴别良恶性病变。因此,目前不做为常规推荐。4.影像学检查:MD-IPMN常见于胰头,为边界相对清晰的囊实性混合病灶,特征性表现为主胰管弥漫性或节段性扩张,可延伸至分支胰管,管腔内充满黏液,囊肿壁有时出现增厚增强并可见强化的乳头状结节。BD-IPMN多见于钩突部,病灶呈分叶状或葡萄串样,可见分隔,与主胰管相通,BD-IPMN也可能出现主胰管扩张。MT-IPMN则同时出现MD-IPMN、BD-IPMN的表现。四、手术策略目前缺乏IPMN最佳治疗策略高度统一的国际共识。2017年修订版福冈指南将IPMN恶性危险因素分为“高危特征(high-riskstigmata,HRs)”和“忧虑特征(worrisomefeatures,WFs)”(表1)。2018版欧洲循证指南则采用绝对指征(absoluteindications,AI)和相对指征(relativeindications,RI)的手术策略(表2)。目前国外指南均建议所有适合手术的MD-IPMN患者均应接受手术治疗;而MT-IPMN发生HGD和浸润癌的几率与MD-IPMN相当,故治疗策略与MD-IPMN相同。对于BD-IPMN,在切除的BD-IPMN中恶性病变(HGD、浸润性癌)发生率为25.5%(6.3%~46.5%),而浸润性癌的发生率也达17.7%(1.4%~36.7%)。因此,任何有HRs、AI的患者,只要适合手术也应接受手术治疗。而欧洲指南支持更积极的策略,如果适合手术的患者存在一个或以上RI,或在有严重合并症且未进行EUS的患者中发现两个或以上RI,则建议手术切除。手术方式主要取决于肿瘤位置、大小、有无邻近侵犯及恶性征象,具体包括胰十二指肠切除术、保留脾脏或不保留脾脏的胰体尾切除术、胰腺中段切除术、全胰腺切除术以及肿瘤剜除术,存在HFs、AI时应联合标准的淋巴结清扫。五、随访策略1.未行手术切除的IPMN随访:随着时间的推移IPMN进展的风险会增加,故对无手术指征的IPMN患者应终生随访,直到不再适合手术为止。MRI应作为首选的影像学随访监测方法,在怀疑存在壁结节等恶性病变高危特征时进一步行EUS、EUS-FNA。2.手术切除的IPMN随访:对于仍适合手术的患者,术后均继续进行随访监测直至不再适合手术治疗。六、预后IPMN预后比胰腺导管腺癌好,非浸润型术后5年生存率77%~100%,浸润型5年生存率仅为24%。(参考《中华肝脏外科手术学电子杂志》2022年第11期)
 陈勇 主任医师 重医大附一院 肝胆外科3729人已读
陈勇 主任医师 重医大附一院 肝胆外科3729人已读 - 精选 心中有光、素履以往,MDT模式给晚期肿瘤患者带来希望
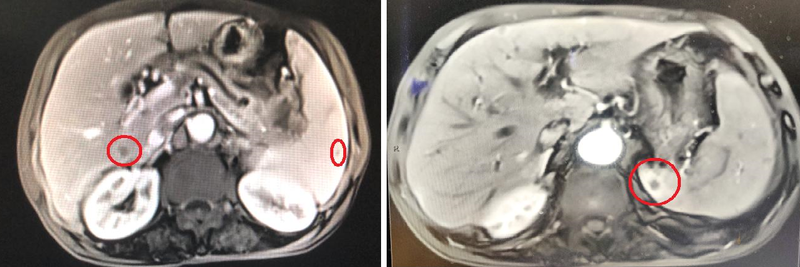
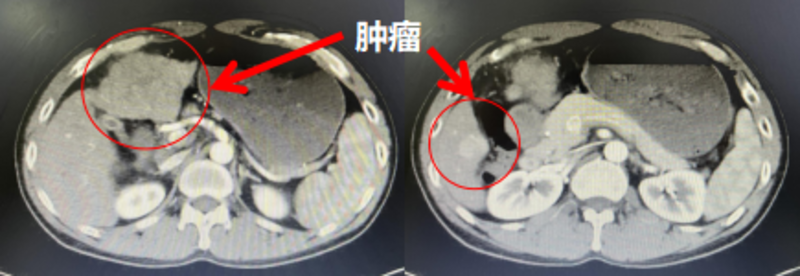
“心中有光、素履以往,MDT模式给晚期肿瘤患者带来希望”----重医附一院胰腺肿瘤MDT诊疗2周年回顾(2)近年来,包括原国务院副总理黄菊、世界著名男高音帕瓦罗蒂、香港著名艺人沈殿霞等不少名人都因胰腺癌逝去。据不完全统计,2005年以来已有16个名人因胰腺癌而去世,并且他们在确诊为胰腺癌后生存时间大部分不超过2年,最短的仅2个月。胰腺癌是一种恶性程度很高,诊断和治疗都很困难的消化道恶性肿瘤。约90%为起源于腺管上皮的导管腺癌,其发病率和死亡率近年来明显上升。5年生存率<10%,是预后最差的恶性肿瘤之一,素有“癌中之王”的称号。胰腺癌的治疗主要是以外科手术为主的综合治疗,但是胰腺癌早期诊断困难,大多数患者一经确诊已属中晚期,手术根治率低,治疗效果极差。面对晚期胰腺癌真就没有手术机会,只能选择放弃吗?重医附一院肝胆胰外科采用多学科诊疗模式(MDT),精确评估患者病情,综合治疗给患者带来希望。“医生,我父亲胰腺癌已经发生了转移,还有机会治好吗?”2021年3月,一位患者家属走进陈勇医生诊室的第一句话便带有很强的失落感。他父亲因“反复中上腹疼痛3月”在当地医院以“胃炎”治疗但效果不佳,后行CT检查提示胰腺癌伴淋巴结多发转移。当地主治医师告诉患者家属为晚期胰腺癌,总体治疗效果很差。家属没有放弃,决定来重医附一院肝胆胰外科寻求帮助。“尽管您父亲病情较重也不要轻易放弃,只有坚持积极治疗,才有希望,心态一定要平和。”陈勇主任医师一边安慰家属一边安排患者入院治疗。 (MRI提示肝脏、脾脏多发转移病灶) 完善检查后,为患者开启了MDT治疗模式。放射科李咏梅教授亲自阅片:“患者MRI检查示:胰腺尾部肿瘤样病变,大小约4334mm,符合胰腺癌表现。肿瘤邻近脾动静脉受侵。胰胃间隙、小肠系膜根部淋巴结肿大,考虑转移;肝脏及脾包膜下小结节,考虑转移。”影像学的准确评估明确了患者的病情为胰腺癌IV期(晚期)。由于存在腹腔多发转移,患者暂无手术机会。化疗需要病理学依据,而患者肝脾等转移灶均较小,穿刺困难。超声科李茂萍副主任医师为其进行了超声引导下经皮胰腺穿刺活检。病理科讯速阅片确定为“胰腺低分化腺癌”。结合患者身体基本情况、治疗意愿、家庭经济等诸多因素,肿瘤科为患者制定了综合治疗方案,以吉西他滨联合白蛋白结合型紫杉醇化疗联合PD-1抗体免疫治疗。经过一个周期的治疗,患者腹痛症状明显缓解,生活质量明显提高。由于疫情影响,患者治疗一度中断。治疗2个月后复查CT、MRI提示胰尾部肿瘤累及脾动静脉,对比旧片提示病灶范围较前缩小,较前对比肝脾包膜下病灶显示不清。CA-199也由最初的1512U/ml降至136.2U/ml。 (CT、MRI提示肝脏、脾脏转移病灶基本消失)初步治疗效果非常明显。再次经过MDT团队讨论,治疗意见为可以继续当前治疗,同时患者也具备了手术切除的条件。患者及家属充分考虑后选择手术治疗。在科室杜成友主任的指导下,陈勇主任医师成功为其实施腹腔镜下胰体尾切除+脾切除+肝部分切除。微创手术顺利,患者术后在营养科等科室协助下康复出院。面对胰腺癌,作为病人和家人常常是无助的,他们可能会将全部的希望都寄托在医生身上。而作为医生,为了担负起这样的期望,尽力去为患者争取更多的获益。本例患者,在放射科、超声科、病理科、肿瘤科、营养科等多个科室和团队的协作,制定个体化的综合治疗方案,患者获得了较好的治疗效果。对于暂时不能手术切除或复发转移的患者,可以进行包括化疗、靶向、免疫治疗等综合治疗。另外,参与新药临床试验也可能让患者获益,我科目前正在开展伊立替康脂质体增强化疗,以及PD-L1/CTLA-4双特异性抗体免疫治疗胰腺癌的两项III期临床研究。专家提示:出现不明原因的腹痛、消化不良、黄疸、血糖升高、体重明显下降的患者,不要掉以轻心,应该及时到医院检查。发现胰腺癌,也不要丧失信心,“心中有光,素履以往”,保持乐观积极的心态,通过综合治疗才可能获得较好的治疗效果。下期我们将分享一例罕见的胰腺癌多发病灶,行全胰腺、十二指肠联合脾脏切除根治手术的病例。
 陈勇 主任医师 重医大附一院 肝胆外科296人已读
陈勇 主任医师 重医大附一院 肝胆外科296人已读 - 精选 一碗酸辣粉“引发”的肝癌?
事情追溯到 2020 年国庆节,大家都沉浸在节日的喜悦中时,40 来岁的邓某,他的心情却从云端跌入了谷底。邓某在进食一碗“酸辣粉”后便感觉 上腹部隐痛不适,本以为只是单纯的胃病,来到医院检查彩超提示肝脏里有肿块,怀疑 “ 肝癌 ” 。晴天霹雳,万念俱灰, “ 当时的心情 用绝望来形容, 一点也不夸张 ”, 邓某回忆到 。 带着肿瘤与绝望邓某来到我院肝胆外科 ,罗放教授 、吴晓健副主任医师等专家团队为其组织了科内讨论, 并 告知还有治疗机会 。 此时邓某仿佛听到有一个声音在鼓励着他, 让他不放弃, “活下去” ! 于是他决定接受治疗 。进一步评估后发现自己有乙肝、肝硬化,甲胎蛋白明显升高,高达 826 ng/ml 。 左右半肝均有肿瘤存在,且肝脏储备功能较差( ICG15分钟滞留率高达 23% ),肝体积明显缩小, 如果直接进行手术治疗可能因剩余肝体积不足而出现肝衰竭 ,且手术风险极大 。强烈的求生欲望让他犹豫了。在与医生充分沟通后, 邓某暂时放弃了手术治疗 ,选择了介入治疗联合靶向、免疫治疗 ,开启了他的抗癌之路。 2020年10月在罗放教授及吴晓健副主任医师的指导下,钟华博士为邓某实施了第一次介入栓塞(D-TACE),术中钟博士使用微导丝微导管超选至肿瘤供应动脉,使用载药微球进行精准化疗栓塞,并于同月开始了联合靶向,免疫治疗。治疗后出现疼痛、发热、恶心、呕吐一系列不良反应,但在我科护理团队的精心照顾下,他都一一克服了,并表示在这里感受到了回家般的温暖。 2021年3月患者复查提示大部分肿瘤已缺血坏死,仅少许肿瘤有动脉供血 ,钟华博士再次予以 D-TACE 介入治疗。此后患者每次复查均未见肿瘤有血供存在,且体积也慢慢在缩小,甲胎蛋白从 800ng/ml 降至 8.6ng/ml 。 但在开始治疗的 9 个月后遇到了瓶颈期,复查肿瘤并没有再缩小, 由于体内肿瘤的存在, 邓某始终 忐忑 不安。有点沮丧的他,愁容满面的找到吴晓健副主任医师询问道是否还可以手术切除肿瘤 。看着焦虑的 他 ,罗放教授和吴晓键副主任医师打算放手一搏,考虑其肝储备功能差,准备行肝 S4 段肿瘤切除联合肝 S6 段肿瘤射频消融。 手术历时 2 个半小时,术中出血量不到 100ml 。 将术中切除的肿瘤及周围粘连的网膜组织行病理检查,均未见癌细胞。术后重庆医科大学病理科 对标本进行 了多次科内会诊讨论,最终考虑为介入栓塞术后使得肿瘤细胞已经完全坏死,确诊为高分化肝细胞肝癌。 手术历时2个半小时,术中出血量不到100ml。术中将切除的肿瘤及周围粘连的网膜组织行病理检查,均未见癌细胞。术后重庆医科大学病理科对标本进行了多次科内会诊讨论,最终考虑为介入栓塞术后使得肿瘤细胞已经完全坏死,确诊为高分化肝细胞肝癌。 术后至今多次复查,均未见肝脏内有复发迹象,可见邓某已获得了完全缓解( CR)。 治疗的效果与成功,让邓某的 脸上洋溢着幸福的笑容 。 当然,抗癌成功不仅与合理有效的治疗有关,患者良好的心态也至关重要。每次与邓某谈话时,他总是说 “肝癌现在的治疗手段那么多,药物那么好,有什么好怕的”。虽然不是每个肝癌患者都能像邓某那么幸运, 吃一碗酸辣粉便能较早的发现肝癌,通过综合治疗能获得完全缓解,毕竟有 70%~80% 的肝癌患者一确诊就是中晚期,但肝癌的局部治疗(介入、射频)联合系统治疗,是可以使肝癌患者获益,甚至完全缓解的 。所以,肝癌并没有想象中可怕,它可以 “ 从有到无 ” ,抗癌成功的希望也可以 “ 从无到有 ” 。 重医附一院金山医院肝胆外科自开科以来,便开始进行肝脏各个段的解剖性切除术(肝叶切除、半肝切除、肝段切除术), 也同步开展腹腔镜下的解剖性肝切除, 肝切除无手术禁区。 目前完成了肝脏肿瘤手术三百余台,肝介入手术五百余台,其中绝大多数患者均能从中获益,联合目前如火如荼的靶向、免疫治疗,中晚期肝癌患者的生存期明显延长,肝癌的治疗手段值得期待 ,预后的改善同样值得期待 !
 罗放 主任医师 重医大附一院 肝胆外科876人已读
罗放 主任医师 重医大附一院 肝胆外科876人已读
问诊记录 查看全部
- 胰腺癌 3月份复查时血管内皮因子430pg/ml,4月17日复查21... 下次复查的时间,和此次报告的阳性结果所代表的意义,是否是复发总交流次数3已给处置建议
- 胰腺肿瘤 陈教授,您好,我父亲邓**胰腺癌化疗6个月了,腹部又开始散痛... 下一步怎么治疗?总交流次数12已给处置建议
- 右上腹疼痛3月余。 患者3月前无明显诱因出现右上腹疼痛,与饮食无明显关系。遂至当... 怎样治疗总交流次数37已给处置建议
- 胆系疾病 我4月9号查血报,除了血管内皮生长因子没出来,cT报告也出来... 好久复查总交流次数27已给处置建议
- 胆管癌 陈教授,我父亲于**2023年9月底在重医您给做的肝门胆管癌... 1.头晕跟肿瘤可能有关系吗,检查什么项目呢?2.头晕好些了再化疗可否?3.化疗改为每三周一次那种。总交流次数6已给处置建议
总访问量 2,542,763次
在线服务患者 12,150位
科普文章 150篇
领导风采



