精选内容
-
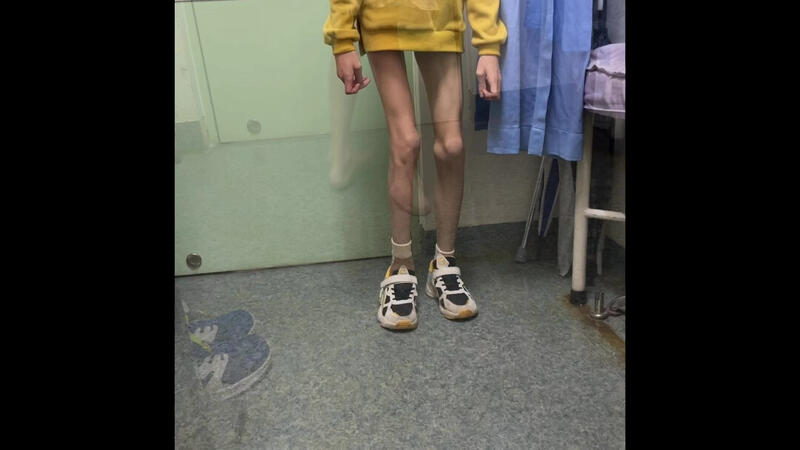
杜良杰教授病例:脊髓肿瘤所致的痉挛性瘫痪,下肢功能重建术前术后行走步态对比
 杜良杰医生的科普号
杜良杰医生的科普号 2024年02月25日
2024年02月25日 311
311
 0
0
 1
1
-
术中发现瘤子巨大无法手术,只能放弃?或许我们仍应抱有希望
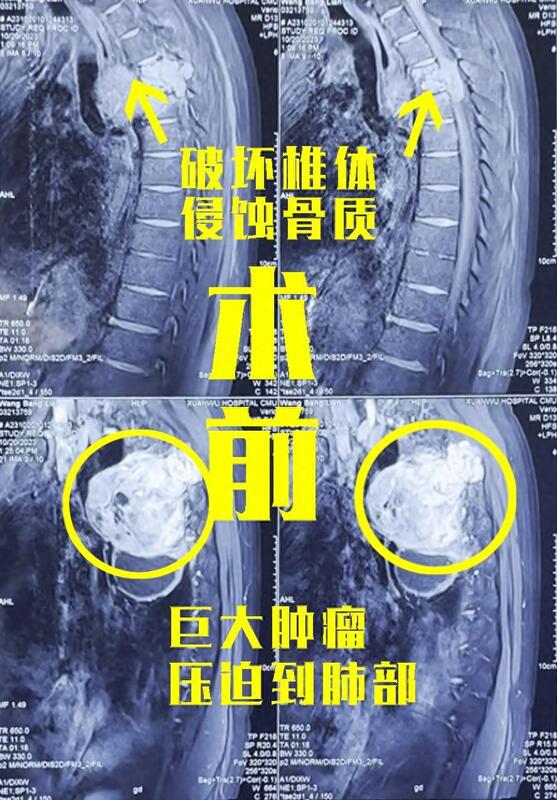
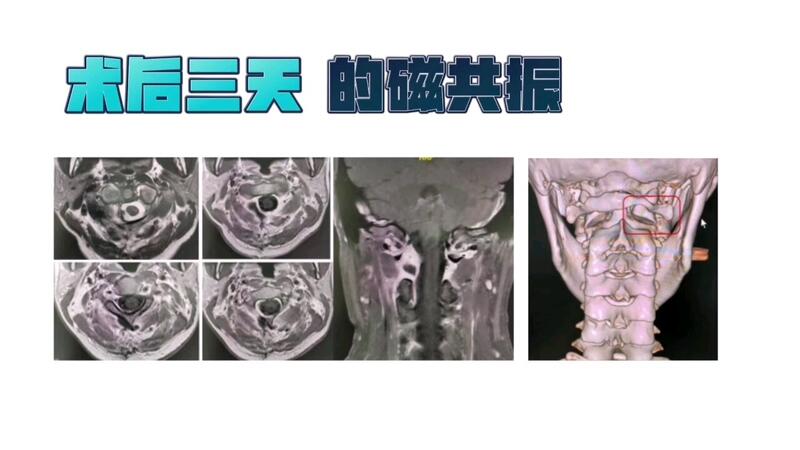
让任何人在生死面前做选择都是非常痛苦的,但往往留在最后的就是遗憾、无奈和无力适从。许多患者、家属或者家庭会遇见这样的绝境,检查出现是肿瘤,想要切掉,却被告知肿瘤太大无法手术。这种境遇下该怎么办?只能听天由命,放弃积极治疗?最近,首都医科大学宣武医院神经外科王作伟主任就遇见了这样一位患者。患者男性,67岁,2、3年前就出现双腿的麻木、无力、走路不稳等情况,有时候还有胸闷、喘不过气的表现,近期感觉到症状加重,于是在当地医院就诊,而这也开启了他们一家波折的求医之旅。手术室的灯灭了,医生的话变成噩耗!患者在家人陪伴下去了他们当地的一家大医院进行检查,发现他在椎管附近长了一个肿瘤,且肿瘤非常大,当时的建议是进行手术切除。一家人做好了准备,对治疗也充满了希望,各项检查都做好后,患者被推进手术室。谁知刚过不久,在外等待的家属就看到手术室的灯灭了,然后医生出来就告知家属,肿瘤长得太大了,手术风险太高,决定不切除肿瘤。就这样,肿瘤仍然原封不动。“无法手术!那怎么办?”这简直就是噩耗,让人陷入绝望的噩耗!但他们并没有放弃,在多家医院咨询后都被告知做不了手术后,他们决定进京求医。北京是全国医疗最好的地方,找这方面最权威的专家试试,他们抱着最后的希望找到了王主任。“我这里可以做!”一句话让家属如释重负看了患者的各项检查结果和片子,王主任当即给了他们一颗“定心丸”,“你这种情况,我们这里可以做手术!”患者的情况确实比较复杂,他的肿瘤部分长在了胸椎管内,严重压迫到里面的脊髓,而且还长到了胸椎,破坏了胸椎体的骨质,而大部分的瘤体在胸腔压迫到了肺部,再加上瘤体巨大,和周围的神经、脊髓、血管等重要组织关系密切,都让手术变得困难重重。但是如果不手术解决,继续进展下去,脊髓损伤可能会导致后期瘫痪,而肺部的压迫也要早早解除为好。术前影像学资料:虽然手术不好做,但对于技术娴熟、经验丰富的神经外科医生来说,这种程度的手术也不是没有做过,完全可以做到心中有底。随后,王主任就为这位患者成功进行了手术。手术中,在尽可能保护周围组织的情况下全切掉肿瘤。切出来的肿瘤巨大,比一颗饱满的大柚子还要大一些。术后,患者的下肢症状和胸闷气短的情况都得到了极大的好转,患者及家属对效果非常满意。术后进行拍片检查,肿瘤已经全切,脊髓彻底减压,恢复充盈。术后影像学资料:面对肿瘤太大不能手术的患者来说,可能不是每个人都有这样的手术机会,但是仍然希望大家不要过早放弃治疗,积极、勇敢地面对。
 王作伟医生的科普号
王作伟医生的科普号 2023年11月05日
2023年11月05日 109
109
 0
0
 0
0
-
脊柱脊髓肿瘤系列三
 中山大学附属肿瘤医院科普号
中山大学附属肿瘤医院科普号 2023年05月20日
2023年05月20日 20
20
 0
0
 0
0
-
我是胸椎脊髓占位术后肢体麻木,肛门会阴部异物感,怎么治疗?

 席焱海医生的科普号
席焱海医生的科普号 2022年11月24日
2022年11月24日 30
30
 0
0
 0
0
-
椎管内肿瘤科普系列五:星形细胞瘤,预后最差的脊髓肿瘤
在前面几个系列中,我们详细介绍了神经鞘瘤、脊膜瘤、室管膜瘤等常见的椎管内肿瘤。这些肿瘤无一例外都有一个特点,以良性病变为主,手术治疗后预后好,就算是恶性的室管膜瘤,也因为与脊髓有明显的分界,手术也能取得不错的效果。但所有的椎管内肿瘤都这么“善良”吗?答案显然是否定的,而今天就来介绍预后最差的脊髓肿瘤——星形细胞瘤。神经组织主要由两类细胞构成:神经细胞和胶质细胞,其中神经细胞是神经组织的“大脑”,起到关键的传递神经信号的作用,而胶质细胞则相当于房子的“框架”,在神经组织中起到连接和支持各种神经成分,分配营养物质、参与修复和吞噬神经细胞的作用,是神经细胞发挥功能的基础。在胶质细胞中,星形胶质细胞又是最多且体积最大的胶质细胞,此类胶质细胞呈星形,能发出许多长而分支的突起,因此而得名。髓内星形细胞瘤是起源于脊髓星形胶质细胞的肿瘤,既然起源于脊髓,那么毫无疑问星形细胞瘤属于髓内肿瘤。脊髓星形细胞瘤占脊髓肿瘤的6%-8%,占髓内肿瘤的30%。星形细胞瘤可发生于任何年龄,但多见于30岁以下,是儿童最常见的髓内肿瘤,在成人中发病率也仅次于室管膜瘤。男性多见,男女比例约为1.5:1。肿瘤可发生于脊髓的任何节段,但以胸段最多见,其次为颈段,在马尾圆锥等部位较罕见,这点与室管膜瘤不同。根据WHO分型,脊髓星形细胞瘤按恶性程度从低到高可分I~IV级。WHOI级为良性肿瘤,如毛细胞型星形细胞瘤;WHOⅡ级为低度恶性肿瘤,如弥漫浸润星形细胞瘤;WHOIII级,恶性程度较高,肿瘤增殖能力强,如间变性星形细胞瘤;WHOIV级恶性程度最高,肿瘤常常早期出现播散转移,如多形胶质母细胞瘤等。与颅内星形细胞瘤不同,多数脊髓星形细胞瘤为低级别肿瘤(I级和Ⅱ级);儿童脊髓星形细胞瘤85%~90%是低级别肿瘤,而成人约为75%。间变性星形细胞瘤占所有星形细胞肿瘤15%-25%,多形胶质母细胞瘤仅占0.2%~1.5%。脊髓星形细胞瘤由于肿瘤生长缓慢,病程长,早期症状多不明显,多表现为肿瘤部位以下肢体麻木、无力,肿瘤累及到脊髓后角的感觉神经可出现神经根痛,但相较于其他椎管内肿瘤少见。随着肿瘤的生长,患者也会逐渐出现感觉、运动障碍,感觉障碍从上向下发展,可出现痛温觉丧失而触觉保留的分离性感觉障碍。患者也可出现肌萎缩、肌震颤,但大多出现较晚且不明显。括约肌功能障碍引起的大小便功能障碍可早期出现。如果肿瘤发生出血,由于脊髓内占位效应突然增加可致瘫痪。星形细胞瘤的生长方式与室管膜瘤有所不同,室管膜瘤多在脊髓中心呈同心圆性生长,但星形细胞多偏向一侧生长,且边界不清,这些在影像学上都有利于星形细胞瘤的诊断。星形细胞瘤的诊断目前主要依靠临床症状及影像学。星形细胞瘤在X线平片上通常显示正常,少数病变可见椎管扩张,CT上可见到脊髓不规则的增粗,肿瘤显示多不清楚。MRI是诊断星形细胞瘤较好的手段,表现为脊髓增粗,肿瘤界限不清,边界不规则,偏心性生长;增强扫描为轻度、不均匀、片状或环状强化。肿瘤内部可出现囊变,但在肿瘤两端空洞少见。手术切除是脊髓内星形细胞瘤的主要治疗方法。既往脊髓髓内星形细胞瘤多倾向保守治疗,常采取椎板减压术、活检术及肿瘤部分切除,再辅以放疗或化疗。近年来,随着显微神经外科技术不断进步,多数学者赞同积极手术治疗。手术切除程度主要取决于肿瘤与脊髓之间有无相对清晰的边界。髓内低级别星形细胞瘤由于与周围正常组织的界限相对清楚,质地软,应用现代显微外科技术大多能达到全切除或次全切除,且手术致残率低,常获得满意效果。但对于浸润性生长的恶性星形细胞瘤不宜勉强全切除,应尽可能行瘤内减压切除,以避免脊髓功能严重受损。髓内星形细胞瘤术后是否放疗目前仍有争议。过去髓内星形细胞瘤手术多采用保守术式,病人术后多接受常规放疗,但疗效并不肯定,且会引起脊髓放射性损伤,脊髓萎缩变性,加重神经功能障碍,青少年病人尤其如此。因此,我们建议能全切除或次全切除的低级别星形细胞瘤术后无需放疗,即使复发,可再次手术;而对于恶性星形细胞瘤通常仅能部分切除,且极易发生脑脊液播散,术后应行放疗,此外还应当联合化疗。文献报道替莫唑胺、顺铂、长春新碱等药物对脊髓星形细胞瘤有效。其他靶向治疗、免疫治疗等新疗法还处于临床试验阶段。脊髓星形细胞瘤预后主要取决于肿瘤的组织学分类。术前神经功能状态、切除程度、术后肿瘤是否有播散是影响手术预后的重要因素。总体来说,脊髓星形细胞瘤的预后要比室管膜瘤差,低级别星形细胞瘤5年生存率为70%,而高级别星形细胞瘤5年生存率仅30%。星形细胞瘤术后容易复发,因此术后遵医嘱定期复查十分重要。早期发现复发的肿瘤,早期再次干预,可选择再次手术或是放射治疗,对于提高星形细胞瘤患者的预后同样十分重要。
吕立权医生的科普号 2022年04月23日
2022年04月23日 920
920
 1
1
 7
7
-
什么是中枢神经系统肿瘤?
中枢神经系统(centralnervoussystem,CNS)肿瘤是位于脑或脊髓的肿瘤性疾病,可根据细胞来源分为原发及继发两类:原发性CNS肿瘤起源于神经系统实质细胞,或位于颅内/脊髓腔内但非脑或脊髓实质的细胞;继发性CNS肿瘤起源于颅外/脊髓腔外,并转移至颅内/脊髓腔内结构。原发性CNS肿瘤的年发病率约为23.8/10万,其中约30%为恶性,主要包括胶质瘤、脑膜瘤、垂体腺瘤、神经鞘瘤等。继发性CNS肿瘤的年发病率约为8.3~14.3/10万,其来源主要包括肺癌、乳腺癌、黑色素瘤、肾癌、结直肠癌等。约5%的原发性CNS肿瘤与遗传相关;电离辐射是被证实与CNS肿瘤发生相关的危险因素。良性和恶性原发性CNS肿瘤患者的5年生存率分别为91.7%和36.0%;继发性CNS肿瘤的预后取决于病变类型及全身病变情况,中位生存期为2~27个月。
郭晓鹏医生的科普号 2022年03月26日
2022年03月26日 521
521
 0
0
 0
0
-
双脚痛且温觉减退 竟是椎管里长了瘤
今年16岁的小玲是一名高中生,半年前,她突然感觉自己左腿无力。一开始,小玲的爸爸妈妈和她并没有把这当一回事,但很快小玲发现自己双腿都出现了无力症状,对温度的感知能力也下降了,她的爸爸妈妈赶紧带她到医院就诊,那一次,小玲被诊断为髌骨软化。进行一段时间的药物治疗后,小玲的情况并没有变好,依旧双腿无力,走路感觉像踩着棉花,原本最喜欢运动的她不能参加体育课上的跑步活动,也无法再和同学一起打羽毛球。于是爸爸妈妈带着她到了另一家医院,在那里,她做了脊椎的核磁共振,检查结果显示她的胸椎部位有一个肿瘤,怀疑是神经鞘瘤。你所不知道的神经鞘瘤神经鞘瘤又名许旺细胞瘤,是由周围神经的神经鞘所形成的肿瘤,亦有人称之为神经瘤,多为良性肿瘤。发生于前庭神经或蜗神经时亦被称为听神经瘤。患者多为30~40岁的中年人,无明显性别差异。常生长于脊神经后根,如肿瘤较大,可有2~3个神经根粘附或被埋入肿瘤中。神经根粗大,亦可多发于几个脊神经根。少数患者可伴有多发性神经纤维瘤病,可见患者皮肤上有咖啡色素斑沉着及多发性小结节状肿瘤。脊髓神经鞘瘤的大小通常为2~3厘米。脊髓神经鞘瘤常见临床表现有哪些?脊髓神经鞘瘤是椎管里最常见的一类肿瘤,而且多是良性肿瘤。其主要表现具体如下:1.神经根性疼痛,主要表现为上肢或者下肢疼痛,颈、肩、胸、背部疼痛。2.部分患者出现感觉障碍,肢体或者躯干部麻木、束带感。3.运动障碍,主要表现为肢体无力、走路不稳。4.直肠功能障碍,主要表现为排便困难、便秘。5.膀胱功能障碍,排尿费力、尿不尽、尿潴留。面对脊髓神经鞘瘤怎样治疗才更有效?如何治疗要看症状以及肿瘤大小,如果肿瘤比较小,没有明显的症状存在,是不需要进行处理的,定期的进行复查即可。而如果肿瘤对于神经造成压迫,那就需要治疗。治疗脊髓神经鞘瘤最有效的方法是手术治疗。手术难度大、要求高。由于神经根内瘤体与运动神经和感觉神经紧密相邻,因而,手术成功的关键在于能否彻底清除瘤体组织,更要竭尽全力保留运动和感觉神经,避免这些神经受到损害。大多数良性的脊髓神经鞘瘤均可通过手术全切而达到治愈,术后复发率很低。无论手术后效果如何,术后随访都是诊疗过程中非常重要的环节,患者要做到定期随访,不仅可以让患者得到更好的针对性指导和诊疗,还能时刻关注肿瘤的动态,以便及时干预治疗。
 贾栋医生的科普号
贾栋医生的科普号 2022年02月28日
2022年02月28日 235
235
 0
0
 0
0
-
脊髓肿瘤是否会转移?
脊髓肿瘤是否会转移到其他位置?什么样的会转移? 脊髓肿瘤一般很少会转移到其他位置。但也不排除其他情况,一般来说有这么几种转移方式。 【第一种】肿瘤细胞在椎管内从原来生长的地方直接掉到了下面的位置。比如肿瘤原来在胸椎的位置生长,后来肿瘤细胞脱落,掉到了下面的腰椎附近,就像是树上的果实掉到了下面的土地里,然后果实重新发芽生长,这叫做脱落转移。 【第二种】肿瘤不光往下掉,还会往上跑。椎管内浸润着脑脊液,脑脊液连通着大脑,形成脑脊液循环,脊髓就“泡”在脑脊液里。有些生长在胸腰椎的肿瘤,顺着脊髓,随着脑脊液往大脑里边钻,这种极其罕见。这说明肿瘤细胞具有游走能力,可以跑到很远的地方,比如脊髓胶质瘤。
 范涛医生的科普号
范涛医生的科普号 2022年02月14日
2022年02月14日 595
595
 0
0
 0
0
-
髓内肿瘤(胶质瘤,室管膜瘤)主要有哪些?
髓内肿瘤(胶质瘤,室管膜瘤)主要有哪些? 脊髓内肿瘤主要为星形细胞瘤及室管膜瘤,约占全部脊髓肿瘤的20%,往延伸若干脊髓节段,临床上表现可与脊髓空洞症相似。可发生进展性两下肢轻瘫,感觉丧失以及括约肌功能障碍。局限于一个节段的肿瘤在临床上可与一个髓外肿瘤很相似,但疼痛通常不显著,而括约肌功能障碍的症状出现较早。
 范涛医生的科普号
范涛医生的科普号 2022年02月14日
2022年02月14日 451
451
 0
0
 0
0
-
神经源性肿瘤是什么?好治吗?该看哪个科?(神经源性肿瘤的正确认识和规范化治疗)
经常有患者拿着影像学报告到我门诊问我:报告报的神经源性肿瘤是什么意思?可以治好吗?该看哪个科呢?在这里,我就具体来说说神经源性肿瘤的定义、就诊科室、治疗方法。1.什么是神经源性肿瘤?神经源性肿瘤本质上是中枢神经(脑、脊髓)或周围神经(颅神经、脊神经等)系统的神经细胞、神经纤维或神经束膜生长的肿瘤,是一类神经系统的肿瘤。肿瘤可以单发,也可以多发,多数为单发,任何年龄均可见,中青年常见。病理上良性占绝大多数,包括颅内、脊柱椎管内、椎管内外沟通性神经鞘瘤、神经纤维瘤和节细胞神经瘤,恶性的有恶性神经鞘瘤(神经性肉瘤)、节神经母细胞瘤和交感神经母细胞瘤。神经源性肿瘤有一个鲜明特点,就是肿瘤沿着神经根局部生长或向远端延伸生长,如突破脊柱椎间孔向椎管外生长,部分神经源性肿瘤可以长入胸腔、腹腔、盆腔。2.神经源性肿瘤应该看哪个科?人体解剖生理分八大系统(呼吸系统、消化系统、循环系统、神经系统、运动系统、内分泌系统、泌尿和生殖系统等等),神经源性肿瘤属于神经系统疾病,一定是神经外科、神经内科医生最专业,这需要深厚的专业学习背景和长期严格训练,而神经系统肿瘤性疾病主要以外科手术治疗为主,辅助以放射治疗和化疗等,故又以神经外科医生和治疗核心,神经外科治疗神经源性肿瘤可以达到最佳效果,这是毋庸置疑的。3.神经源性肿瘤如何规范化的治疗?长征医院神经外科戴大伟教授团队指出,目前唯一有效的治疗手段是显微或内镜神经外科手术切除。手术均在显微镜下或神经内镜下行肿瘤切除,达到对神经、血管和辅助支撑结构的最大程度的保护。(1)良性肿瘤手术治疗:良性肿瘤手术全切,疗效非常理想,不影响生活质量和远期寿命,对于不涉及脊柱稳定性者,显微或内镜手术切除加椎板复位;对于导致脊柱不稳者,显微或内镜手术切除加脊柱内固定。(2)恶性肿瘤手术治疗:恶性肿瘤尽量挽救神经功能,解除患者痛苦症状,最大程度延长生命,行肿瘤切除及去椎板减压;影响脊柱稳定性的恶性脊柱肿瘤,可手术行肿瘤切除及脊柱内固定,必要时术后辅助放化疗,减少种植转移和远期复发。(3)如合并神经功能障碍,术后可行规范化的康复治疗。
戴大伟医生的科普号 2022年02月07日
2022年02月07日 1476
1476
 0
0
 6
6
脊髓肿瘤相关科普号

张永超医生的科普号
张永超 主任医师
山东省立医院
神经外科
541粉丝1.9万阅读

贾栋医生的科普号
贾栋 主任医师
医生集团-陕西
神经外科
3830粉丝824.2万阅读

崔后春医生的科普号
崔后春 主任医师
扬州大学附属医院
骨科
1041粉丝7.2万阅读
-

 推荐热度5.0马骏鹏 副主任医师华西医院 神经外科
推荐热度5.0马骏鹏 副主任医师华西医院 神经外科椎管内肿瘤 173票
颈椎病 37票
小脑扁桃体下疝 18票
擅长:精准治疗各类脊柱脊髓肿瘤、椎管内外肿瘤(神经鞘瘤、脊膜瘤、室管膜瘤、血管母细胞瘤)、颅脑肿瘤(脑膜瘤、胶质瘤、脑转移瘤)、小脑扁桃体下疝畸形、脊髓空洞、寰枢椎脱位、颈椎病、椎间盘突出、腰椎滑脱、椎管狭窄、脑出血、脑外伤、颅骨缺损、三叉神经痛、面肌痉挛。尤其精通各类椎管内外肿瘤、椎间孔肿瘤、脊髓髓内肿瘤、各类哑铃型肿瘤、椎管狭窄、椎间盘突出和各类颅底畸形的精准微创治疗,精通脊髓电刺激治疗顽固性疼痛和促醒,在追求保护神经功能和脊柱稳定性的情况下提高了手术的全切率,依靠国际先进的理念、规范化的诊疗和精细的显微手术技术极大地提高了患者的手术疗效和满意度。 -
 推荐热度4.9蒋磊 副主任医师上海长征医院 神经外科
推荐热度4.9蒋磊 副主任医师上海长征医院 神经外科椎管内肿瘤 162票
垂体瘤 63票
脑膜瘤 51票
擅长:复杂及不同部位椎管内肿瘤如神经鞘瘤、脊膜瘤、髓内室管膜瘤、胶质瘤、椎管内外沟通性肿瘤、脊髓血管母细胞瘤、脂肪瘤、脊髓血管畸形的微创外科治疗,神经电生理监测条件下脊髓及马尾神经功能保护,功功能性及无功能性、侵袭性垂体腺瘤的微创内镜手术治疗,脑胶质瘤的综合治疗,高难度颅底肿瘤如岩斜区脑膜瘤、听神经瘤、三叉神经鞘瘤、胆脂瘤,三叉神经痛、面肌痉挛,难治性脑积水和颅颈交界畸形的显微外科治疗。 -
 推荐热度4.5吕立权 副主任医师上海长征医院 神经外科
推荐热度4.5吕立权 副主任医师上海长征医院 神经外科骶管囊肿 241票
椎管内肿瘤 78票
脑肿瘤 33票
擅长:神经外科疑难复杂病诊治。尤其擅长脑和脊髓肿瘤(椎管内肿瘤)、骶管囊肿、小脑扁桃体下疝畸形(Chiari畸形)、脊髓空洞、脊髓栓系、三叉神经痛、面肌痉挛微创手术。




