医学科普
发表者:张静 人已读
先天性肾上腺皮质增生症又称肾上腺生殖器综合征或肾上腺性变态征。主要由于肾上腺皮质激素生物合成过程中所必需的酶存在缺陷,致使皮质激素合成不正常。多数病例肾上腺分泌理糖激素、理盐激素不足而雄性激素过多,故临床上出现不同程度的肾上腺皮质功能减退,伴有女孩男性化,而男孩则表现性早熟,此外尚可有低血钠或高血压等多种症候群。
治疗:
1、及早应用氢化可的松或强的松。
2、应坚持终身服药。
3、手术治疗。
疾病描述
先天性肾上腺皮质增生症(CAH)是一组由于肾上腺皮质激素合成过程中酶的缺陷所引起的疾病,属常染色体隐性遗传病,引起男性化者又称肾上腺性征异常综合征。典型的CHA发病率约为10/10万,而非典型的发病率约为典型的10倍,并有种族特异性。[1]症状体征
本症以女孩多见,男女之比约为1:2,本病的临床表现取决于酶缺陷的部位及缺陷的严重程度,常见的有以下几种类型:
1、21—羟化酶缺乏症(ZD—OHD)
是先天性肾上腺皮质增生症中最常见的一种,占典型病例的90%—95%,21—羟化酶基因定位于第6号染色体短臂(6p21.3),与HLA基因族紧密连锁,由A基因(CYP21A)和B基因(CYP21B)两个基因座构成,CYP21B又称CYP2的,是21—羟化酶的编码基因:CIP21A又称CYP21p,是无功能的假基因。CYP2的基因突变,包括点突变、缺点和基因转换等,致使21—羟化酶部分或完全缺乏,由于皮质醇合成分泌不足,雄激素合成过多,致使临床出现轻重不等的症状。可表现为单纯男性化典型、失盐型、非典型型三种类型。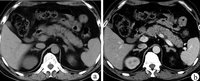 肾上腺皮质增生症(1)单纯男性化型(SV)
肾上腺皮质增生症(1)单纯男性化型(SV)
系21—羟化酶不完全缺乏所致,酶缺乏呈中等程度,11—脱氧皮质醇和皮质醇、11—脱氧皮质酮等不能正常合成,其前体物质17—羟孕酮、孕酮、脱氢异雄酮增多,但仍可合成少量皮质醇和醛固酮,故临床无失盐症状主要表现为雄激素增高的症状和体征。
女孩表现为假两畸形:由于类固醇激素合成缺陷在胎儿期即存在,因此,女孩在出生时即呈现程度不同的男性化体征,如阴蒂肥大、类似男性的尿道下裂,大阴唇似男孩的阴囊,但无睾丸,或有不同程度的阴唇融合。虽然外生殖器有两性畸形,但内生殖器仍为女性型,有卵巢、输卵管、子宫、患儿2—3岁后可出现阴毛、腋毛,于青春期,女性性征缺乏,无乳房发育和月经来潮。
男孩表现为假性性早熟,出生时无症状,生后4个月以后出现性早熟征象,一般1—2后外生殖器明显增大,阴囊增大,但睾丸大小与年龄相称。可早期出现阴毛、腋毛、胡须、痤疮、喉结,声音低沉和肌肉发达。 肾上腺皮质增生症男孩还是女孩运出现体格发育过块,骨龄超出年龄,因骨骺融合早,其最终身材矮小,由于ACTH增高,可有皮肤粘膜色素沉着。
肾上腺皮质增生症男孩还是女孩运出现体格发育过块,骨龄超出年龄,因骨骺融合早,其最终身材矮小,由于ACTH增高,可有皮肤粘膜色素沉着。
(2)失盐型(SW)
是21—羟化酶完全缺乏所致,皮质醇的前体物质如孕酮、17—羟孕酮等分泌增多,而醛固酮合成减少,使远端肾小管排钠过多,排钾过少,因为,患儿除具有上述男性化表现外,生后不久即可有拒食、呕吐、腹泻、体重不增加或者下降、脱水、低血钠、高血钾、代谢性酸中毒等。若治疗不及时,可因循环衰竭而死亡。女性患儿出生时已有两性畸形,易于真吨,男性患儿诊断较为困难,常误诊为幽门狭窄而手术或误诊为婴儿腹泻而耽误治疗。
(3)非典型型(NC)
亦称迟发型、隐匿型或轻型,是由于21—羟化酶轻微缺乏所致。本症的临床表现各异,发病年龄不一。在儿童期或青春期才出现男性化表现。男孩为阴毛、性早熟、生长加速、骨龄提前;女性患儿可出现初潮延迟、原发性闭经、多毛症及不育症等。
2、11β—羟化酶缺陷症(11β—OHD)
约占本病的5%—8%,此酶缺乏时,雄激素和11—脱氧皮质酮均增多,临床表现出与21—羟化酶缺乏相似的男性化症状,但程度较轻,可有高血压和钠潴留,多数患儿血压中等程度增高,其特点是给予糖皮质激素后血压可下降,而停药后血压又回升。
3、3β—羟类固醇脱氢酶缺乏症(3β—HSD)
本型较罕见,该酶缺乏时,醛固酮、皮质醇、睾丸酮的合成均受阻,男孩出现假两性畸形,如阴茎发育差、尿道下裂。女孩出生时出现轻度男性化现象。由于醛固酮分泌低下,在新生儿期即发生失盐、脱水症状,病情较重。
4、17—羟化酶缺乏症(17—OHD)
本型亦罕见,由于皮质醇和性激素合成受阻,而11—脱氧皮质酮分泌增加,临床出现低钾性碱中毒和高血压,由于性激素缺乏,女孩可有幼稚型性征、原发性闭经等,男孩则表现为男性假两性畸形,外生殖器女性化,有乳房发育、但患儿有睾丸。
疾病病因
肾上腺皮质由球状带、束状带、网状代组成。球状带位于最外层,约占皮质的5%~10%,是盐皮质激素—醛固酮的唯一来源,束状带位于中间层,是最大的皮质带,约占75%,是皮质醇和少量盐皮质激素(脱氧皮质酮、脱氧皮质醇、皮质酮)的合成场所,网状带位于最内层,主要合成肾上腺雄激素和少量雌激素。正常肾上腺以胆固醇为原料合成糖皮质激素、盐皮质激素、性激素(雄、雌激素和孕激素)三类主要激素,都是胆固醇的衍生物。其过程极为复杂,每一步骤都比较经过一系列酶催化,有些酶是合成这一类激素或其中两类激素的过程中所共同需要的。肾上腺合成皮质醇是在垂体分泌的ACTH控制下进行的,先天性肾上腺皮质增生症时,由于上述激素合成过程中有不同部位的酶缺陷致使糖皮质激素、盐皮质激素由于血皮质醇水平降低,负反馈作用消除,以致垂体前叶分泌ACTH增多,刺激肾上腺品质增生,并使雄激素和一些中间代谢产物增多,由于醛固酮合成和分泌在长见类型的CAH中亦缺陷有:21—羟化酶(CYP21)、11β—羟化酶(CYP17)、3β—羟类乙醇脱氢酶(3β—HSD无)、18—羟化酶(CYP11B2)等。
诊断检查
(一)生化检测
1、尿液17—羟类固醇(17—OHCS)、17—酮类固醇(17—KS)和孕三醇测定,其中17—KS是反映肾上腺皮质分泌雄激素的重要指标,对本病的诊断价值优于17—OHCS。肾上腺皮质增生症患者17—KS明显升高。
2、血液17—羟孕酮(17—OHP)、肾素血管紧张素原(PRA)、醛固酮(Aldo)、脱氢异雄酮(DHEA)、脱氧皮质酮(DOC)及睾酮(T)等的测定,17—OHP基础值升高是21—羟化酶缺乏的特异性指标,它还可用于检测药物剂量和疗效。
3、血电解质测定:失盐型可有低钠、高甲血症。
(二)其他检查
1、染色体检查
外生殖器严重畸形时,可做染色体核型分析,以鉴别性别。
2、X线检查
拍摄左手腕张支骨正位片,判断骨龄,患者骨龄超过年龄。
3、B超或CT检查
可发现双侧肾上腺增大。
4、基因诊断
采用直接聚合酶链反应,寡核苷酸杂交,限制性内酶片段长度多态性和基因讯序列分析可发现相关基因突变或缺失。
治疗方案
治疗本病的目的:①纠正肾上腺皮质激素缺乏,维持正常生理代谢,②抑制男性化,促进正常的生长发育。
1、及时纠正水、电解质紊乱(针对失盐型患儿)
静脉补液可用生理盐水,有代谢性酸中毒则用0.45%氯化钠和碳酸氢钠溶液。忌用含钾溶液。重症失盐型需静脉滴注氢化可的松25—100mg,若低钠和脱水不易纠正,则可肌肉注射醋酸脱氧皮质酮(DOCA)1—3mg/d或口服氟氢可的松0.05—0.1mg/d,脱水纠正后,糖皮质激素改为口服,并长期维持,同时口服氯化钠2—4d/d。其量可根据病情适当调整。
2、长期治疗
(1)糖皮质激素
糖皮质激素治疗一方面可补偿肾上腺分泌皮质醇的不足,一方面可抑制过多的ACTH释放,从而减轻雄激素的过度产生,故可改善男性化、性早熟等症状,保证患儿正常的生长发育过程。一般氢化可的松口服量为每日10—20mg/m2,2/3量睡前服,1/3量早晨服。
(2)盐皮质激素
盐皮质激素可协同糖皮质激素的作用,使ACTH的分泌进一步减少。可口服氟氢可的松0.05—0.1mg/d,症状改善后,逐渐减量,停药。因长期应用可引起高血压。0.1mg氟氢可的松相当于1.5mg氢化可的松,应将其量计算于皮质醇的用量中,以免皮质醇过量。
在皮质激素治疗的过程中,应注意监测血17—羟孕酮或尿17—酮类固醇,失盐型还应该监测血钾、钠、氯等。调节激素用量,患儿在应激情况下(如:感染、过度劳累、手术等)或青春期,糖皮质激素的剂量应比平时增加1.5—2倍。
3、手术治疗
男性患儿勿需手术治疗。女性两性畸形患儿宜6个月—1岁阴蒂部分切除术或矫形术。
疾病预防
1、新生儿筛查
运用干血滴纸片法,经ELSA、荧光免疫法测定17—OHP可筛查21—OHD。
2、产前诊断
(1)21—OHD:在孕9—11周取绒毛膜活检进行胎儿细胞DNA分析,孕16—20周取羊水检测孕三醇,17—OHP等,因大部分非典型21—OHD患儿生后17—OHP水平无明显升高,因而基因检测是此型患儿童唯一早期诊断手段。
(2)11β—OHD:主要测羊水DOC及取绒毛膜作相关基因分析进行诊断。
本文为转载文章,如有侵权请联系作者删除。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅
发表于:2014-11-06