胡润磊医生的科普号
- 精选 分享不太典型的肺结节1例
肺Ca的影像学表现多种多样!28岁的小伙3月前CT提示右上肺小结节,不典型混合型磨玻璃样改变,予以随访,复查变化不明显,患者走访了杭州、上海多家医院,认为是炎症的居多。但是我始终认为结节有空泡征,恶性
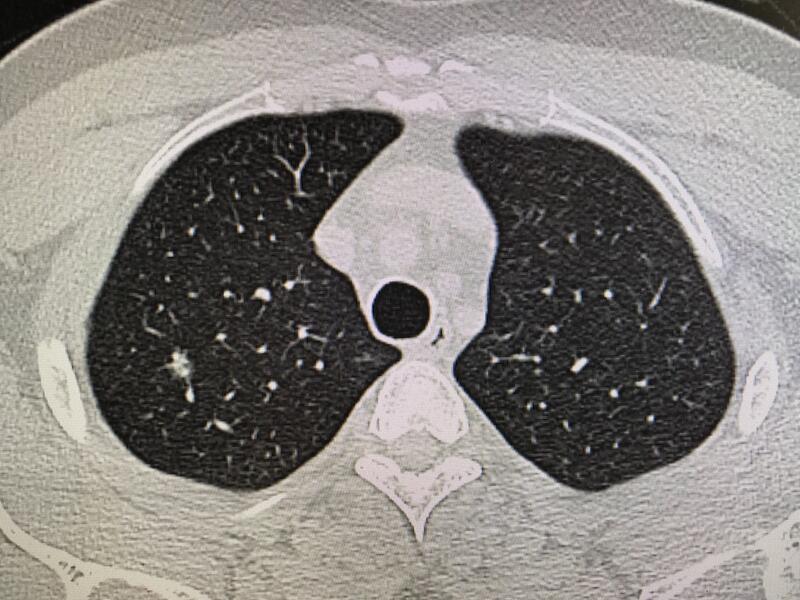 胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科1611人已读
胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科1611人已读 - 精选 成功将中央型巨大肺癌切除,并保留了肺功能
1例左下肺中央型鳞癌患者,斜裂不发育,肿瘤侵犯下叶支气管和上叶舌段支气管,切除左下肺叶和上叶舌段,两根气管根部均成型,切缘均阴性!保留了固有段,避免了全肺和袖切,由于固有段不太大,担心术后扭转,结果术后胸片提示固有段复张相当好
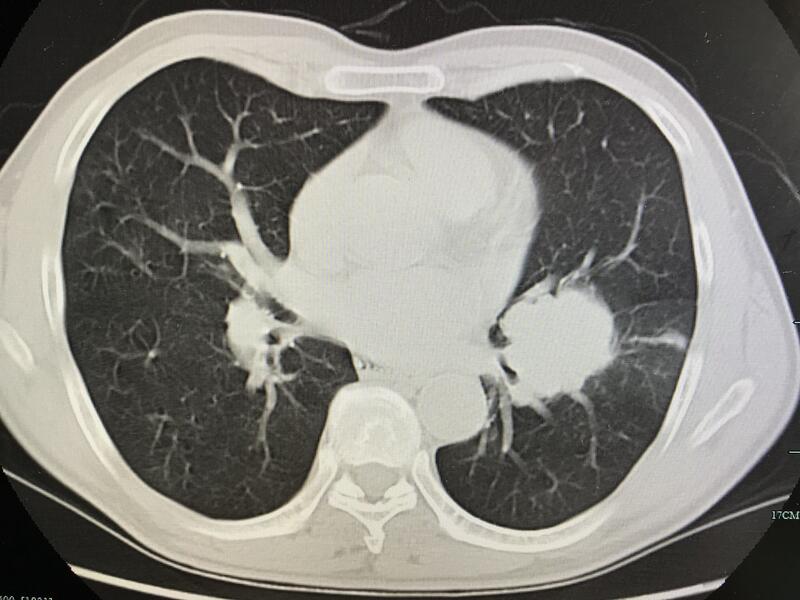 胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科1842人已读
胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科1842人已读 - 精选 肺部小结节手术时机还是要慎重点
张先生是一家公司的职员,往年每年都安排健康体检一次,胸片检查提示肺部未见明显异常,今年体检是3个月前,做了胸部CT,结果提示左上肺混合性磨玻璃结节,直径约8mm。张先生一下子吓蒙了。因为他们单位这几年有好几个人肺部结节而接受了手术治疗,病理结果都是肺癌。于是张先生拿着片子看了好几家大医院,几乎一致认为恶性可能性大,建议手术治疗。张先生下不了决心,找到我院心胸外科胡润磊副主任医师。胡主任仔细阅读了片子,虽然片子看上去是典型的混合性磨玻璃结节,有明显的实性成分,从影响学上首先考虑恶性肿瘤,但是由于患者是首次发现,而且直径没有超过8mm,出于谨慎的态度,还是建议观察,3个月后再复查,如果复查结节没有缩小,再手术也不迟。张先生听取胡主任的意见,3个月后再次复查,结果左上肺磨玻璃结节基本上消失了。张先生绷紧的心一下子放松了,连声说谢谢,感谢胡主任“刀下留人”,避免了白挨一刀。上图为3月前CT提示左上肺混合性磨玻璃结节;下图提示3个月后复查结节基本消失
胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科2.1万人已读 - 精选 微创治疗并非切口越小越好
微创治疗,不能仅停留在切口小这个层面上。在2017胸部肿瘤规范化治疗上海国际论坛的间隙,上海复旦大学附属肿瘤医院胸外科主任、胸部肿瘤多学科诊治组首席专家、肺癌防治中心主任陈海泉教授接受了澎湃新闻(ww
胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科1704人已读 - 精选 EACTS:脓胸外科治疗专家共识
胸膜腔感染是一个常见的临床疾病,在英国和美国每年约有 8 万例患者。其中 20% 的患者需要外科干预和进一步治疗,从而降低住院费用,并发症发生率和死亡率。目前,临床关于脓胸的治疗已取得很大进展。近日,
胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科2863人已读 - 精选 中国手汗症微创治疗专家共识
胸腔镜下行胸交感神经切断术(endoscopic thoracic sympathicotomy,ETS)是治疗手汗症惟一有效的微创方法。近年来,随着社会经济高速发展和年轻人对生活质量的高要求,要求手术的患者日益增多。ETS 手术效果良好,施行手术的单位也积累了较多经验。同时我们也注意到对于手汗症微创治疗中的许多问题仍然存在一些模糊的认识,如手术适应证、胸交感神经干切断水平及其术式、术后代偿性多汗的防治以及术后随访等均亟待进一步的研究、总结和提高。针对这些问题,根据中华医学会胸心血管外科分会胸腔镜外科学组的倡议,我们于 2009 年 3 月成立了「中国手汗症微创治疗协作组」,并在福州召开首届专题研讨会,与会专家就规范手术方法、规避手术风险、进一步提高疗效以及减少手术并发症等问题进行了深人的探讨,达成初步共识。两年来这些共识几经完善,得到越来越多的认同,现公布供同道们参考。手术适应证与禁忌证已明确诊断的中度(出汗时湿透一条手帕)、重度(出汗时手掌呈滴珠状)的手汗症病例是手术适应证,轻度病例则不必考虑手术。推荐 12-50 岁为 ETS 手术的最佳年龄。12 岁以下儿童不建议接受此项手术,待到上中学年龄以后,病人及家属确定严重影响学习生活,要求治疗者再行考虑。50 岁以上病人可能因主动脉硬化扩张甚至弯曲覆盖交感神经干导致术中寻找困难。术前必须认真询问病史,应排除甲状腺机能亢进症或结核等疾病;患者及家属应该具有强烈手术愿望;建议不同期施行两种手术,如附加肺大疱或肺结节切除等;对于严重心动过缓、胸膜粘连、胸膜肥厚和既往胸腔手术视为手术禁忌;神经质者最好不施行手术。手术前准备术前常规检查包括抽血化验、心电图、X 线胸片或胸部 CT 平扫。化验检查方面应做血常规、肝肾功能检查、电解质分析、凝血分析和必要的传染病筛查;如近期有感冒、发热、咳嗽等上呼吸道症状或恶心、呕吐、腹泻等消化道不适等均应推迟手术。麻醉与手术操作ETS 的主要特点是在全身麻醉下采用胸部微创方法,即通过两侧腋下 1-3 个微小切口(即一孔法、二孔法和三孔法)施行。一孔法使用的是 10 mm 单孔胸腔镜、经肋间纵隔镜或「Y」形胸膜活检镜;三孔法一般是因某种原因术中操作困难时施加的一个切口。麻醉和腔镜术者可根据自己的经验、设备和条件选择,没有必要作硬性规定。但必须指出,手术应由经验丰富的医师操作,切不可疏忽大意。以下是标准的二孔法手术操作。1. 麻醉根据本单位实际情况和条件选择双腔插管、单腔插管、喉罩或者面罩通气全身麻醉。不是双腔气管插管者,手术时需停止通气 3-5 min,使肺尖部自然塌陷,显露术野,其间严密监护脉搏、心率及血氧饱和度,若血氧饱和度降低至 0.90 以下,或停止通气超过 5 min,应立即暂停手术操作,恢复通气待血氧饱和度上升至 0.95-1.00 后,再重新停止通气进行手术操作。2. 体位采用仰卧,上半身抬高 30°至 45°,双上臂外展与胸壁成 90°并固定于手架上,暴露双侧腋窝。3. 切口腋中线第 5 肋间做一个 1.0 cm 切口,请麻醉师停止通气后,插入 trocar 并置入胸腔镜,在胸腔镜引导下于腋前线第 3 肋间另做一个 5 mm 切口置入 trocar 为操作孔,经此孔置人电凝钩,通过监视器进行操作。切口位置的选择和大小可由术者根据自己的经验和习惯适当调整。4. 操作胸腔镜进人胸腔后,先辨认上胸腔解剖结构,由于第 1 肋骨,尤其是后肋部分往往被黄色脂肪垫等软组织被覆,故胸顶处可以看到的即为第 2 肋骨,交感神经链位于肋骨小头外侧旁与脊柱平行,呈白色索条样,多数直径约 2-3 mm,用电凝钩轻触滑动可感知。在第 3 肋骨表面(T3 切断)或第 4 肋骨表面(T4 切断)将相应神经干电凝灼断。切断后的神经断端应轻轻点烧一下,保证两断端有约 3-5 mm 的距离,防止以后再生复发。另 外,为了消除可能存在的 Kuntz 束及侧支,应将切开范围向交感干内、外侧做适当延伸,尤其是向外侧延伸至少应达 2 cm,以保证神经主干和侧支均能完整切断。术中应仔细检查,确认切断的是神经主干而非侧支。术毕仔细检查术野确认无活动性出血,在胸腔镜监视下,从另一切口置入 16F 细管,一端置于胸顶,另一端在体外浸人牛理盐水碗(杯)中,构成临时胸腔闭式引流管。嘱麻醉师鼓肺充分排气后拔除,缝合切口。一侧术毕,再同法施行对侧手术。只要止血彻底,肺组织未发生损伤,不必留置胸管。术式与切断平面及其效果胸腔镜上胸段交感神经手术的方式主要有切除术、切断术和交通支切断术 3 种。在多汗症治疗中,切除术已被废除;交通支切断术因效果不佳未获推广;目前公认交感干切断术为主流术式。阻断交感干的方法有电凝灼断、钛夹夹闭、超声刀切断;我们推荐简单有效的电凝灼断为首选,后二者方法神经阻断不够确实,效果欠佳,不宜推广。手术切断平面目前尚未统一,我们主张 T3 或 T4 单段切断加旁路神经烧灼,不提倡多段切断。T2 切断术常会引起严重代偿性多汗,目前多不再建议行此手术。术中及术后监护术中应严密监测心率、心律和血氧饱和度。有条件的单位还可行掌温监测。交感神经切断后,同侧掌温一般会上升。故掌温变化可以作为神经切断与否的一个参考指标。个别患者术毕拔管后可能出现一过性呼吸不畅,可在复苏室吸氧观察。返冋病房后须做心电及血氧饱和度等监护至次日。术后当晚或第 1 天复查 X 线胸片,如肺复张良好,无液气胸表现一般即可出院。手术并发症及防治尽管 ETS 是典型的微创手术,但其同样也会发生并发症。常见的并发症有以下几点。术中出血术中出血通常是分离胸交感神经干时来自肋间动、静脉或奇静脉属支的损伤,也有来自 trocar 进胸处的肋间血管出血等。右胸交感乃或 T4 神经干更贴近奇静脉属支,其表面可能有小静脉穿过,操作时要非常小心。在 T3 附近,有时有纵横交错呈爪状分布的静脉分支,交感神经可能掩藏在血管间隙中,可先在靠近神经干的两侧无血管区域(有时仅电凝钩头大小区域)电灼壁层胸膜,然后将隐约可见的神经干用电凝钩头挑出电灼切断;另一方法是先在神经干的一侧用电凝钩稍用力将神经干向另一侧边推移边电灼。在 T4 附近,静脉分支往往较少且更偏近内侧,与交感干有一定距离,但有时会有肋间动脉的起始段斜行跨过第 4 肋骨巨与交感干并行。我们推荐,在行 T4 切断时可不必游离挑起神经,而是将电钩紧贴肋骨表面,连同壁层胸膜和交感神经一并灼断。遇到有并行的肋间动脉时,可采用从血管两侧逐步靠拢的办法予以电凝灼断,一般不会引起出血。这样做可以切断藏于血管深面的神经分支,保证手术效果。当然,遇到较粗血管时,也要慎重地予以保留。一旦出血,切不可慌乱盲目烧灼电凝,应立即用内镜钳钳夹电凝止血,或夹取小纱布球压迫止血,一般均成功。2. 心脏骤停有个别报道术中出现心脏骤停或术后出现严重心动过缓需起搏器维持的情况。在开展这一手术时必须有所警惕,尤其在做左侧交感神经链切断手术时,因为该侧是心脏支配的优势侧,切断后可能对心率有一定的影响,故手术应先在右侧施行。手术时应高度注意患者的心率、心律及血压的变化。不过多数研究认为,该手术对心血管系统的影响尽管存在,但一般均比较微弱,尤其是目前采用的较低位置单一节段切断术更是如此。3. 霍纳综合征表现为眼睑下垂、眼球内陷、瞳孔缩小、伤侧面部无汗,这是 ETS 的严重并发症,主要是术中因辨认不清损伤或烧灼交感神经干时热传导波及星状神经节所致。近年开展 T3 或 T4 以来,这种并发症已十分罕见。4. 一过性手掌多汗一过性多汗多发生于术后 1 周内,表现为无任何诱因手掌多汗症状「复发」,与术前相似甚至更严重,出现时间不分白昼,持续数分钟至数小时不定,一日可反复发作数次,数天后即自愈。其发生机制未明,可能是汗腺去交感神经支配后,残存的神经递质释放,或效应器在 1 周内出现「敏感化」或「反跳」而引起汗腺过度分泌。代偿性多汗现象与对策代偿性多汗一般被称为术后副作用(side effect),是上胸段交感神经切断后最常见的并发症,发生机制不明。目前研究己证实,减少交感神经切断范围或降低切断节段可以减少这一副作用。T4 切断术是迄今认为最少出现代偿性多汗的术式。代偿性多汗主要表现为术后没有去交感神经支配的部位,如胸部、腹部、背部、臀部、大腿及小腿出汗比术前明显增加,头面部和足部不会出现代偿性多汗。其诱因主要是高温或活动后,有时静息状态下也可能出现。发生率报道差异很大,可在 10%-80%,大约 3%-5% 病人与情绪激动或精神紧张有关。术后代偿性多汗的分级标准可参考表 1。表 1. 代偿性多汗的参考标准轻度出汗量少,汗液不成滴,不流淌,不产生明显不适感或轻度不适,患者可以忍受,一日之内不需因出汗而史换衣服中度中等量出汗,汗液可汇成滴并流淌,患者有明显不适感,但可以忍受,一日之内不需因出汗而更换衣服重度出汗量多,汗液流淌,严重影响正常生活、工作, 患者感觉尴尬,难以耐受,一天内需一次或多次更换衣服轻度者一般不引起不适症状;中度病人经过较长一段时间的适应和心理调整后能够耐受,不影响术后生活质量;但仍有个别病人因此引起不适和生活困扰,这是此项手术术后患者不满意的主要原因。重度代偿性多汗在现有术式的术后病人中很少见,出现时可能会令患者后悔手术。代偿性多汗的发生. 机制目前尚未明确,一旦出现也无有效治疗措施,对于这一点,一定要作为术前谈话的主要内容之一,要让患者有充分的思想准备。术前谈话或告知由于 ETS 手术技术成熟,迷你美容切口,手术效果显著,并发症少,术后恢复快,住院时间短和费用比较经济等原因,故而要求手术治疗的患者越来越多。但是,我们必须清醒认识到,任何一种手术都有利和弊,尽管这种手术获得 98% 以上术后患者的满意,但仍然有个别患者不满意或后悔手术,甚至在网上恶意炒作造成不利影响。因此,医师和患者及家属进行术前谈话或告知尤为重要。关于术后复发:术后复发非常少见,最主要的原因可能是神经走行变异所致,对这种情况可以通过再次施行交感神经手术获得治愈。关于腋汗和脚汗:腋汗和脚汗也足多汗症的一种局部表现。施行 ETS 后确实有一部分患者腋汗和脚汗也消失或减轻,但也有患者未缓解甚至加剧,这点也要加以说明。关于狐臭:是腋窝大汗腺过度发育产生的一种异常发臭的体液,尽管 ETS 后可能使汗液减少,但不能根治,这点也应加以说明。关于头汗症:手术必须切断 T2 才能有效,但是术后可能会发生严電的代偿性多汗,术者和患者必须慎之又慎。目前可尝试 T3 切断术用于头面多汗症的治疗。关于面红症(社交恐怖症):临床主要表现为某种情景下,患者因为害羞、胆怯、不安,而出现脸红和出汗等现象。国外有人采用 ETS 治疗,收到一定疗效,但这种情况属精神心理疾患,应以心理治疗为主,手术应慎重选择。最后需要强调的是,手汗症是一种仅仅影响病人情绪和生活质量的良性疾患,对人基本的健康状态和预期寿命等一般没有任何影响。而交感神经手术是一种有创的干预手段,对人体植物神经系统会产生一些不可逆的干扰,当然,这种干扰或许很轻微,但是否会对人体的机能状态产生细微的或很远期的影响,目前尚无清晰的认识。故此,建议开展此项技术的同道们,一方面,术中操作要认真、仔细、规范,尽可能减少对神经干的无谓「破坏」;要意识到,这类病人是很难接受诸如术中出血、中转开胸、术后血气胸等这些看似平常的并发症;另一方面,术后要与病人保持密切联络,长期甚至终身随访,以获得更多、更细的第一手伯息,为这一治疗措施未来更加完善做出我们自己的贡献。文章摘自:《中华胸心血管外科杂志》
胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科2167人已读 - 精选 概述:胸腺肿瘤分期的历史及进展
胸腺上皮肿瘤是比较少见的原发性纵隔肿瘤。因发病率低,目前缺少一个由Unionfor International Cancer Control(UICC)和the American Joint Commission on Cancer(AJCC)发布的官方分期系统。现有的分期系统种类繁多,争议较大,也未得到临床的验证,难以指导临床治疗策略的选择,也不利于术后的管理和判断预后,阻碍了该类疾病的研究进展。目前国际胸腺恶性肿瘤兴趣组(International Thymic Malignancy Interest Group,ITMIG)和国际肺癌研究协会(International Association for the Study of Lung Cancer,IASLC)正联合着手制定一个广泛的、统一的、操作性强的胸腺恶性肿瘤新分期系统。胸腺上皮肿瘤(Thymic epithelial tumors,TETs)是罕见的原发性纵隔肿瘤,起自胸腺的上皮组织,包括胸腺瘤、胸腺癌和神经内分泌肿瘤(NETs),约占前纵隔肿瘤的50%,占所有肿瘤的比例不到1%,因此也被称为孤儿病(orphan diseases)。该疾病临床进程缓慢,存在多种组织学特征及生物学行为,其病因学到目前为止仍不清楚。外科手术是主要的治疗方法,化疗和放疗也经常应用。文献显示[1-2],彻底的手术切除、组织学类型和肿瘤分期是该病的相关预后因子。1.胸腺肿瘤分期的历史从1978年至今,至少提出了15种以上的胸腺肿瘤分期方案[3],大体上可分为两大类:1.非-TNM的分期系统最早可追溯到1960年,胸腺瘤被分为侵袭性和非侵袭性两大类[4]。1978年,Bergh[5]根据症状、肿瘤的范围和组织学类型首次提出胸腺瘤的分期,将胸腺瘤分成三期(见表1),提出了彻底的肿瘤切除(R0)与好的生存有关。1979年wilkins和Castleman[6]也强调了彻底的手术切除是最重要的预后因素,10年的生存率可达到68%,并在Bergh分期的II期中增加了纵隔胸膜或心包侵犯,指出肿瘤的浸润性生长是一个不利的预后因素。表1 Bergh分期分期描述I具有完整的包膜或包膜内生长II包膜外生长侵犯到纵隔脂肪组织III侵袭性生长侵犯周围器官和(或)胸腔内转移1981年Masaoka总结了1954-1979年在日本大阪医学院就诊的93例胸腺瘤病人的资料,提出了Masaoka分期[7](表2),这也是迄今为止应用最广泛的分期系统。该分期将胸腺瘤分为4期,其中Ⅰ、Ⅱ期可以行彻底的手术切除(R0),而大部分Ⅳ期的胸腺瘤病人(8/11)仅能行部分切除手术(减瘤手术)。该分期强调了临床特征的重要性,提出了胸腺瘤临床进程的惰性,从最初局部组织浸润到后期通过淋巴或血运转移,其生存率逐步下降。回顾性研究得出R0切除的3年和10年的生存率分别为89%和75%,提示肿瘤的外侵和彻底的手术切除是重要的预后因子。与Berg和Wilkins分期的区别在于对II期外侵的描述上,认为应该正确区分宏观肉眼所见的侵犯至胸腺周围脂肪组织或纵隔胸膜与微观病理学上观察到的包膜受侵,事实上界定侵犯或纤维粘连有时是比较困难的[8]。表2 Masaoka分期分期描述I肉眼可见肿瘤在包膜内生长,显微镜下观察肿瘤并未侵犯包膜IIab肉眼可见肿瘤侵犯至周围脂肪组织或纵隔胸膜显微镜下观察肿瘤侵犯包膜III肿瘤侵犯周围脏器(心包、大血管或肺)IVab胸膜或心包播散淋巴或血运转移1985年,Verley和Hollmann结合术中肿瘤外侵情况和手术切除程度提出了新的分期方案[9],该方案强调了胸腺瘤外侵对于预后的重要性。研究发现胸腺瘤不外侵与外侵5年和10年的生存率分别为85%和80%和50%和35%,随着肿瘤外侵的程度增加,生存率逐步下降。1991年Gamondes等提出了GETT(The Groupe d’Etude des Tumeurs Thymiques)分期方案[10],该分期是基于法国巴黎地区11家医疗机构共识的基础上得出的,目前仍在法国的一些医疗机构沿用[11]。该分期是结合了Masaoka的宏观评估和外科手术切除的情况综合考虑的。根据他们的分期,胸腺瘤5年和10年的生存率分别为,Ⅰ期96%、88%,Ⅲ期84%、56%,Ⅳ期73%、18%,得出的结论是肿瘤分期和彻底的手术切除是主要的预后因子。1994年,Koga在Masaoka分期的基础上进行了改进,将其中的一些内容进行了简化,部分情形得到了降期[12](表3)。Koga认为显微镜下的包膜受侵并不是真正意义上的外侵,除非肿瘤真正突破了包膜,将原来Masaoka分期中Ⅱb期降到了Ⅰ期。并对Masaoka分期中Ⅱa和Ⅱb期进行了重新定义,将显微镜下外侵突破了包膜定为Ⅱa期,肉眼可见侵犯到周围脂肪组织定义为Ⅱb期。后期统计的生存曲线显示,Masaoka-koga分期中Ⅰ期与Ⅱ期,Ⅲ期与Ⅳ期没有差别,高分期中肿瘤复发和死亡率更高,因此作者认为4期的分期系统又可以简化为有外侵(Ⅲ期/Ⅳ期)和无外侵(Ⅰ期/Ⅱ期)两大类胸腺瘤。值得一提的是Masaoka-koga分期是目前唯一通过了大样本(1320例)验证的分期系统[13],也是目前ITMIG和IASLC组织制定新分期过程中建立数据库的基础。2003年,Asamura[14]认为包膜受侵不影响生存,提出应根据胸腺上皮肿瘤的直径和侵犯周围结构/器官的数量来进行分期。侵犯的结构/器官的类型和数量决定了手术能否切除彻底。Asamura将Masaoka-koga分期中Ⅰ、Ⅱ期合并为Ⅰ期,定义为:不管是否有包膜侵犯,肿瘤局限于两侧的纵隔胸膜内;拆分了Masaoka-koga分期中的Ⅲ期,并根据肿瘤大小和侵犯结构/器官的数量重新定义了Ⅱ期和Ⅲ期,Ⅳ期与Masaoka分期相同。表3:Koga(Masaoka-Koga)分期分期描述Ⅰ肿瘤明显位于包膜内以及显微镜下观察肿瘤侵犯但尚未突破包膜Ⅱab显微镜下肿瘤突破包膜肉眼可见肿瘤侵犯胸腺或周围脂肪组织或与心包及纵隔胸膜黏连紧密但尚未突破心包及纵隔胸膜Ⅲ可见肿瘤侵犯周围脏器(心包、大血管或肺)Ⅳab胸膜或心包播散淋巴或血运转移2011年,ITMIG为建立一个官方统一的胸腺恶性肿瘤新分期,在Masaoka-Koga分期的基础上建立了数据库。召集了国际上相关领域的专家对Masaoka-Koga分期的细节进行了阐述和明确[15],以使各中心来源的数据具有统一性和可比性。Moran等[16]2012年也提出了一个4期的胸腺瘤分期系统。与别的分期不同的是这里提出了0期的概念。Moran分期中的0期对应于MasaokaⅠ期中的包膜内肿瘤,并提出0期的胸腺瘤可能是一个“原位癌”或者“癌前病变”[17]。Moran分期中的Ⅰ期、Ⅱ期、Ⅲa期、Ⅲb期分别对应于Masaoka分期中的Ⅱ期、Ⅲ期、Ⅳa期、Ⅳb期。该分期对“包膜内”、“胸膜、心包外侵”等概念进行了明确的定义。2.TNM的分期系统胸腺瘤淋巴转移和血运转移的比例分别为2%、1%,局部侵犯是胸腺瘤最常见的扩散方式;胸腺癌/神经内分泌肿瘤则更多的表现为淋巴转移(25%)和血运转移(12%),因此,对于这类的肿瘤,似乎更适合应用TNM分期系统。1988年,Yamakawa将Masaoka分期改进为TNM系统[18]。T的描述沿用了Masaoka的标准;前纵隔淋巴结受侵被定义为N1;无血运转移为M0,有血运转移为M1。该研究中,作者未发现肿瘤的大小与预后相关。Tsuchiya于1994年专门针对胸腺癌(Thymic carcinoma,TC)提出了一个TNM分期系统[19],N的描述与Yamakawa的相同,将肿瘤侵犯到纵隔胸膜或者心包定义为T3,强调了淋巴结转移在分期中的作用。虽然研究中发现Ⅰ与Ⅲ、Ⅳ期以及Ⅲ期与Ⅳ期之间的生存曲线分的很开,但是由于样本量太小(仅16例),统计学并未显示出差异。2004年WHO针对TET肿瘤发布了TNM的分期[20]。肿瘤侵犯包膜和生长至周围器官/结构决定了T的分期,是否侵犯可以由外科医生或病理医生来评估;其淋巴结分类的定义与其他肿瘤的TNM分期类似,可惜的是,与N1-N3淋巴结分组的相关性并没有研究过。Bedini等[21]2005年提出了另外一个针对TET肿瘤的TNM分期系统,该分期在T和N的定义上做了比较详细的描述。主要特征为:(1)侵犯纵隔胸膜为T3;(2)侵犯周围器管(胸骨、大血管、肺等)为T4;(3)侵犯胸膜-心包,但仅为前心包受侵并可完整手术切除的定义为T4(以往被定义为M1a),(4)锁骨上或前斜角肌淋巴结转移为N3(以往胸腔外的淋巴结被定义为M1b),(5)对于不能完整手术切除仅行减瘤手术的R2又进行了亚组分析[20-22]。这样的分期对临床选择治疗策略有一定的指导意义:(1)局限性胸腺瘤建议行完整手术切除;(2)局部晚期病例,需要行扩大手术切除;(3)出现全身性转移的病例,很少行扩大手术切除,一般行化、放疗治疗。2012年Weissferdt和Moran针对TC也提出了一个3分期的TNM方案[17]。其中将肿瘤局限于胸腺内定义为T1,肿瘤侵犯脏层胸膜、肺、心包、大血管、胸壁或膈肌为T2,肿瘤直接生长至胸腔外但淋巴结仍局限在胸腔内的为T3,局部淋巴结转移为N0,胸腔外淋巴结转移为N1,任何T3、N1或M1都被定义为Ⅲ期。以上胸腺瘤的分期特征和总结见表4表4胸腺分期系统的概述2.胸腺肿瘤分期的现状当前胸腺肿瘤的分期主要依靠单中心、回顾性研究,更多的是依靠经验,由于病例数量有限,很难去验证这些分期的效果,缺少依据的支持导致了临床上分期应用的混乱。我们知道,一个统一的分期是全世界不同机构医生之间信息交流和不同中心间临床试验合作的基础,而胸腺肿瘤至今没有一个官方统一的、公认的分期方案;即使不同中心应用了同一种分期方案,也由于方案中分期的定义和描述很含糊,甚至模棱两可,导致了各中心理解的差异,数据之间的可比性较差,既不能指导胸腺肿瘤的治疗策略,也不能提供一个科学的术后管理和预后判断,阻碍了胸腺肿瘤这类疾病的研究和进展。3.胸腺肿瘤分期存在的问题现有胸腺瘤的分期比较混乱,各分期之间既有些相似之处,也存在着差别甚至有矛盾的地方。目前应用最广泛的Masaoka-koga分期,其定义描述简单、言辞含糊,导致了临床应用时的差异。主要集中在:(1)transcapsular invasion的确切含义是什么?(2)缺少完整的包膜应该被分到哪一期?(3)如何区分纵隔胸膜、心包的“macroscopic invasion”和“adherence”?(4)“adherence”的确切含义是什么?(5)纵隔胸膜或心包的“invasion of”和“breaking through”对应的是不同的分期,区别是什么?(6)部分胸腺癌或神经内分泌肿瘤也应用了该分期系统。鉴于此,新的胸腺肿瘤的分期应着重解决以下几个问题:(1)突破包膜的定义是什么?是否为重要的预后因素?(2)如何明确不同纵隔结构受侵对预后的影响。(3)哪些外科医生对于外侵判断造成的影响尚未被病理所证实。(4)新的TNM分期如何纳入淋巴结?4.胸腺恶性肿瘤新分期的制定1.制定胸腺恶性肿瘤新分期的组织架构AJCC/UICC拟于2016年发布胸腺恶性肿瘤的新分期,由ITMIG/IASLC于2014年完成新分期改进的工作。之前,ITMIG和IASLC已各自进行了这项工作,并于2010年将前期的工作综合到一起,由ITMIG提供临床资料和数据库,应用IASLC在肺癌第7版分期中获得的经验和分期框架,国际上该领域的专家组成的胸腺恶性肿瘤的分期和预后因素委员会(Thymic Malignancies Domain of the Staging and Prognostic Factors Committee,SPFC-TD)负责新分期的提案,并由IASLC通过癌症研究和生物统计组织(Cancer Research AndBiostatistics,CRAB)对这个分期提案进行广泛的验证。2.胸腺恶性肿瘤数据库的建立新分期的建立需要进行全球性的合作,ITMIG分别建立回顾性和前瞻性的两个数据库。回顾性数据库[23]总样本数为10808例,其中ITMIG收集了6079例,日本胸腺研究协会收集了2897例,欧洲胸外科协会胸腺组收集1814例,来源于世界范围内的105个地方。这些数据通过整理后提交给CRAB进行分析。回顾性数据库的收集有一定的限制,要求能够提供这些数据的细节和必要的解释,便于后期整理、分析,尽量使不同中心来源的数据具有可比性。前瞻性数据库是建立在Masaoka-Koga分期基础上的,由于该分期中的部分描述比较含糊,ITMIG对此进行了详细的解释[15],并以此作为前瞻性数据库建立时的标准。ITMIG明确要求不要改变Masaoka-Koga分期中的任何内容,也不要去讨论这个分期系统是否合适,仅仅是为了提供一个标准使各中心收集的数据具有可比性。该数据库的建立,有望能够在胸腺肿瘤的研究中取得突破。3.胸腺恶性肿瘤新分期的特征SPFC-TD认为一个胸腺的新分期应该具备以下几个特征:(1)仅从解剖学上的病变范围来描述,预后因素不应成为描述分期的一部分。解剖学上的病变范围是具体的,可以应用于所有个体,而预后因素是变化的、多因素的,而且部分因素很难去获取,存在着复杂性和不确定性,难以适用于所有个体;(2)适用于所有类型的胸腺恶性肿瘤,包括胸腺瘤、胸腺癌、胸腺类癌等。虽然胸腺肿瘤的生物学行为迥然不同,组织学分期上也存在着一些灰色地带[24],尤其是对于有限的活组织检查标本。不过肺癌的分期系统就适用于小细胞肺癌、非小细胞肺癌和肺类癌,为这项工作提供了先例。(3)基于TNM分期系统。因为对于胸腺恶性肿瘤来说,包含淋巴结评估的TNM分期可能更有意义,最近的一篇文献报道了Ⅲ期胸腺瘤(胸腺癌除外)手术切除的淋巴结中有29%出现了淋巴结转移[25],所以即使对于胸腺瘤,淋巴结的评估同样有意义,不过目前并没有详细的关于胸腺瘤淋巴结评价的研究。4.胸腺恶性肿瘤新分期的指导原则胸腺瘤新分期的指导原则包括:(1)能够被一致的应用,这是制定新分期的基本目的;(2)适用的临床分期。因为医生往往在取得病理标本之前就需要决定治疗策略,所以临床分期较病理分期更有实用价值。ITMIG也建立了一个前瞻性的影像资源库,将来可用于验证临床分期;(3)适用于所有类型的胸腺肿瘤,最好能与现有的分期系统有一定的兼容性。因为目前并没有一个统一的、应用广泛的分期系统,事实上后者并不重要。(4)能够预测预后。预后作为一个工具,已经广泛应用于TNM分期。然而,预后不仅受肿瘤本身特性的影响,还受许多混杂因素的影响,根据预后差异进行亚组分析来区分混杂因素的影响比较困难,尤其对于胸腺肿瘤,因为病人数量的限制,其亚组分析更加困难。另外,与其他恶性肿瘤不同,胸腺恶性肿瘤的复发和死亡的相关性很弱,其预后更难评估,而与胸腺恶性肿瘤无关的其他因素,却影响着总生存。5.胸腺恶性肿瘤新分期制定的进程4.5.1制定时间漫长因为胸腺肿瘤的发病率低,前瞻性数据库的建立将是一个比较漫长的过程,所以评估胸腺恶性肿瘤的预期总生存需要花费较长的时间,即使对于Ⅲ期以上的病例,其中位复发时间也需要3-4年,所以目前正在进行的胸腺恶性肿瘤新分期的工作仅仅只是个开始。在新分期发布之前,还将应用前瞻性数据库对依据回顾性数据库得出的结果进行初步的验证,以确定其有效性。胸腺恶性肿瘤预后模型的建立也需要一个较长的过程,因为以往这方面的数据很少。SPFC-TD将收集包括从回顾性数据库得出的预后信息,研究者内部和观察者之间的差异,以及其他研究组织或个人公开发表的一些建议等数据资源来进行综合评估。ITMIG已着手计划了这项工作,包括建立前瞻性数据库,应用贝叶斯统计方法等,不过该项工作也比较困难,预期在胸腺恶性肿瘤新分期发布的时候该模型尚不能完成。4.5.2一些值得探索的问题4.5.2.1肿瘤的大小是一个值得研究的方面。过去的一些研究发现[14][26],一个或多个肿瘤维度的测量可能会对肿瘤的预后有意义。然而,大的胸腺恶性肿瘤形状并不规则,如何去进行肿瘤大小的测量?如何将临床测量(通常是基于CT影像中横断面的最大径)与病理学的测量结合起来需要进一步的研究。4.5.2.2ITMIG同时开展了按照Masaoka分期进行亚组分析后不同群组间差异的研究。依据肺癌分期时的经验,一些非组织学特征的亚组分析,可能与预后相关。对于胸腺恶性肿瘤,非组织学因素导致死亡的原因(比如并发症)和治疗方案可能是2个最重要的混杂因素[27],为了明确这些因素的影响,研究将重点将关注那些术后和复发的病人,研究之前需区分之前的手术是R0还是R1。4.5.2.3新分期中除了对TNM的的情况进行具体分析,还将考虑更多的可能会对预后产生影响的其他因素。比如对肿瘤侵犯特定纵隔器官或结构(比如胸膜、心包等)对预后的影响。5.总结胸腺恶性肿瘤是一个发病率较低的孤儿病,缺少对该类疾病准确、统一的分期,阻碍了该疾病的进一步研究和进展。目前,ITMIG和IASLC正合作制定一个胸腺恶性肿瘤新分期的工作,邀请了国际上相关领域的专家、机构加入,按照统一的标准建立数据库,并将通过后期对数据的整理、分析,发布一个定义明确、通俗易懂、操作性强的胸腺恶性肿瘤分期系统,促进胸腺恶性肿瘤研究的进展。
胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科3231人已读 - 媒体报道 胡润磊荣获首届胸外科青年医师手术竞技大赛决赛全国三等奖
http://www.hz-hospital.com/admin/search/news/3092/4192.html为搭建一个完善的青年医师成长与自我展示的平台,培养综合素质更强的胸外科接班人,促进胸外科发展,更好的服务于人类健康事业。由中华医学会胸心血管外科分会青年委员会主办的首届胸外科青年医师大于2017年3月拉开帷幕。大赛的主题是:成长、展示、坚守、超越。我院胸外科胡润磊副主任医师经过初赛,南方区复赛的激烈比拼,顺利进入7月15日在呼和浩特举行的全国总决赛,在总决赛中发挥出色,获得了三等奖,为我院争夺了荣誉。
胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科2263人已读 - 媒体报道 胡润磊副主任医师在2017胸外科青年医师竞技大赛喜获佳绩
文章来源:http://www.hz-hospital.com/admin/search/news/3062/4132.html 由中华医学会医学会胸心血管外科分会青年委员会主办的“胸外科青年医师竞技大赛”复赛南方赛区于2017年5月6日在上海举行。大赛的主题是“展青年医师风采,秀卓越外科技艺”。比赛主要由胸外科知识抢答和手术视频比赛两部分组成。我院胸外科胡润磊副主任医师顺利通过初赛后进入了这次复赛,在比赛中发挥出色,获得总分第二名,顺利进入决赛。
胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科1440人已读 - 学术前沿 Ⅰ期和Ⅱ期非小细胞肺癌治疗进展
http://app.medtrib.cn/media/phone/post/app/168/711d59ce-3eb8-4865-a7ba-6fcee21cbfc5.html?from=timeline&code=041NfdD528Uq0N0SjXz52MEsD52NfdDV&state=userinfo
胡润磊 副主任医师 浙江大学医学院附属第一医院 普胸外科972人已读





