贾云鹏医生的科普号
- 精选 伟哥可能增加了恶性黑色素瘤的风险
背景 对于口服勃起功能障碍药物的靶点,5型磷酸二酯酶(PDE5)抑制剂(伟哥),是与恶性黑色素瘤的发展途径密切相关的一部分。最近报道西地那非使用者的恶性黑色素瘤的风险增加。意义 为了检测使用PDE5抑制剂和黑素瘤风险之间的联系,包括特定PDE5抑制剂的数据,处方编号,和黑素瘤的阶段。方法 一项全国范围,以人群为基础,巢式病例对照研究在瑞典处方药注册,瑞典黑色素瘤注册,和其他卫生保健登记,并在瑞典人口数据库进行,包括从2006年到2012年的诊断的4065例黑色素瘤者,和5例与之出生年份相匹配随机挑选的对照病例。暴露点为PDE5抑制剂西地那非和伐地那非或他达拉非填写处方的数量。主要结果为多变量逻辑回归分析中的黑色素瘤风险及基底细胞癌的分期和风险。结果 4065例黑色素瘤病例中,435(11%)例男性处方中充满了PDE5抑制剂,20325例对照中的1713例患者(8%)也是如此。在多变量分析中,服用PDE5抑制剂的男性患黑色素瘤风险增加(OR,1.21[95%Cl,1.08-1.36])。最显著增加的风险在单一处方的男性中观察到(OR,1.32[95%Cl,1.10-1.59];曝光率,病例中的4% vs 对照中的3%),而有多个填充处方的男性中不显著(2-5个处方:OR,1.14[95%CIl,0.95-1.37],病例中的4% vs 对照中的3%;对于≥6个处方:OR,1.17[95%Cl,0.95-1.44],病例中的3% vs 对照中的2%)。PDE5抑制剂与黑色素瘤0阶段(OR,1.49[95%Cl,1.22-1.83],病例中的13% vs 对照中的8%)和I阶段(OR,1.21[95%Cl,1.02-1.43] 病例中的12% vs 对照中的10%)显著相关,但与II阶段至IV阶段过程不相关(OR 0.83[95%Cl,0.63-1.09],病例中的6% vs 对照中的7%)。对于西地那非和伐地那非或他达拉非的风险估计是相似的。PDE5抑制剂的使用也与基底细胞癌的风险增加(OR,1.19[95%Cl,1.14-1.25],病例中的9% vs 对照中的8%)相关。服用PDE5抑制剂的男性有较高的教育程度和年收入,这些因素也显著与黑色素瘤风险相关。
贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)1567人已读 - 精选 晚期前列腺癌的内分泌治疗
前列腺癌(prostate cancer,Pca)的内分泌治疗已有60多年的历史,自1941年加拿大医生Huggins和Hodges首次报道以来, Pca的内分泌治疗即在临床上得到了广泛应用[1]。目前,内分泌治疗仍是晚期Pca的主要治疗手段,其目的在于减少或消除雄激素对前列腺癌细胞的生长促进作用。主要包括去势治疗、抗雄激素药物治疗、最大雄激素阻断、间歇性雄激素阻断及雄激素非依赖性前列腺癌的治疗等。本文就目前这一领域研究的最新观点加以综述。1 去势治疗 去势治疗的目的是使血清睾酮(testosterone,T)浓度降低至去势水平。一般认为T降低到治疗前基线值的5%-10%以下,即可判断达到去势水平。但也有学者认为去势水平应以T低于50ng/dl,甚至以低于20ng/dl为标准[2]。包括手术去势和药物去势两种。1.1 手术去势 采用双侧睾丸切除术仍是目前国内外晚期Pca去势治疗的金标准,术后可去除体内90%-95%的T,并可明显减轻Pca骨转移灶所引起的疼痛。手术操作简单,除出血及感染外,几乎没有并发症,可在局麻下进行,具有高效、安全、简便及廉价特点。Pca患者做双侧睾丸切除术或双侧睾丸精曲小管剥除术后,血清中T、游离睾酮(FT)分别可下降92.27%、92.26%,双氢睾酮(DHT)仅下降58.36%[3],这是因为肾上腺网状带所产生DHT不会随去势手术而消除,因此去势术后必须加用药物才能达到最大限度雄激素阻断或全雄激素阻断。1.2 药物去势 是指在不切除睾丸的前提下使用雌激素类药物、黄体生成素释放激素(lufeihizing hormone releasing hormone,LHRH)类似物阻断雄激素的产生,使T浓度达到去势水平。1.2.1 雌激素药物治疗 雌激素可抑制垂体促黄体生成素(LH)释放,从而使血中T下降而发挥治疗Pca的作用。雌激素中最常用的是己烯雌酚(diaethylstilbestrol,DES),其价格便宜,也有较好的疗效,对于经济条件有限的患者,也是一种很好的选择。DES的剂量减为1mg/d,并加用阿斯匹林(aspirin) 75mg,可减低心血管毒性。DES曾是经典的去势药物,但由于可能导致明显的心血管疾病(包括心肌梗塞、脑血栓和肺梗塞)限制了其在临床上的广泛使用。因LHRH类似物具有与雌激素类似的疗效,且无心血管并发症,故随着LHRH类似物的应用而被逐渐淘汰,目前,已烯雌酚已不作为药物去势的一线选择。1.2.2 LHRH类似物 包括LHRH激动剂(LHRH-a)及LHRH拮抗剂。LHRH-a常用药物为戈舍瑞林(goserelin),商品名:诺雷德(zoladex),3.6mg;亮丙瑞林(leuprolide),商品名:郁那通(enantone),3.75mg;此外还有曲普瑞林(triptorelin),商品名:达菲林(depherelin)3.75mg;均为皮下注射,每4周一次。LHRH-a是目前使用最广泛的去势药物,能与脑垂体促性腺激素产生细胞上的受体结合,并在治疗初期导致短暂的促性腺激素释放及血清T上升,这种一过性T升高可能出现临床症状的加剧,如骨痛、急性尿潴留以及高凝状态导致的心血管疾患,这也是此类药物的主要副作用,因此初次用药的前2周需同时服用抗雄激素治疗。在LHRH-a治疗大约1周后,LHRH受体减少,脑垂体对LHRH的反应逐渐降低,并于3-4周后达到去势效果。国内仅在患者拒绝接受手术去势且经济上又能接受时方才使用。另外约10%患者注射LHRH-a后T无法达到去势水平,这部分患者可能需要用外科去势的方法进行治疗[4]。LHRH拮抗剂作用机理与激动剂相似,但由于其特殊的分子结构,使用后不会导致T一过性升高及临床症状加剧。常用药物为阿巴瑞克(abarelix),商品名:普来纳西(Plenaxis),是由美国Praecis制药公司开发的纯LHRH阻滞剂,2003年获美国FDA批准,次年在美国上市[5]。阿巴瑞克是在患者没有其他可供选择的疗法时,用于治疗晚期前列腺癌的一种药品。该药标明用于:不能采用其他激素疗法的和拒绝手术去势的晚期前列腺癌的症状治疗。此外还有地盖瑞利(degarelix),由Ferring公司开发,2006年2月开始进行III期临床试验,地盖瑞利连续给药一年可以快速持续地抑制T水平,同时还可以持久有效地维持前列腺特异性抗原(prostatic specific antigen,PSA)减少,主要不良反应如疲劳是由T水平降低所引起的,没有发现严重的毒副作用及局部或系统性过敏,目前尚未发现它也具有像其他LHRH阻滞剂一样引起组胺释放的作用[6]。2 抗雄激素药物治疗 抗雄激素药物(即雄激素受体阻滞剂)具有使用方便,不良反应小等优点,并且避免了睾丸切除术后患者的心理异常,因而在临床上被广泛应用[5].能与前列腺癌细胞核内的雄激素受体结合,从而降低T和DHT对癌细胞生长促进作用,根据化学结构不同,分为甾类与非甾类两种。2.1 甾类抗雄激素药 以醋酸环丙孕酮(cyproterone acetate,CPA)为代表,此外还包括醋酸甲地孕酮及醋酸甲羟孕酮,但总体疗效低于CPA,甾类抗雄激素除了有阻断雄激素受体的作用外,还有抑制垂体分泌LH及肾上腺分泌雄激素的作用,由于没有量效相关研究,因此无法确定CPA的最佳治疗剂量,一般推荐每次100mg,tid。由于CPA降低血清T,因此具有性趣降低,勃起功能障碍等副作用,少数患者出现乳房胀痛、心血管毒性及肝脏损害。2.2 非甾类抗雄激素 常用的有氟他胺(fiutamide),比卡鲁胺(bicalutamide)及尼鲁米特(nilutamide)。这类药物作用单一,仅仅是与雄激素受体结合,故又称为纯抗雄激素,最大优点是保持患者的性功能,而且对心血管无副作用亦不引起血栓。2.2.1 氟他胺(商品名:福至尔,以前称缓退瘤) 建议用量为250mg,tid,是现使用最多的抗雄激素药物。由于其需要在肝脏内转化为活性药物形式羟基氟他胺,因此具有脏脏毒性,轻度的肝脏损害如转氨酶等往往在停药后具有自限性(发生率约10%),但也有报道服用氟他胺后致命性肝损害的发生率为3/10 000,高于普通人群10倍,因此服药期间应定期检查肝脏功能[7]。2.2.2 比卡鲁胺,商品名:康士德(casodex) 常用量50mg,qd,是目前应用较多的一种选择性抗雄激素药,与雄激素受体的亲和力比fiutamide强4倍,其结构和成分与fiutamide不同,某些被fiutamide刺激而突变的雄激素受体可被比卡鲁胺所抑制[8],说明两种药物在雄激素受体的作用位点不同。与氟他胺相比,比卡鲁胺对晚期Pca患者生活质量的提高、PSA控制率及症状缓解效果类似,但其肝脏毒性及其它副作用均低于氟他胺,目前认为比卡鲁胺的安全性和耐受性最佳。2.2.3 尼鲁米特 诱导剂量300mg/d,连服4周,维持剂量150mg/d。nilutamide在体内化学结构较少受代谢变化,对受体的作用较持久,如与手术或化学(用LHRH类似物)去势合用,可使外周抗雄激素作用更为完全,即可抑制去势后肾上腺皮质仍然分泌的雄激素的效应,并可抑制使用LHRH类似物作用后最初几天出现的血清T增加、Pca恶化现象。由此,作用表现较彻底。适用于已转移的Pca,可与手术或化学去势合用。3 最大雄激素阻断(maximal androgen blockade,MAB)治疗MAB又称雄激素全阻断或联合雄激素阻断(combined androgen blockade,CAB),其目的在于阻断睾丸和肾上腺分泌的所有T对雄激素的作用。男性90%-95%T由睾丸产生,其余5%-10%由肾上腺产生,手术去势与药物去势效果相当,但都对肾上腺来源的T没有影响, 由此可见,单纯去势对雄激素的阻断是不完全的,而且这种部分雄激素阻断被认为有可能引起雄激素非依赖性肿瘤细胞的迅速生长[9],导致内分泌治疗的失败。因此有人提出睾丸切除或LHRH类似物+抗雄激素药物(如氟他胺)治疗模式,即雄激素全阻断(MAB)治疗[10],可彻底阻断体内T对前列腺癌细胞的生长促进作用,进而提高晚期Pca的治疗效果。MAB目前已逐渐成为晚期Pca患者最常用的内分泌治疗方法。Janknegt研究结果表明,睾丸切除联合缓退瘤效果明显优于单纯睾丸切除者[11]。目前MAB主要应用于晚期及复发性Pca,根治术前新辅助内分泌治疗及配合放疗的辅助内分泌治疗。然而迄今MAB是否较单一的内分泌治疗更为有效还存在争论。欧美前列腺协作临床试验工作组(PCTCG)[12]有一项迄今最具规模的比较雄激素完全阻断治疗与单一去势的荟萃分析,包括了27项临床随机试验的8 275例局部晚期或转移性Pca患者,结果显示,接受MAB治疗的患者5年存活率为25.4%,略高于仅接受单一药物或手术支势者的23.6%,统计学差异无显著性。且长期MAB治疗有三个明显的弊端:治疗费用高、不可避免的出现雄激素非依赖性、生活质量的恶化。4 间歇性雄激素阻断(Intermittent androgen blockade,IAB)治疗 IAB治疗是指Pca患者行内分泌治疗一段时间后血清T下降至去势水平, PSA降至正常水平以下停止治疗,根据肿瘤进一步发展情况(如PSA升高)再重新开始下一个治疗同期的循环治疗方法。目前文献中IAB又称为间断性雄激素去除(Intermittent androgen deprivation,IAD)或间断性雄激素抑制(Intermittent androgen suppression,IAS)。随着MAB治疗的进行,大部分Pca患者最终将发展成不依赖于雄激素而生长的雄激素非依赖性前列腺癌(androgen independent prostate cancer,AIPC)。最近的研究表明,MAB不能延长前列腺癌细胞进展到非雄激素依赖的时间[13],还可使患者生活质量下降,如性欲低下、阳痿、疲乏、抑郁等,而且费用昂贵。因此有人提出了间歇性雄激素阻断,以延长肿瘤细胞向非激素依赖细胞转变的时间[14]。最近的三期临床报道显示,随访51个月时,进行间歇内分泌治疗的局部晚期和转移患者的生存与持续治疗者相似,并且首次治疗后PSA降至2ng/ml以下者有82%的生存时间无需治疗[15]。目前研究显示,IAB是一种切实可行的治疗策略,延长了生存期和耐药出现时间,且患者花费少并获得了较好的生存质量[16]。目前国外的IAB治疗方案是联合应用药物去势和雄激素受体阻断剂间歇性治疗Pca患者。常见的联合方法主要为LHRH类似物enantone或zoladex加非甾类抗雄激素药氟他胺或康士德[17]。IAB每周期治疗的时间及停止治疗的标准各家报道不一,国内推荐停药标准为PSA<0.2ng psa="">4ng/ml时开始新一轮治疗。IAB重新治疗的标准也存在很大差异,一般来说,根据患者临床分期、治疗前血清PSA水平,实现血清PSA水平个体化:(1)治疗前血清PSA水平不高患者,当血清PSA值达到最初水平则恢复治疗;(2)治疗前血清PSA水平高的患者,当血清PSA>20ug/L左右恢复治疗;(3)治疗3个月血清PSA<4ug psa="">10ug/L;无症状患者PSA>20ug/L均恢复治疗[18]。5 雄激素非依赖性前列腺癌(AIPC)的内分泌治疗 AIPC是指在血清T处于去势水平而病变发生进展,出现新的转移灶、原有病灶增大或间隔2周连续检测的PSA水平上升。AIPC是Pca内分泌治疗后的必然结果,也是造成患者癌死亡的原因。对初始内分泌治疗失败后的AIPC患者仍可给予二线内分泌治疗,因其毒副作用较少,故应在全身化疗之前优行采用。治疗方式包括抗雄激素药物撤退、加用或换用抗雄激素药物、使用肾上腺来源雄激素的抑制药及皮质类固醇药物的应用等。5.1 抗雄激素药物撤停 Kelly和Scher[19]发现采用flutamide治疗后反应良好的患者,长期应用后症状复发并有加重,血PSA水平升高,撤退后症状迅速好转且血PSA下降,称之为抗雄激素撤退综合症(antiandrogen withdraw syndrome)。任何抗雄激素药物都存在所谓的“撤退”效应,因此停止使用后部分患者可有一定效果。5.2 加用或换用雄激素药物 因各类雄激素药物对雄激素受体的作用不同,对初始抗雄激素或雄激素完全阻断治疗失败的患者仍可使用其它替代的抗雄激素药物治疗。Small[20]等认为,对fiutamide发生抵抗的患者,换用bicalutamide仍有效。故可将二者交替使用以延缓耐药发生,每次用药最好不超过2个月[21]。5.3 肾上腺素雄激素抑制剂 对已更换雄激素药物并行撤退治疗仍无效的患者可使用肾上腺雄激素抑制剂(如酮康唑等)。酮康唑不但可抑制肾上腺合成雄激素,且对前列腺癌细胞具有直接的细胞毒性作用。酮康唑在国外被认为是标准的二线内分泌治疗药物,不同的研究者分别采用酮康唑1200mg/d,800mg/d,600mg/d 治疗AIPC[22-24],疗效相似而低剂量时毒副反应较轻。Small等[25]报道了50例雄激素完全阻断治疗失败后经抗雄激素药物撤停仍出现肿瘤进展的患者应用酮康唑(400mg,tid)和氢化可的松治疗的疗效。5.4 皮质类固醇类药物 上述这些治疗仍无效后可使用糖皮质激素治疗,糖皮质激素(如强的松、地塞米松和氢化可的松)能减低垂体产生的促肾上腺皮质激素(corticotrophin,ACTH),从而抑制肾上腺激素(包括肾上腺雄激素)的生成,还可通过干扰细胞内信号传导路径,直接抑制肿瘤细胞生长。Sartor等[26]报道了29例AIPC 患者接受强的松(10mg,bid)治疗的疗效。6 总结 Pca是一种雄激素依赖性肿瘤,对晚期Pca患者一般首先采用手术去势或LHRH类似物的药物去势。由于手术去势操作简单,安全有效,是目前内分泌治疗的首选方法,其效果肯定,已在临床上得到广泛使用。药物去势的治疗可采用zoladex,3.6mg或enantone,3.75mg等类似药物每四周一次皮下注射。对单一去势治疗无效的患者可采用最大雄激素阻断治疗。也可根据患者身体状况,采用单一抗雄激素药物治疗。IAB治疗提出了Pca内分泌治疗的新策略,以最小的药物蓄积毒性提高患者生活质量,表现为治疗间歇期性功能恢复和全身情况改善,延长雄激素依赖状态,减少治疗费用。雄激素阻断治疗一般在2年左右减退并逐渐失效,此时即进入AIPC治疗阶段,可继续给予二线内分泌治疗。对于AIPC患者,维持雄激素在去势水平是必要的,即使患者已进入激素抵抗性前列腺癌(hormonal refractory prostate cancer,HRPC)期,也仍需要维持内分泌治疗。
贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)3984人已读 - 精选 男性下尿路症状与前列腺炎贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)1391人已读
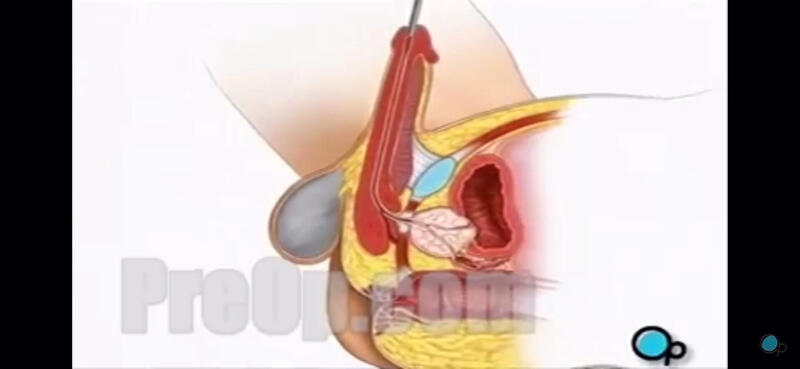
- 视频 经尿道前列腺电切术是如何完成的
 贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)8人已观看
贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)8人已观看 - 医学科普 无菌性前列腺炎是病吗?
一、什么是无菌性前列腺炎 大多数前列腺炎病人属于无菌性前列腺炎,发病率明显比细菌性前列腺炎高。前列腺炎的致病原因目前尚无一致性意见,主要包括夫妻长期分居、盆腔充血、性交中断、过度手淫、长途骑自行车或久坐工作均为发病因素。文献报道滴虫、沙眼衣原体、解脲支原体、隐球菌等被认为与此病有关。 无菌性前列腺炎的病理过程多为慢性,炎症反应比急性细菌性前列腺炎局限且不明显,突出表现是腺泡内及其周围有不同程度的浆细胞和巨噬细胞浸润及区域性淋巴细胞集聚,腺叶中纤维组织增生明显。肛门指诊时可触及前列腺腺体呈柔韧感,如前列腺纤维变性,腺体可萎缩,且可延至后尿道,使膀胱颈硬化。 二、有何症状?应该怎么诊断? 无菌性前列腺炎的临床症状主要包括以下几个方面: (1)排尿刺激症状,如尿频、尿急、尿痛、排尿烧灼感。 (2)排尿梗阻症状:如排尿困难、排尿细、排尿踌躇、尿不尽、尿末滴沥等。 图片 (3)与排尿无关的疼痛症状,主要表现为定位不明确的胀痛,隐痛,疼痛分布位置可以很广泛,可为会阴部,耻骨上,肛门周围,阴囊,大腿根部内侧,阴茎等。 (4)精神症状,表现为头昏,记忆力减退,焦虑,失眠,多疑,抑郁等,对身体的不适和疼痛过度敏感。 无菌性前列腺炎的诊断和细菌性前列腺炎相类似,但不同的是没有反复的尿道感染病史,常可有前列腺液自尿道口溢出。直肠指诊发现前列腺较饱满,质感稍软,可有轻度压痛。体检与临床症状不一定相符合,前列腺液细菌涂片和培养均为阴性。 三、如何治疗 无菌性前列腺炎的治疗主要是通过生活方式治疗。包括:(1)适当进行体育锻炼,增强体质,促进血液循环,提高抗病能力。(2)生活有规律,避免劳累熬夜,受寒受凉。(3)禁烟酒,勿食用辛辣刺激性强的食物。(4)防止便秘,保持大便通畅。(5)有条件者定期行前列腺按摩,有利于前列腺液的引流,更新前列腺内环境。(6)规律的性行为,避免过度手淫,减少盆腔充血机会。无菌性前列腺患者对下腹部症状非常敏感,心情抑郁。对精神症状严重者可请精神心理科医生配合治疗,必要时可用镇静药物、抗抑郁药物等。 图片 慢性无细菌性前列腺炎的治疗药物很多,但到目前为止还没有非常特效的药物,且不同的药物对症状改善的侧重点不一样,建议联合应用。前列腺液培养无细菌的情况下,可以尝试进行衣原体或支原体检测,明确后可以使用红霉素,诺氟沙星等药物治疗。如果以排尿困难,尿路梗阻症状为主,则可选用哈乐,可多华等药物治疗。一些植物药,如舍尼通,可抑制前列腺的炎症反应,减轻症状。对以疼痛为主的病人可以使用解热镇痛药,如布洛芬,西乐葆等。 慢性无菌性前列腺炎主要的治疗是改善症状,可使用一些物理疗法,主要是热能疗法,增强前列腺及周围组织的血液循环,促进炎症吸收。常用的方法有热水坐浴、射频和微波、经尿道针刺消融,经直肠热疗等。大多数病人可以通过以上治疗得到明显改善。对于老年人前列腺炎患者,如果合并前列腺增生,或前列腺癌,可以考虑经尿道前列腺等离子电切术或前列腺根治术。对于年轻患者不建议手术切除前列腺,小前列腺的切除可能导致膀胱颈部挛缩等并发症,导致排尿梗阻症状加重,并且需要更进一步的复杂手术干预。
贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)1256人已读 - 学术前沿 NCCN/EAU指南:新型内分泌治疗药物恩扎卢胺相关更新要点和研究进展
近年来,多项临床研究成果极大推进了新型内分泌治疗药物在晚期前列腺癌治疗中的应用。目前多种新型内分泌治疗药物已获批用于晚期前列腺癌的治疗,包括阿比特龙、恩扎卢胺、阿帕他胺、达洛鲁胺。多项重磅临床研究改变了临床实践,前列腺癌领域重要的国际指南NCCN和EAU指南已更新,一起来回顾下,指南中与新型内分泌治疗药物恩扎卢胺相关的更新要点和研究进展吧! 恩扎卢胺用于转移性激素敏感性前列腺癌(mHSPC)一线治疗 ENZAMET是一项开放标签、随机、III期临床研究,旨在评估恩扎卢胺+雄激素剥夺治疗(ADT)对比单独ADT用于mHSPC的疗效和安全性,研究结果于2019年发表在《NEJM》杂志,研究纳入1125例患者,主要终点为总生存期(OS),第一次中期分析时,中位随访时间为34个月,研究即达到主要研究终点(HR=0.67,P=0.002)。另外,结果还显示,恩扎卢胺也能为列腺特异性抗原无进展生存期(PSA-PFS)和无进展生存期(PFS)带来明显获益,且获益优势更大[1]。 OS、PSA-PFS、PFS分析 ARCHES是一项随机、双盲、III期研究,旨在探索ADT+恩扎卢胺对比ADT+安慰剂用于mHSPC的疗效和安全性。主要研究终点为放射学无进展生存期(rPFS),2019年发表于《JCO》杂志的结果显示,中位随访14.4个月时,恩扎卢胺使患者的中位rPFS明显改善,两组分别为19个月和未达到(HR=0.39,P<0.001),且亚组分析显示了与总人群一致的生存获益。基于此,2019年12月,恩扎卢胺获FDA批准用于mHSPC患者的治疗[2]。 基于这两项研究,NCCN指南V1和V2版推荐恩扎卢胺用于转移性未经去势前列腺癌(或mHSPC)的一线治疗。 未经去势前列腺癌(或)的系统治疗(NCCN指南V2版) 基于ENZAMET和TITAN研究,新版EAU新增推荐要点: 对首次出现M1疾病且适合以下方案的患者,应给予ADT+阿比特龙+强的松或阿帕他胺或恩扎卢胺作为一线治疗(强烈推荐)。 转移性疾病的一线治疗(2020 EAU前列腺癌指南6.4.9) 恩扎卢胺用于非转移性去势抵抗性前列腺癌(nmCRPC)的治疗 PROSPER研究是一项随机、双盲、安慰剂对照的III期研究,旨在评估恩扎卢胺对比安慰剂用于nmCRPC患者的疗效和安全性,研究纳入1401例nmCRPC患者,分层因素包括PSADT(<6个月vs.≥6个月[≤10个月])和基线骨靶向药物的使用等,既往结果显示,与ADT相比,恩扎卢胺+ADT治疗可明显降低转移或死亡风险(HR=0.29,P<0.001)。 今年ASCO大会上,PROSPER研究公布了第三次中期分析结果(最终分析结果),研究结果同步发表在《NEJM》杂志,结果显示,恩扎卢胺和安慰剂组的中位OS分别为67个月和56.3个月,恩扎卢胺+ADT可降低患者27%死亡风险(0.73,P=0.001)。另外,恩扎卢胺与延迟使用后续抗肿瘤治疗相关(HR=0.29),两组的至中位首次使用新治疗时间为66.7个月和19.1个月[3]。2018年7月,FDA扩大了恩扎卢胺的适应证范围,批准其可用于nmCRPC患者的治疗。 基于此,NCCN指南专家组指出:对于nmCRPC(或M0 CRPC)患者,若PSADT≤10个月,可给予恩扎卢胺治疗(1类推荐)。 M0 CRPC患者的系统治疗(2020 NCCN前列腺癌指南V2) 此外,2020 EAU指南也更新推荐:对于nmCRPC且有高转移风险的患者(PSA-DT<10个月),应给予阿帕他胺、darolutamide或恩扎卢胺治疗以延长转移发生时间(强烈推荐)。 非转移性去势抵抗性疾病(2020 EAU前列腺癌指南) 对于去势抵抗性前列腺癌(CRPC)的治疗,还有两个更新点: 一线治疗的选择应基于患者的表现状况、症状、合并症、疾病位置和程度、患者偏好,以及既往HSPC的治疗情况,给予可延长生存的药物:阿比特龙、卡巴他赛、多西他赛、恩扎卢胺、镭-233、sipuleucel-T(强烈推荐)。 对于CRPC的支持性照护,当给予患者地诺单抗或双磷酸盐时,应监测血清钙、并补充钙和维生素D(强烈推荐)。 恩扎卢胺用于转移性去势抵抗性前列腺癌(mCRPC)的一线治疗和二线治疗 早在2012年8月,基于AFFIRM研究,恩扎卢胺首获FDA批准用于多西他赛治疗后mCRPC的治疗。AFFIRM研究是恩扎卢胺的首个III期临床研究,旨在评估恩扎卢胺对比安慰剂用于化疗后mCRPC患者的疗效和安全性,研究纳入1199例患者,主要终点为OS,2012年发表在《NEJM》杂志上的结果显示,恩扎卢胺使患者的OS从13.6个月提高至18.4个月(HR=0.63,P<0.001),至PSA进展时间和rPFS也得到显著改善[4]。 另一项III期随机对照PREVAIL研究,探索了多西他赛化疗前恩扎卢胺用于转移性前列腺癌患者的疗效和安全性,研究纳入1717例未经化疗的转移性前列腺癌患者,中期分析时,恩扎卢胺组即显示出明显的生存优势,恩扎卢胺组对比安慰剂显著改善了患者的中位PFS,分别为20.0个月和5.4个月,中位OS分别为35.3个月和31.3个月,因而提前终止了研究[5]。 近日,《European Urology》上公布了PREVAIL研究5年随访结果,结果显示,恩扎卢胺降低患者17%死亡风险(HR=0.83,P<0.001),两组的中位OS分别为36个月和31个月,两组的2年、3年、5年生存率分别为71% vs 62%、49% vs 44%、26% vs 21%[6]。 基于此,NCCN指南指出:对于多西他赛治疗前和治疗后的转移性CRPC患者,恩扎卢胺均是可选治疗方案。对于初治转移性CRPC患者,恩扎卢胺为一线治疗优选推荐方案(1类推荐),对于一线治疗为多西他赛的转移性CRPC患者,恩扎卢胺为二线治疗治疗优选推荐方案(1类推荐)。2014年,FDA批准恩扎卢胺的适应证扩展至初治mCRPC患者。 2020 V1版指南将“M1 CRPC系统治疗:无内脏转移腺癌”和“M1 CRPC系统治疗:有内脏转移腺癌”合并为M1 CRPC的系统治疗:腺癌。 参考文献: [1] Davis ID, Martin AJ, Stockler MR, et al. Enzalutamide with Standard First-Line Therapy in Metastatic Prostate Cancer. N Engl J Med. 2019;381(2):121-131. doi:10.1056/NEJMoa1903835 [2] Armstrong AJ, Szmulewitz RZ, Petrylak DP, et al. ARCHES: A Randomized, Phase III Study of Androgen Deprivation Therapy With Enzalutamide or Placebo in Men With Metastatic Hormone-Sensitive Prostate Cancer. J Clin Oncol. 2019;37(32):2974-2986. doi:10.1200/JCO.19.00799
贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)2410人已读 - 学术前沿 成人尿道狭窄治疗现状
对于前尿道狭窄,现有的指南和共识认为应尽早进行开放式尿道重建手术,腔内治疗方法如直视下尿道内切开术、尿道扩张,仅适用于短段、单处、球部尿道狭窄。这是因为尿道端端吻合术和尿道成形术的成功率可分别达到91%和88%,而且对于长段、复杂尿道狭窄,尿道内切开术和尿道扩张的成功率很低。那么泌尿外科医师在临床实践中对指南和共识所推荐的治疗流程的依从性如何?具体是如何实施的? 对此,发表于《Urologia Internationalis》杂志题为《Management of Anterior Urethral Strictures in Adults: A Survey of Contemporary Practice in Germany.》的文章以德国泌尿外科医师作为调查对象进行了相关研究,相信对国内同道有一定的参考价值。 【Abstract】 Introduction: Treatment methods of anterior urethral strictures in adults have undergone considerable changes in the recent past. Our goal was to determine national practice patterns among German urologists and to compare results with the results of prior international surveys. 介绍:近年来,成人前尿道狭窄的治疗方法有了很大变化。我们旨在确定德国泌尿外科医师对前尿道狭窄的治疗模式,并与之前的国际调查结果对比。 Methods: We conducted a survey on the management of urethral strictures among German urologists. 方法:我们在德国泌尿外科医师中进行了一项关于尿道狭窄治疗方法的调查。 Results: Eight hundred forty-five urologists, representing about 14.6% of German urologists, answered the survey. Most common procedures were direct vision internal urethrotomy (DVIU; 87.2%), blind internal urethrotomy (57.5%), dilatation (56.3%), ventral buccal mucosa graft urethroplasty (31.6%) and excision and primary anastomosis (28.9%). In case of a 3.5-cm bulbar stricture and in the case of a 1-cm bulbar stricture after 2 failed DVIUs, a consecutive urethroplasty was significantly more often favoured compared to transurethral treatment options (44.9 vs. 21.3% and 59.4 vs. 8.3%, both p < 0.001). 结果:共有845名泌尿外科医师参与了该调查,约占德国泌尿外科医师总数的14.6%。常见的手术方式包括直视下尿道内切开术(DVIU;87.2%)、非可视尿道内切开术(57.5%)、尿道扩张(56.3%)、颊粘膜尿道成形术(31.6%)以及切除狭窄并一期吻合术(28.9%)。在治疗3.5cm球部狭窄以及2次DVIU治疗失败的1cm球部狭窄时,更青睐于尿道成形术,而不是经尿道手术(44.9 vs. 21.3%和59.4 vs. 8.3%,二者p<0.001)。 Conclusion: Open urethral reconstruction reveals to be a more common method in practice nowadays. Adherence to recommended treatment algorithms improved in comparison to prior surveys. 结论:如今,开放式尿道重建术已成为一种更为普遍的治疗方法。与之前的调查结果相比,对推荐的治疗流程的依从性已得到了改善。 译者述评 原作者研究表明,在德国尿道扩张及尿道内切开术在前尿道狭窄治疗中占有主要作用。这是由于多数医生每年尿道狭窄的手术量少于10台,使得尿道狭窄对于多数受访者来说是一个罕见问题。其次,如此少的手术量无法保证医生获得或者保持良好的尿道重建手术技术。Mundy指出,每年至少需要15台尿道成形手术量才能保证良好的手术质量。Fossiati等研究表明,即使做了大量的尿道成形手术,学习曲线也不会达到平稳状态。 与既往研究结果类似的是,每年完成20台以上尿道狭窄手术的医生仍占少数,并且每年完成5台以上尿道成形手术的医生人数开始减少,约有10%的受访者表示每年完成6台或更多的尿道成形手术,只有5.5%的受访者表示每年有10台以上的尿道成形手术量。大约四分之三的受访者表示会先采用一种微创治疗方法,如果治疗失败则应进行尿道成形术,并且认为2cm或以下的尿道狭窄可采用直视下尿道内切开术。对于一些简单病例如短段球部狭窄,直视下尿道内切开术的成功率可达77%。Barbagli等研究表明,单次尿道切开术的失败不会影响尿道成形术的远期效果。因此上述治疗流程似乎是合理的,可能也更符合成本效益。但仍有24.3%的受访者表示应尽可能长时间的采用微创方法。不过现有的指南和文献均不支持这种说法。多个研究表明,反复的尿道切开术或尿道扩张的成功率很低,并且微创治疗的花费并不划算。与既往研究结果不同的是,越来越多的医生会考虑采用开放式尿道重建手术,约有三分之一的受访者表示会进行尿道成形手术如尿道端端吻合术、颊粘膜尿道成形术。 原作者还指出该调查存在的一些局限性,首先是问卷的回复率相对较低,其次存在选择偏倚,调查人数未达到一定比例可能会使调查结果不准确,未回答者可能并不在意尿道狭窄的治疗方式,这就导致可能高估了医生在选择治疗方法时对指南的依从性,而低估了腔内治疗的数量。 尽管如此,我们也不难看出德国泌尿外科医师越来越熟悉指南和共识推荐的尿道狭窄治疗流程,并且依从性越来越高。这似乎给了我们这样一个启示:与花费大量的时间和精力去掌握具体的手术技术相比,建立良好的治疗流程、培养正确的治疗思路可能更简单,但对治疗效果的影响却至关重要。 参考文献: Rosenbaum CM, Reiss CP, Borgmann H, et al. Management of Anterior Urethral Strictures in Adults: A Survey of Contemporary Practice in Germany. Urol Int. 2017;99(1):43-50
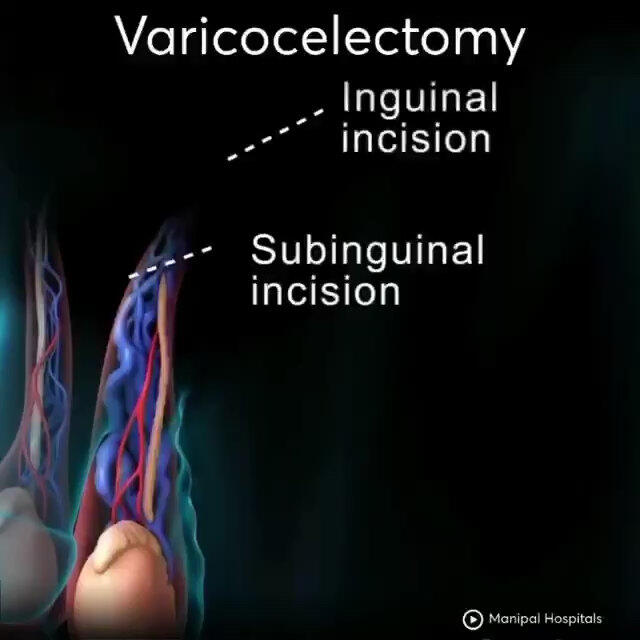
贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)1640人已读 - 视频 显微镜下精索静脉结扎术
 贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)1145人已观看
贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)1145人已观看 - 视频 肾结石的形成原理及治疗方法
 贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)1075人已观看
贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)1075人已观看 - 学术前沿 新冠病毒引起泌尿系统损害
新型冠状病毒感染性肺炎已对公共卫生构成严重威胁。 已有研究表明,部分患者除呼吸系统损伤外,还存在肾功能异常甚至肾损伤,其相关机制尚不清楚。 为了确定新冠病毒感染者是否有肾功能异常或肾损伤,研究组回顾了最近3项针对这类患者临床特征的研究。 研究结果表明,约3%至10%感染新冠病毒的患者肾功能出现异常,包括肌酐或尿素氮升高。此外,7%的患者出现急性肾功能损伤。 鉴于感染者众多,有必要探讨肾功能异常的机制。 已有研究证实血管紧张素转换酶2(ACE2)是介导新冠病毒进入人体细胞的主要受体之一,因此研究组通过在线数据集来了解ACE2在泌尿系统中的表达水平。 结果不出所料,ACE2mRNA在肾细胞中的表达水平相对较高。 免疫组织化学(IHC)结果也表明,ACE2蛋白在肾脏,尤其是肾小管细胞中的表达水平明显较高,但mRNA的表达水平并不高;在免疫细胞和肾小球壁上皮细胞中没有观察到ACE2的表达。 肾小管细胞具有重吸收和排泄功能,在代谢产物的排泄、体液平衡和酸碱平衡的维持中起着关键作用。 新冠病毒可通过与ACE2结合而进入肾小管细胞,从而引起细胞毒性和肾功能异常。 应当对新冠病毒感染者进行肾功能检查和随访,及时发现肾功能损害,及早干预。 出乎意料的是,研究组还发现ACE2在睾丸细胞中表达很高。 睾丸中ACE2蛋白和mRNA的表达几乎是体内最高的。此外,生精管和间质细胞中的细胞均显示出高水平的ACE2表达。 这些结果表明,睾丸细胞是新冠病毒的潜在靶点。 众所周知,HIV、HBV、腮腺炎等病毒可以进入睾丸细胞,引起病毒性睾丸炎。 此外,在某些情况下,病毒引起的睾丸组织损伤可能导致男性不育和睾丸癌。 SARS-CoV就像新冠病毒的“表亲”,也通过ACE2受体进入人体细胞。 先前的研究表明,睾丸炎是SARS的并发症,感染后生精功能可能受到影响。 临床资料表明,新冠病毒感染的肺炎患者中有一定比例是年轻人和儿童,病毒引发的潜在睾丸损伤可能会成为晚期并发症。 然而,目前新冠病毒感染是否影响生殖器官的临床信息很有限。 可针对曾感染SARS并已治愈的男性患者,尤其是年轻男性患者,进行生殖功能随访和评价。 总之,鉴于病毒引起的肾损害和具有一定肾毒性的抗病毒药物,临床工作中应对新冠病毒感染者进行肾功能评价和特殊护理。 另外,由于该病毒对睾丸组织具有潜在的致病性,临床医生在住院治疗和后期临床随访中应注意患者睾丸损伤的风险,特别是对年轻男性患者生育能力的评估和适当干预。 作者: Caibin Fan, Kai Li, Yanhong Ding, Wei LuLu,Jianqing Wang 论文链接: https://www.medrxiv.org/content/10.1101/2020.02.12.20022418v1
贾云鹏 副主任医师 甘肃省中医院 外二科(泌尿外科)4761人已读





