杨祎医生的科普号
- 精选 关于“马凡氏综合症”你所需要知道的一切
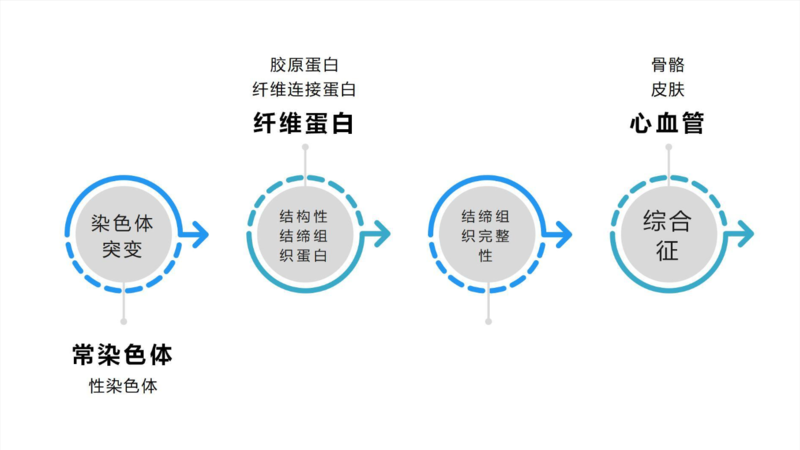
马凡氏综合症是一种由基因突变引起的,影响心血管系统、骨骼系统、眼视光系统等全身多个器官的疾病。马凡氏综合征患者的FBN-1基因突变导致结缔组织发育障碍,由于结缔组织遍布全身,比如心脏、血管、骨骼、关节和眼睛,因此马凡氏综合症也会影响身体的许多不同部位。个体差异不同,症状出现的时间也不同,多数患者青春期后表现明显。但基因表达量不一样,可能出现以下一种或多种症状。但马凡氏综合征并不影响智力。纤维蛋白就像人体大厦的钢筋混凝土,基因突变导致人体组织的延展度大,但是强度却降低了。马凡患者最显著的特点就是身材瘦高,手脚细长。马凡患者往往从小身材就比同龄孩子要高很多,中学甚至小学身高就能达到170cm甚至180cm以上。马凡综合征是由于基因突变引起的,也就是所谓先天的,目前没有证据显示与后天因素有关大约每5000人中就有1人患有马凡氏综合症大约四分之三的患者是通过父亲或母亲遗传但也有患者是自发突变由于马凡氏综合征是常染色体显性遗传,所以患有马凡氏综合症的人,通过自然生育,每个孩子都有50%的几率被遗传马凡综合症举例来讲:张小瘦(马凡)和王小美结婚,他们俩的第一个孩子有50%的可能是马凡,如果要二胎的话,不管第一个孩子是不是马凡,第二个孩子仍然有有50%的可能是马凡,往下推理,每个孩子都是如此。要想诊断马凡氏综合征需要非常有经验的医生做详细的体格检查,眼底检查,和超声心动检查,甚至是基因检测才能确诊。所以最好到门诊当面请医生帮忙诊断。但是马凡综合征也有些非常典型、非常特异的表现,需要引起你的注意,如果有以下情况建议到找医生咨询1家族史:如果父母或祖父母有确诊马凡综合征,或年轻时因动脉瘤或动脉夹层破裂,甚至不明原因猝死的2晶状体脱位:如果做过眼底检查,医生提示有晶状体脱位的3超声心动:儿童或者青少年,不明原因主动脉窦扩张的好,跟着我往下做,拿出纸和笔,记录每一项是否得分?≥7分非常可疑3-5分建议找专科医生咨询2分以下还不足以说明什么实际上并不是每个病人都会表现的很典型,尤其是未到青春期的青少年儿童。另外有些其他疾病的表现和马凡综合征十分相似,Loeys-Dietz综合征,Ehlers-Danlos综合征(血管型),Beals综合征因此如果你对自己有怀疑,最好还是咨询专业的医生马凡的诊断并不依赖基因检测。对于典型的患者,有经验的医生往往通过体格检查和常规检查就可以诊断,但是对于下面三种情况,基因检测就很重要1首次确诊,应该做超声心动图检查,确定主动脉根部、升主动脉的直径、是否有瓣膜返流。6个月后再次复查超声心动,进行对比2至少每年复查一次超声心动图检查,如果病情有变化,应该提高检查频率3如果主动脉直径已经超过45mm,或者瓣膜返流已经中度以上,建议立刻咨询医生,制定你的治疗方案4如果已经做过手术,要根据医生的要求,至少每年复查超声心动和主动脉CTA1应该避免劳累,保持心情舒畅2健康饮食,无需特殊忌口3最好准备一个血压计和运动手表,定期监测心率和血压马凡综合征的主动脉较脆弱,不适合剧烈运动和身体对抗性强的运动对于经过检查或治疗,确定当前身体相对健康的人,指南推荐轻中度的有氧运动散步慢跑慢速游泳骑自行车瑜伽普拉提高尔夫钓鱼跳舞羽毛球保龄球根据每个人的具体请咨询专业医生目前指南推荐的药物有贝塔受体阻滞剂,可以延缓主动脉扩张的速度,常见的有比索洛尔、美托洛尔、阿替洛尔等。此类药物为处方药,应在医生监督下应用。注意:未成年人、心率慢、血压低、有传导阻滞及哮喘患者慎用。血管紧张素转换酶抑制剂(ACEI)类药物如氯沙坦钾有用吗?虽然此类药物对马凡患者的作用尚有争议,但2022年的指南已推荐使用此类药物预防主动脉时间的发生。喹诺酮类的药物不能吃,有研究表明,喹诺酮类药物可能会增加主动疾病的风险,美国食品药品管理局建议有主动脉疾病风险的患者谨慎应用比类药物。如诺氟沙星、氧氟沙星、左氧氟沙星、莫西沙星、环丙沙星,沙星类抗菌药物基本都属于喹诺酮类抗菌药。马凡患者通过辅助生殖技术是可以要孩子的,推荐到正规医院应用3代试管婴儿技术,有很大可能获得一个非马凡的孩子女性患者怀孕和生产都会增加母亲主动脉夹层、破裂的风险,所以一旦有怀孕计划,应尽早进行全面检查,在妇产科及心外科专家咨询后,再考虑怀孕,整个孕期都应该严密监测每周一下午我会在安贞医院门诊8楼,心外科22诊室出诊,可以通过微信公众号“安贞医院-心外科-主动脉外科2区-马凡专病专诊预约
 杨祎 主治医师 北京安贞医院 主动脉外科中心7143人已读
杨祎 主治医师 北京安贞医院 主动脉外科中心7143人已读 - 精选 瓣膜置换患者如何调整华法林剂量?杨祎 主治医师 北京安贞医院 主动脉外科中心1409人已读
- 精选 马凡氏综合征的诊断杨祎 主治医师 北京安贞医院 主动脉外科中心2983人已读
- 精选 全面了解腹主动脉瘤杨祎 主治医师 北京安贞医院 主动脉外科中心2364人已读
- 精选 剧烈胸背痛当心主动脉夹层!
主动脉是心脏通往各个器官的“主干线” 我们都知道石油工厂通过管道源源不断的把动力输送给各个加工厂,在人体内如果把心脏比作石油工厂的话,那么主动脉就是向全身各个器官输送养料的“石油管道”,这条管道一旦破裂会怎样呢?会瞬间导致大出血,并且所有的器官都会因此失去血供,后果不堪想象!主动脉夹层就是由于主动脉壁内膜与中层分离而引起的“灾难性疾病”,其凶险程度可想而知。 主动脉的形状像一个倒置的伞柄 主动脉从心脏上端出发,转弯向下为全身供血,伞柄的直段把手部分被称为“升主动脉”,弯曲把手部分被称为“主动脉弓”,笔直的伞骨部分就是继续负责全身供血的“降主动脉”。主动脉夹层发生于整个动脉全段时就叫A型主动脉夹层,仅发生在降主动脉时叫B型主动脉夹层。“主动脉夹层”在医学上被称为凶、险、急的恶性生命杀手其中的急性A型主动脉夹层是一种非常凶险的外科急症,在我国好发年龄为45至60岁,男女发病比例为3﹕1,发病凶险,无预兆性,大约2/3的患者在发生夹层的前2周内死于夹层破裂,根据国外文献报道,未经手术治疗的主动脉夹层,约50%的患者在发病后48小时内死亡(最初48小时内,死亡率以每小时1%的速度递增),也就是发病最初48~72小时内死亡率为约50%,1周内死亡率高达70%,1个月内死亡率达到90%以上。主动脉夹层的典型症状为突发、持续、剧烈的撕裂样疼痛疼痛通常不断加重,可以发生在背部、腰部、或者腹部,病人往往不能忍受,易与其他疾病混淆。主动脉夹层是指主动脉内膜破裂,主动脉壁内膜与中层分离主动脉的结构从内到外分为三层,即内膜、中层、外膜,当血管腔内压力升高到一定程度,血管内膜的薄弱处会突然撕裂,大量血液冲进内膜与中层之间,将主动脉壁内膜与中层分离,并在内膜与中层之间形成相对于原来血管腔(真腔)的“假腔”,这种情况就称为主动脉夹层。正常成人的主动脉壁耐受压力颇强,使壁内裂开需66.7kPa(500mmHg)以上的压力,而正常人血压一般在100-130mmHg,因此,造成夹层裂开的先决条件为动脉壁缺陷,尤其中层的缺陷,各种原因导致主动脉壁退变或中层弹力纤维和平滑肌病变是主动脉夹层形成的内因,而主动脉腔内血液动力学变化(如高血压)是形成的外因。内膜撕裂口多数发生在主动脉腔内血流压力最大或变化最大的管壁处,即升主动脉外右侧壁或降主动脉近端,主动脉腔内血液经内膜撕裂口将中层分离形成夹层,夹层沿主动脉壁纵向和环形扩展,扩展范围可局限和广泛,广泛者可自升主动脉直至腹主动脉。假腔持续扩张和真腔受压变窄或塌陷是主动脉夹层最重要的和基本的病理生理改变。主动脉真腔受压变窄或塌陷,并累及主动脉各分支血管,导致脏器缺血或坏死改变,特别是冠状动脉﹑脊髓动脉和腹腔脏器血管及双髂动脉。“假腔”如果其他部位没有破口,因而血液淤积在“假腔”中,并且血管腔内相对压力高的血液不断涌入“假腔”,进而内造成血管增粗,膨大,随时可能破裂,破裂后快速出血,心包填塞而致临床死亡,抢救成功率微乎其微,是一种死亡率极高的急性大血管疾病。
杨祎 主治医师 北京安贞医院 主动脉外科中心1888人已读 - 医学科普 老年人沉默的杀手,一个视频带您了解主动脉瘤
 杨祎 主治医师 北京安贞医院 主动脉外科中心5人已观看
杨祎 主治医师 北京安贞医院 主动脉外科中心5人已观看 - 诊后必读 做了手术后能不能做核磁检查?
《磁共振成像安全管理 中国专家共识(2017)》 对11类植入物的核磁检查建议 --中华放射学杂志 2017.10 如果体内有颅内动脉瘤夹、牙科植入物、输液泵和留置导管,能否进行核磁检查呢?关于磁共振成像安全,2017年发布了一份中国专家共识 1.颅内动脉瘤夹 动脉瘤夹由不同磁敏感性的多种物质构成,形状各异,其中的铁磁物质含量达多少会导致MRI检查时发生危险,目前尚无定论。强铁磁性材料的动脉瘤夹禁止用于MRI检查;非铁磁性或弱铁磁性材料的动脉瘤夹可用于1.5 T(含)以下的MRI检查。 如果不清楚受检者颅内是否有动脉瘤夹,应先进行X线平片检查,或查看近期(术后)的颅脑X线平片、CT图像来判断是否存在动脉瘤夹。 对于有动脉瘤夹但属性不明的患者,应对其风险-获益比进行谨慎评估,告知受检者所有潜在风险,并由患者和(或)监护人签署知情同意书。 2.心脏植入式电子设备 心脏植入式电子设备包括心脏起搏器、ICD、植入式心血管监测仪(CM)和植入式循环记录仪(ILR)等,种类越来越多,也越来越复杂。目前临床上应用的绝大多数心脏植入式电子设备都不能与MRI兼容。 放射科和心血管病专家必须熟悉每个设备的使用条件和限制,意识到每个MRI设备都有其独特性,不存在“通用”的安全性判别标准。不遵循产品说明随意使用设备可能会造成严重不良后果。 3.人工耳蜗 人工耳蜗是一种电子装置。MRI扫描可能会使人工耳蜗磁极发生翻转,需要通过有创手术方法进行复位,建议充分评估MRI检查的风险-获益比后再行扫描。头部扫描时,磁极片翻转的概率低于胸腹部和下肢扫描,可能与胸腹部、下肢扫描时频繁移床以及MRI扫描孔边沿处的磁场梯度较大有关,对植有人工耳蜗的患者行MRI检查时应注意缓慢移床。 人工耳蜗在MRI扫描中虽有产热的风险,但在1.5 T(含)以下的磁场环境中还是比较安全的。 4.骨科植入物 骨科植入物(如钢板、钢针、螺钉以及各种人工关节等)大多呈非铁磁性或少量弱磁性,由于在术中已被牢固地固定在骨骼、韧带或肌腱上,通常不会移动。但植入物可能会引入图像伪影,影响周围组织的观察。另外,也有发生热灼伤的风险。 5.外科和介入器材 各种穿刺活检手术,包括各种MRI引导下的治疗(如引流、射频消融、微波治疗和无水乙醇注射等),所用穿刺定位针、导丝、导管、射频消融和微波治疗等设备均应是非铁磁性的。铁磁性的穿刺针在强磁场下可发生移位和误刺,带有铁磁性的设备可能发生抛射,具有很大的危险性。 目前已有专门用于MRI引导下介入手术的各类穿刺针、活检针、导管、导丝及相应的监护设备。另外,在MRI引导下植入放射性粒子也需相应的非铁磁性器材,放射粒子的壳为钛合金材料,植入后行MRI检查是安全的。 6.输液泵和留置导管 输液泵通常植入于胸部皮下,由穿刺座和静脉导管系统组成,材料主要有合金、硅橡胶和塑料等,呈非铁磁性和弱磁性,因此进行MRI检查是安全的。带有胰岛素泵的患者在进入MRI检查室时应移除胰岛素泵,因为强磁场可能会破坏胰岛素泵功能。 7.牙科植入物 许多牙科植入物(如种植牙、固定的假牙和烤瓷牙等)含有金属和合金,有些甚至呈现铁磁性。由于种植牙已牢固地固定在牙槽骨上或黏合在相应的连接物上,具有很高的强度,通常在3.0 T(含)以下场强的MRI设备中不会发生移动和变形,但在牙科植入物所在的部位可能会出现一些伪影。 8.宫内节育器及乳腺植入物 金属宫内节育器一般由铜制成。目前尚未发现宫内节育器在3.0 T(含)以下MRI检查中引起明显不良反应,但可能产生伪影。 乳腺整形手术和隆胸所用的植入物大多为非铁磁性物质,这些患者行MRI检查是安全的,但少数整形用的配件可能带有金属,应予以注意。 9.冠脉与外周血管支架 几乎所有市面上的冠状动脉支架产品在MRI时都是安全的,可在3.0 T(含)以下的MR设备上进行检查。2007年前的外周动脉支架可能存在弱磁性,但通常认为在手术6周后也可以行MRI检查。 10.人工心脏瓣膜和瓣膜成形环 市面上几乎所有的人工心脏瓣膜和瓣膜成形环都是MRI安全的,手术后任意时间都可在3.0 T(含)以下的MR扫描仪中进行检查。但由于不同厂家产品的差异性,还是应在MRI检查前对材料进行确认。 11.眼内植入物 磁性眼内植入物,有可能在强磁场中发生移位,这类患者不宜进行MRI检查。 此外,考虑到射频场热效应(致热效应),共识指出,高热患者不宜行MRI检查,还需注意如下问题: 在MRI检查前,要将受检者体外所有不必要的导电材料移除;如果受检者衣服内含有不可拆卸的导电材料,建议为其更换特定的检查服。 只要皮肤表面的金属钉或缝线不是铁磁性的,而且也不在射频辐射区域内或附近,受检者就可以进行MRI检查。 如果成像区域覆盖了大面积或深色的纹身(包括纹眼线),为了减少热量累积,建议在MRI扫描过程中敷上冰袋降温;同时告知受检者,MRI扫描可能会使48 h之内的纹身图案变得模糊。 一些药物贴片中含有金属,为避免MRI扫描时贴片过热发生危险,一般可将冰袋置于金属贴片上进行冷敷;然而,这样做有时会影响药物传送速率以及吸收效果。
杨祎 主治医师 北京安贞医院 主动脉外科中心9102人已读 - 就诊指南 主动脉夹层的中国专家共识
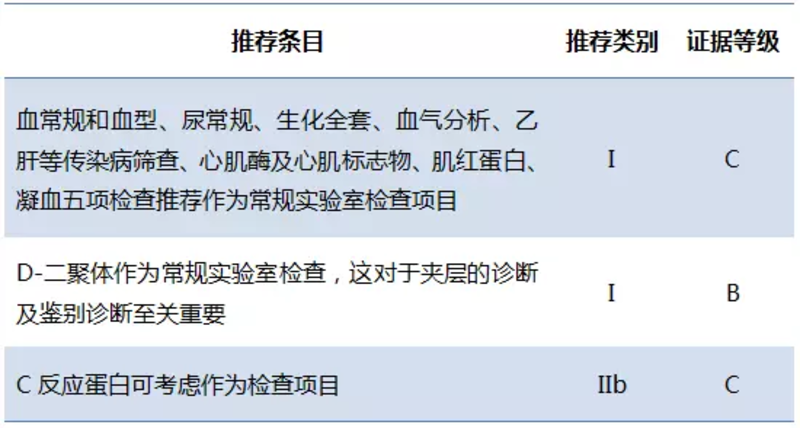
主动脉夹层(aortic dissection,AD)是一种严重的心血管急、危、重症,起病急,进展快,非常凶险,病死率极高。尽早诊断才能把握先机,获取挽救患者生命的可能性。2017年底发布的《主动脉夹层诊断与治疗规范中国专家共识》对主动脉夹层的分型、分期、临床表现、辅助检查和治疗流程进行了全面的总结。 共识指出,与发达国家相比,我国AD患者存在下述特点:(1)病因以高血压为主,青壮年多,高血压的知晓率和控制率比发达国家低;(2)患者的平均年龄较发达国家低10~20岁,预期寿命长。 一、AD的危险因素 AD发病主要和以下危险因素有关:①增加主动脉壁张力的各种因素,如高血压、主动脉缩窄、外伤等;②导致主动脉壁结构异常的因素,如动脉粥样硬化、遗传性结缔组织疾病(如Marfan综合征、Loeys-Dietz综合征、Ehlers-Danlos综合征等)、家族性遗传性AD或主动脉瘤、大动脉炎等;③其他因素如妊娠、医源性AD等。 国内多中心研究表明,高血压、Marfan综合征、吸烟、饮酒、主动脉瓣二叶畸形(BAV)、动脉粥样硬化等是国人AD发病的主要独立危险因素。文献报道国人AD患者高血压发生率为50.1%~75.9%。 急性AD患者死亡的主要原因是主动脉破裂、急性心脏填塞、急性心肌梗死、卒中、腹腔脏器缺血、肢体缺血等。 二、国际分型和孙氏细化分型 1.DeBakey分型 I型:原发破口位于升主动脉或主动脉弓,夹层累及大部或全部胸升主动脉、主动脉弓、胸降主动脉、腹主动脉; II型:原发破口位于升主动脉,夹层累及升主动脉,少数可累及主动脉弓; III型:原发破口位于左锁骨下动脉以远,夹层范围局限于胸降主动脉为IIIa型,向下同时累及腹主动脉为IIIb型。 2.Stanford分型 夹层累及升主动脉者为Stanford A型,相当于DeBakey I型和Ⅱ型;夹层仅累及胸降主动脉及其远端为Stanford B型,相当于DeBakeyⅢ型。 图1 Stanford分型和DeBakey分型 3.孙氏细化分型 北京安贞医院孙立忠教授团队根据我国AD的发病特征,在Stanford分型的基础上提出了AD细化分型(亦称孙氏分型)。 (1)Stanford A型主动脉夹层的孙氏细化分型 根据主动脉根部受累情况细分为3个亚型: A1型,窦管交界和其近端正常,无主动脉瓣关闭不全; A2型,主动脉窦部直径小于3.5cm,夹层累及右冠状动脉,致其开口处内膜部分剥离或全部撕脱,轻至中度主动脉瓣关闭不全; A3型根部重度受累型,窦部直径大于5.0cm,或直径为3.5~5.0cm但窦管交界结构破坏,有严重主动脉瓣关闭不全。 根据病因及弓部病变情况分为C型(复杂型)和S型(简单型): 符合以下任意一项者为C型:①原发内膜破口在弓部或其远端,夹层逆行剥离至升主动脉或近端主动脉弓;②弓部或其远端有动脉瘤形成(直径大于5.0cm);③头臂动脉有夹层或动脉瘤形成;④TEVAR术后逆撕A型AD;⑤套筒样内膜剥脱和广泛壁内血肿:⑥主动脉根部或升主动脉术后残余夹层或新发夹层;⑦病因为遗传性结缔组织病,如Marfan综合征。 S型:原发内膜破口位于升主动脉且不合并上述任何一种C型病变。临床诊断时根据实际情况组合分型,如A1C型。 图2 Stanford A型主动脉夹层的孙氏细化分型 (2)Stanford B型AD的孙氏细化分型 根降主动脉的扩张部位分为3个亚型: B1型:降主动脉无扩张或仅近端扩张,中、远端直径接近正常; B2型:全胸降主动脉扩张,腹主动脉直径接近正常; B3型:全胸降主动脉、腹主动脉均扩张。 根据病因及弓部有无夹层累及亦分为C型和S型: 符合以下任意一项者为C型:①夹层累及左锁骨下动脉开口或远端主动脉弓;②合并心脏疾病,如瓣膜病、冠心病等;③合并近端主动脉病变,如主动脉根部瘤、升主动脉或主动脉弓部瘤等;④病因为遗传性结缔组织疾病,如 Marfan综合征。 S型:不合并上述任何一种情况者。 图3 Stanford B型主动脉夹层的孙氏细化分型 三、AD的临床表现 1.疼痛 疼痛是AD患者最为普遍的主诉。AD导致的疼痛常被描述为“撕裂样”或“刀割样”持续性难以忍受的锐痛。部分患者亦可无疼痛症状。 疼痛的部位和性质可提示AD破口的部位及进展情况。Stanford A型夹层常表现为前胸痛或背痛,Stanford B型夹层常表现为背痛或腹痛,但两者疼痛部位可存在交叉。 对于剧烈胸背痛且伴高危病史及体征者应怀疑AD的可能;出现迁移性疼痛可能提示夹层进展,如患者出现下肢疼痛,则提示夹层可能累及髂动脉或股动脉。 2.心脏并发症 心脏是Stanford A型AD最常受累的器官。AD可导致心脏正常解剖结构破坏或心脏活动受限从而引起相关症状: (1)夹层导致主动脉根部扩张、主动脉瓣对合不良等可引起主动脉瓣关闭不全,轻者无明显临床表现,重者可出现心力衰竭甚至心源性休克。 (2)夹层累及冠状动脉开口可导致急性心肌梗死、心功能衰竭或恶性心律失常,患者可表现为典型的冠状动脉综合征,如胸痛、胸闷和呼吸困难,心电图ST段抬高和T波改变。 (3)夹层假腔渗漏或夹层破入心包可引起心包积液或心包压塞,发生率约为17.7%。 (4)急性主动脉瓣关闭不全、急性心缺血或梗死及心包压塞常表现为心力衰竭。 3.其他脏器灌注不良表现 AD累及主动脉的其他重要分支血管可导致脏器缺血或灌注不良的临床表现: (1)夹层累及无名动脉或左颈总动脉可导致中枢神经系统症状,3%~6%的患者发生脑血管意外,患者表现为晕厥或意识障碍;夹层影响脊髓动脉灌注时,脊髓局部缺血或坏死可导致下肢轻瘫或截瘫。 (2)夹层累及一侧或双侧肾动脉可有血尿、无尿、严重高血压甚至肾功能衰竭。 (3)夹层累及腹腔干、肠系膜上及肠系膜下动脉时可引起胃肠道缺血表现,如急腹症和肠坏死,部分患者表现为黑便或血便;有时腹腔动脉受累引起肝脏或脾脏梗死。 (4)夹层累及下肢动脉时可出现急性下肢缺血症状,如疼痛、无脉甚至下肢缺血坏死等。 4.AD的体征 疑似AD的患者出现以下体征有助于临床诊断: (1)血压异常:AD常可引起远端肢体血流减少,导致四肢血压差别较大。若测量的肢体是夹层受累一侧,将会误诊为低血压,从而导致误诊和错误治疗。因此对于AD患者,应常规测量四肢血压。50.1%~75.9%的AD患者合并高血压,但也有部分患者就诊时表现为低血压,此时应考虑心脏填塞的可能。 (2)主动脉瓣区舒张期杂音且患者既往无心脏病史,则提示夹层所致急性主动脉瓣反流可能。 (3)胸部体征:AD大量渗出或者破裂出血时,可出现气管向右侧偏移,左胸叩诊呈浊音,左侧呼吸音减弱;双肺湿啰音提示急性左心衰。 (4)腹部体征:AD导致腹腔脏器供血障碍时,可造成肠麻痹甚至坏死,表现为腹部膨隆,叩诊呈鼓音,广泛压痛、反跳痛及肌紧张。 (5)神经系统体征:脑供血障碍时出现淡漠嗜睡、昏迷或偏瘫;脊髓供血障碍时,可有下肢肌力减弱甚至截瘫。 四、AD的辅助检查建议 1.实验室检查 胸痛且高度怀疑急性AD的患者,应完善常规检查如血常规及血型、尿常规、肝肾功、血气分析、血糖、传染病筛查、心肌酶、肌红蛋白、凝血5项(包括D-二聚体)和血脂检查。这些检查有助于鉴别诊断及评估脏器功能及手术风险,减少术前准备的时间。 表1 疑诊主动脉夹层患者实验室检查项目的推荐 患者D-二聚体快速升高时,拟诊为AD的可能性增大。研究表明,发病24 h内,当D-二聚体达到临界值500 μg/L时,其诊断急性AD的敏感性为100%,特异性为67%,故可作为急性AD诊断的排除指标。但D-二聚体阴性也不能除外主动脉溃疡或壁间血肿可能。 2.影像学检查 AD的影像学检查目的是要对全主动脉进行综合评价,包括AD受累的范围、形态、不同部位主动脉的直径、主动脉瓣及各分支受累情况、与周围组织的关系,以及AD的其他相关表现如心包积液、胸腔积液及脏器缺血情况等。 表2 疑诊主动脉夹层患者影像学检查的推荐 五、AD的诊断流程 对于急性胸痛的患者,2010 AHA指南中提出了疑诊AD的高危易感因素、胸痛特征和体征。 表3 主动脉夹层的高危病史、症状及体征 IRAD研究基于上述高危因素提出AD危险评分,根据患者符合危险因素分类(高危易感因素、高危疼痛特征及高危体征)的类别数计0~3分(0分为低危,1分为中危,≥2分为高危);该评分≥1分诊断AD的敏感度达95.7%。因此,对存在上述高危病史、症状及体征的初诊患者,应考虑AD可能并安排合理的辅助检查以明确诊断。 图4 主动脉夹层的诊断流程 六、AD的初步治疗原则 AD初步治疗的原则是有效镇痛、控制心率和血压,减轻主动脉剪应力,降低主动脉破裂的风险。 1.镇痛 适当肌注或静脉应用阿片类药物(吗啡、哌替啶)可降低交感神经兴奋导致的心率和血压的上升,提高控制心率和血压的效果。 2.控制心率和血压 静脉应用β受体阻滞剂(如美托洛尔、艾司洛尔等)是最基础的药物治疗方法,但应保证能维持最低的有效终末器官灌注。对于降压效果不佳者,可在β受体阻滞剂的基础上联用一种或多种降压药物。 AD患者降压药物的选择、用药方案及注意事项详见相关指南。药物治疗的目标为控制收缩压至100~120 mmHg、心率60~80次/min。 需注意的是,若患者心率未得到良好控制,不要首选硝普钠降压。因硝普钠可引起反射性儿茶酚胺释放,使左心室收缩力和主动脉壁切应力增加,加重夹层病情。 进一步治疗方案应根据AD的类型、合并症、疾病进展等因素综合考虑。 来源:孙立忠. 主动脉夹层诊断与治疗规范中国专家共识. 中华胸心血管外科杂志. 2017, 33(11): 641-654.
 杨祎 主治医师 北京安贞医院 主动脉外科中心8765人已读
杨祎 主治医师 北京安贞医院 主动脉外科中心8765人已读 - 就诊指南 出现造影剂过敏以后还可以做造影吗?
 杨祎 主治医师 北京安贞医院 主动脉外科中心5202人已读
杨祎 主治医师 北京安贞医院 主动脉外科中心5202人已读 - 就诊指南 做了心脏手术还能做核磁吗?(转载)
转自微信公众号,夏与何谈心脏 临床工作中,经常会碰到做了心脏瓣膜手术,特别是换了机械瓣膜的患者,如果腰椎不好了,想做个磁共振。结果放射科医生说你这个有金属瓣在心脏里,磁共振不能做的。你看人家把轮椅带进去,直接就吸在磁共振上下不来了。你的瓣膜也是金属的,会被吸出来的!!!是不是有种不明觉厉的恐慌呢。 其实这个误区不能怪放射科医生,很多心外科医生包括早期的夏医生,也是同样的想法。直到2007年美国心导管诊断介入学会领衔多家学会发布的《心血管器械植入患者MRI检查安全性科学申明》和2010年美国心脏病学基金会领衔制定的《心血管磁共振专家共识》的发布,才让我们对这个事情有了全面的了解。 我们对心脏有金属植入物的做磁共振主要会有两个担心,第一怕金属植入物在磁共振机的磁场影响下移位。其次,怕磁共振射频脉冲可使金属局部的温度升高,烫伤了心脏。对于以上两个担心,夏医生将一一解释。首先,我们的瓣膜都是手工缝合上去的,而磁场施加于人工瓣膜的力量远低于心脏跳动、射血产生的冲击力,有研究证实手术缝线固定瓣环组织的力量比4.7特斯拉场强产生的磁诱导力(目前医院常用磁共振最高场强3.0特斯拉)还要大得多。看到下面这张密密麻麻的缝线,你是不是觉得心安了不少呢。 目前的机械瓣膜,材料都是弱磁性的,在≤3.0特斯拉的磁共振中,产生的温度并不高,加上心脏内血液的流动带走热量,因此完全不用担心产热会烫伤心脏组织。来看看目前常用的几种瓣膜的说明书上怎么写的吧,看了以后,是不是完全心安了呢。 目前医院里面常规使用的磁共振,最大磁场强度为3.0特斯拉。也就是说我们所换的瓣膜,是可以立即进行磁共振扫描的。不过,我们要注意到,瓣膜的存在会导致它周围磁共振成像出现伪影。所以对于心脏磁共振,还是不建议做,因为显示不清。 在心外科,植入材料除了心脏瓣膜是金属的,还有一项植入物,几乎所有手术病人都要使用,那就是钢丝,用作胸骨的缝合。这个也是金属材质,夏医生往往会告诉手术后的病人,上飞机过安检的时候,警报器到胸口的时候可能会滴滴的报警,这时候淡定的来一句“我做过心脏手术的”,保证你不会被当作恐怖分子。 关于钢丝,夏医生还有个真实的故事要讲,也正是这个故事,让夏医生有了写这篇文章的想法。一位心脏术后的患者,因为腰部疾患需要做腰椎磁共振,结果放射科医生死活不给做,说是有钢丝不能做磁共振。最后,患者不得不去到外科开刀拿掉钢丝。夏医生第一次听到这个事件的时候也是很震惊的,医务人员尚且有这么大的认识误区,更不用说对医疗毫无所知的患者。在这里,请允许夏医生一一解释。 首先,我们现在用的钢丝,材料是316L不锈钢。夏医生特意拿来了钢丝的说明书展示下。 这个316L不锈钢其主要成分是铬和镍,搜索下百度,可以看到这款不锈钢是弱磁性或无磁性的。 钢丝的缝合是固定在胸骨上,比瓣膜的缝合更加牢固。并且,深埋在皮下组织和皮肤之下,再加上几乎无磁性状态,在3.0及以下的磁场中是很安全的。至于产热情况,因为钢丝本身极为纤细,对应瓣膜这样大片金属在磁场中才上升1度左右的产热,纤细的钢丝产热完全可以忽略不计。所以,带钢丝的患者去做磁共振,没问题!!! 心脏外科还有一类疾病,叫主动脉夹层,治疗方案中可能会放入一个主动脉的支架。这个支架也是含有金属的。 夏医生找了一个支架的说明书,里面也有关于磁共振的说明 划线的部分翻译过来,其实和瓣膜的说明类似,,在3.0及以下强度,最大空间磁场梯度为720高斯/厘米或以下做磁共振是安全的。 最后,还需要着重指出,夏医生所有的资料都来自于近期。非常早期的瓣膜及支架有可能不适用,但是每个瓣膜或者支架都会有一本使用说明,做磁共振之前请参阅说明。 希望看过这篇文章的患者,可以不再出现为做磁共振再去做一次手术的悲剧。
杨祎 主治医师 北京安贞医院 主动脉外科中心9154人已读






