梁磊医生的科普号
- 精选 FAP患者的腹腔镜次全结肠切除noses手术
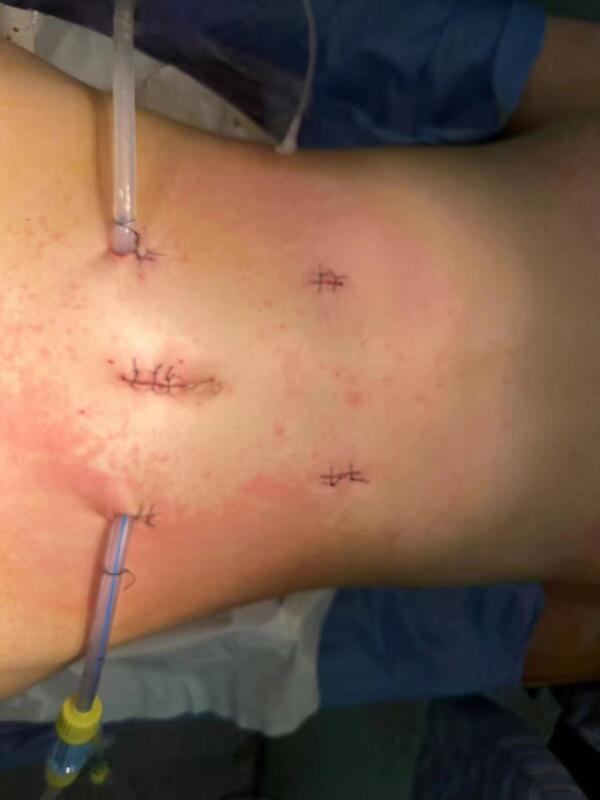
近期,成功进行一例次全结肠的noses手术,先介绍一下病例,患者女,18岁,未婚未育,因腹部不适2月入院,外院肠镜提示全结肠及直肠布满大小不等息肉,约0.3-1.5cm,病理:管状腺瘤伴低级别上皮内瘤
 梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科106人已读
梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科106人已读 - 医学科普 老梁肠谈——高龄老人得了肠癌能手术么?
近期,收治了一例的高龄女性肠癌患者,老太太95岁,因便血半年,伴近期腹痛入院,肠镜提示距离肛门5-8cm见环周不规则肿物伴狭窄,肠镜无法通过。病理腺癌。磁共振直肠中下段增厚,肿瘤可能。术前检查无远处转
 梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科460人已读
梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科460人已读 - 典型病例 侧方淋巴结清扫病例
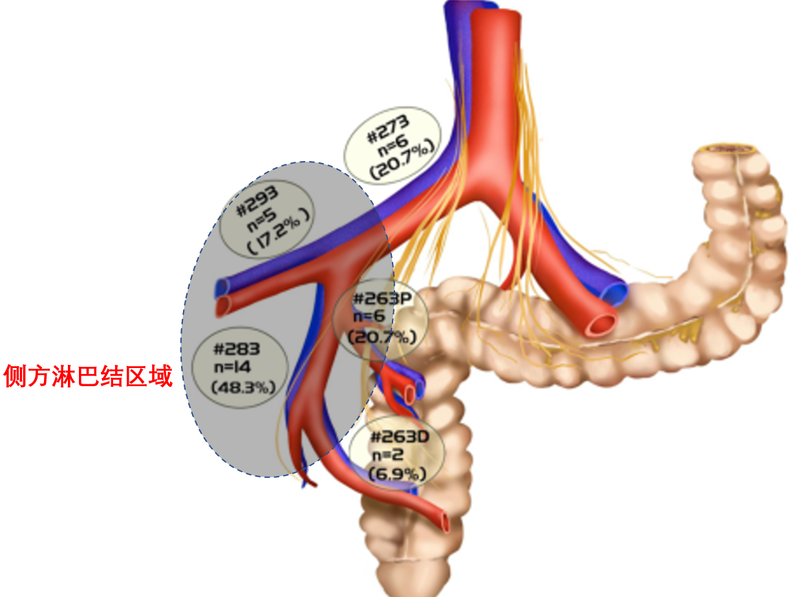
患者为50岁女性,肛管癌新辅助放化疗后,既往肠镜提示距离肛门8cm弥漫隆起病变,病理提示腺癌。磁共振:肛管直肠占位,分期T2N1a,MRF-,EMVI-,有侧髂内血管旁、有腹股沟强化淋巴结,短径12mm。我院于2022年4月行放疗,经放化疗直肠占位较前缩小,右侧髂血管旁及腹股沟淋巴结较前缩小。患者于近期行腹腔镜下miles术+右侧侧方淋巴结清扫术+右侧腹股沟淋巴结清扫术。侧方淋巴结是定义为直肠系膜以外的直肠侧方的淋巴结,位于直肠侧方的髂外和髂内血管旁,以及二者之间的闭孔神经区域。通常直肠癌的侧方淋巴结转移并不常见,但是一旦发生,通常意味着局部肿瘤的分期偏晚。因为该区域并不属于直肠癌手术的清扫区域,所以若不能清扫,势必导致后续肿瘤的复发。 侧方淋巴结的区域血管神经丰富,包括闭孔神经,髂内髂外动静脉、膀胱动静脉、闭孔动静脉等重要血管和神经,区域狭小,清扫难度及出血风险高,既往认为侧方淋巴结若出现转移即为远处转移,加上侧方淋巴结清扫存在手术时间长、增加术中出血量、影响排尿及性功能等并发症,所以并不常规开展侧方淋巴结清扫,而以新辅助放化疗和直肠癌TME手术模式替代侧方淋巴结清扫术。但是后续发现术前新辅助放化疗尽管能有效降低局部乃至侧方型局部复发,但并不足以彻底杀灭已经存在的侧方转移性淋巴结。对于经过放化疗后淋巴结仍然偏大的复发的概率较高,所以侧方淋巴结清扫依然有进行的必要。腹腔镜技术的发展为侧方淋巴结清扫提供了便利的条件,并降低了术中并发症的发生概率,腔镜可视化操作可实现精细分离以使术中出血量的最小化,为该术式的推广提供了良好的基础。
 梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科603人已读
梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科603人已读 - 典型病例 腹腔镜左半结肠的全腔镜吻合
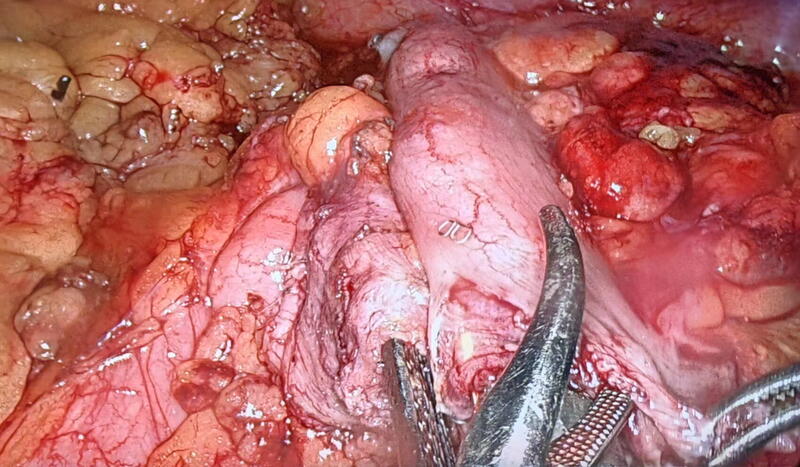
患者为55岁男性,体重约85kg,较为肥胖,肿瘤位于结肠脾曲,行标准腹腔镜左半结肠切除,全腔镜吻合,overlap术式,切除肠管约20cm,肿瘤远近端各切除约10cm左右。切口长度约5cm,位于左下腹
 梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科247人已读
梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科247人已读 - 医学科普 TAMIS手术病例:特别的爱给特别的你
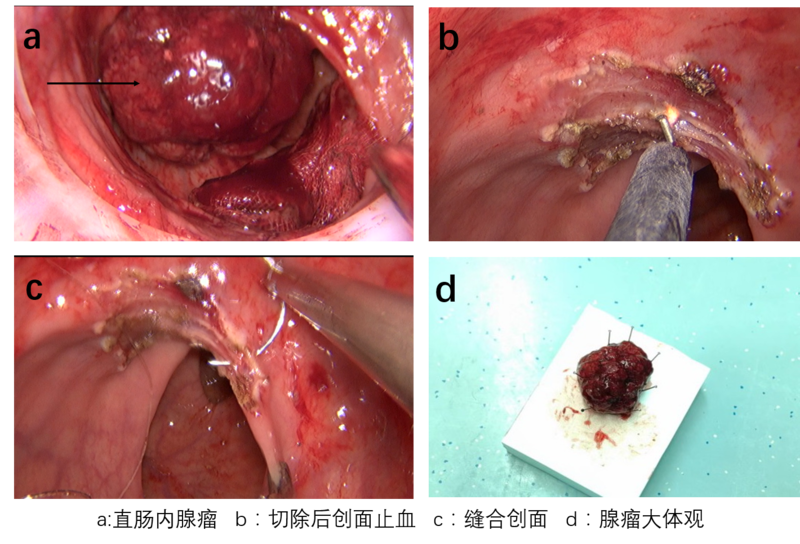
患者老年女性,83岁,因大便出血4月入院,患者术前肠镜提示进镜至肛缘约10cm处因固态粪便不能进镜,距离肛门约3-7cm见大小约44cm,宽基粘膜隆起,呈绒毛状改变,活检质软。病理:绒毛状腺瘤,伴低级别上皮内瘤变。肛门指检:肛门松弛,直肠内充满固态大便,肿瘤位于距离肛门4cm处,质地软,大小约45cm,未明确扪及肿瘤蒂部。考虑患者高龄,肛门功能差,病理绒毛状腺瘤合并低级别瘤变,良性可能性大。决定行经肛手术,肠道准备后扩肛,见肛内肿瘤大小约55cm大小,充满肠腔,肿瘤的蒂部位于距离肛门约7cm,宽蒂,遂决定行TAMIS术。 手术过程:充分扩肛后置入port,低气腹压力,直视下剥离肿瘤蒂部,完整切除肿瘤,3-0倒刺线缝合创面。患者术后恢复好,术后第二天出院。术后病理:绒毛状腺瘤伴低级别上皮内瘤变,切缘阴性。经肛门微创直肠肿瘤切除术(TAMIS术),是将腹腔镜通过通道置入肛管,利用常规腹腔镜器械经肛门途径完成直肠肿瘤局部切除和根治手术。TAMIS最大的特点就是无需专门设备,利用常规单孔腹腔镜通道和腹腔镜器械即可完成手术。经肛门手术主要适用于直肠早期癌,直肠癌放化疗后退缩完全仅剩疤痕患者,直肠神经内分泌肿瘤,直肠巨大绒毛状腺瘤,间质瘤等患者。传统的经肛门手术只能对距离肛门5cm以内的病变进行治疗。中段及上段直肠病变距离肛门较远,已经超越了传统经肛门手术的极限。而内镜粘膜切除术(EMR)或粘膜下剥离术(ESD)一般适用于表浅病变进行切除,完整切除较为困难,尤其是实施肠壁全层切除患者,切除后的创面缝合关闭困难。所以面对这些困境,很多患者只得接受腹腔镜或开腹手术切除病变肠管,手术创伤较大,并发症多,住院时间长,费用昂贵。经肛门腔镜手术(TAMIS)的出现,给这些患者带来了福音,适用于距离肛门5-15cm直肠的病变切除,并可行创面的关闭,具有安全有效,并发症少、住院时间短,费用低廉等优势。该手术特别适用于直肠良性肿瘤包括巨大的绒毛状腺瘤、间质瘤、神经内分泌肿瘤的切除手术。该手术示例的患者的特点是高龄、肛门功能差、大便有失禁、肿瘤较大且为良性、肿瘤的根部在距离肛门约7cm处,是该手术的适应症,通过该手术治疗,患者避免了行直肠部分切除的手术,既有效的切除了病变,又保留了直肠器官功能,减少或者避免了术后并发症的发生,所以针对不同的疾病特点,选择不同的适合的手术方式,才能最大程度上使患者获益。
 梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科420人已读
梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科420人已读 - 精选 个人手术案例展示
标准术式1、结肠手术腹腔镜右半结肠手术是结直肠癌手术中难度较大的手术之一,其原因在于右半结肠血管变异较多,此外,标准的右半结肠手术需要显露及清扫肠系膜上静脉乃至肠系膜上动脉旁淋巴脂肪组织(D2/D3根
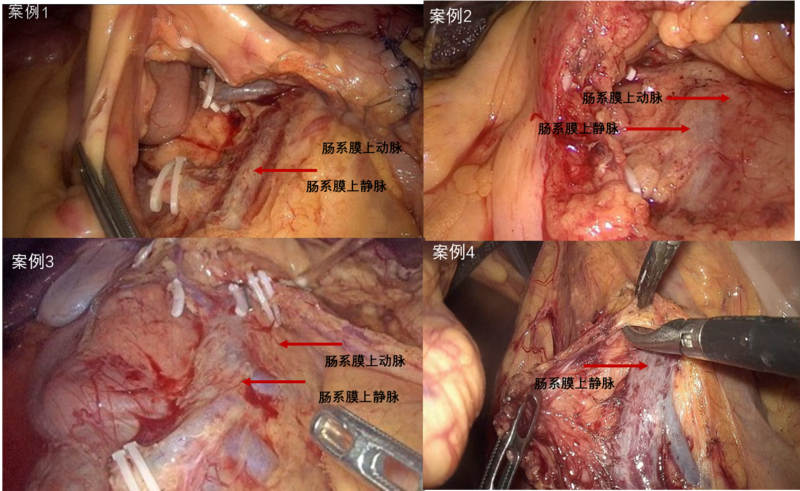 梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科550人已读
梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科550人已读 - 精选 老梁“肠谈”:保肛——你知道的和不知道的那些事
“医生,我能不能保肛啊?”这句话恐怕是门诊碰到直肠癌病人问的最多的话了。大部分人都对是否能够保肛感到焦虑,可以看出在患者心中,对于改道手术存在巨大的心理压力。甚至有的病人还表达出“如果保不了肛,我就坚决拒绝手术“的决心。大部分患者会认为是医生掌握了自己保不保肛的决定大权,也可能会有医生会解释:保不保肛还不是由你的病情决定的。那么保肛究竟是怎么个事情,简单的几句话真说不清楚,这涉及到手术技术和病人自身的各个因素,总体来说是五分看天,五分看人,这里我将从解剖、手术技术和适合手术的人群方面谈谈这个问题。首先我们简单的了解下下半身这些事---直肠肛管的解剖知识。直肠肛管不仅仅是一个粪便的出口,更重要的是它是一个高度精密的“阀门”。但是肛门并不像阀门一样单薄,其实是一个管状的肌肉环,外口是我们看到的肛门口,内口是以齿状线为界限,大致长度在2.5-3cm左右。直肠的长度大致在15cm(距离肛门外口的距离),根据距离我们将直肠分为中高位直肠(距离肛门外口7-15cm),低位直肠(距离肛门外口3-7cm)。为什么要以7cm为界限,这里需要解释下,人体的腹膜返折距离肛门约7cm左右,简单的讲7cm以下的直肠是被后方及两侧的骨盆及前方的器官包绕的,而7cm以上是位于骨盆外腹腔里的,这两个部位手术的解剖和困难程度是有差异的,因此是以7cm为界限定低位直肠。下面我们再了解下围绕直肠的周围结构,包绕直肠的骨盆呈漏斗状,包括直肠后方的骶骨,左右两侧的髂骨,直肠前方则是骨性的耻骨联合,男性直肠前方还有前列腺及膀胱,女性则为子宫、阴道等脏器。在这漏斗状的盆腔里面,肛管就是漏斗的出口,环绕直肠肛管的是丰富的盆底肌肉(肛提肌,顾名思义把直肠肛管提着),能够通过肌肉的收缩,参与控便和排便。了解了直肠肛门的基本结构后,我们再聊聊在手术技术上保肛的困难性究竟在哪里以及各种保肛手术的特点。首先我认为距离肛门7cm以上的肿瘤无论开放手术和腹腔镜手术保肛的困难性均不大,除非碰到肿瘤巨大,或者侵犯周围脏器(膀胱,子宫,骶骨等),这部分不在本文的讨论范围内。本文讨论的是距离肛门7cm以下的低位直肠癌的保肛手术。目前直肠癌的手术类型主要分为传统的开腹手术及腹腔镜手术以及腹腔镜手术衍生的手术方式等。1、传统的开放手术传统的开放手术即传统的开大刀手术,取下腹部的切口大概15-20cm,完成直肠手术。传统的开放手术在外科手术的发展阶段起着不可磨灭的作用,并且目前依然是主要的手术方式之一,手术的优点在于外科医生手的精密和灵活性及腹腔镜手术器械所无法带来的触感。但是需要指出的是,在做低位直肠时有其天然不能克服的劣势,分离低位直肠时,因为骨盆的天然弯曲,直肠下段的解剖肉眼无法直视观察,所以通常此时,主刀需要通过助手的S形拉钩进行强力的牵引,而主刀的右手则深入盆底,通过触感分离远端直肠的系膜结构,这样做的后果是直肠的系膜可能会有残留,或者低位肿瘤无法完全游离,显露肿瘤下缘。特别尴尬的是,男性的或者是肥胖的患者,骨盆狭小,加上肠管粗大,骨盆甚至不能容下主刀的一只手,所以主刀往往累了一头汗,但是效果还不好,最终这部分病人将以挖肛门收场,或者勉强保肛后早期复发了。国内的corean研究经过10年的随访,评估低位直肠腹腔镜和开腹手术的长期随访结果,结果显示10年局部复发率开腹手术组要显著高于腹腔镜手术组(复发风险2.22倍),原因大致如此。2、腹腔镜手术我们需要知道的是腹腔镜的优势并不仅仅是通常理解的腹部小切口。腔镜设备在经过20余年的发展已经非常完善。4k、3d的高清显示器基本已经在市级的医院普及,自动除烟稳压的气腹机在我院也普遍应用。在这些高端的设备的加持下,加上腹腔镜特有的5倍左右的放大作用,和镜头的可旋转,术中可以深入盆底,非常清晰观察直肠及周围的任何一个角落,这个是低位保肛的基础。在目视下仔细解剖、分离,在不影响肿瘤的根治性前提下,又能保护盆腔自主神经等重要组织,从而最大程度保留患者的性功能和泌尿功能,使得低位直肠癌患者的高质量的保肛成为可能。那么既然比开腹好,腹腔镜手术的保肛难度在哪里?这里还是要提到骨盆的S形结构及右侧的髂骨所构成的反弧形。直肠在进入骨盆后会沿着骶前反向向上,医生的主刀位置是在患者的右侧。操作中,直肠的后壁和左侧壁游离一般不会遇到困难,但是在前壁游离时,前壁的突出部(男性膀胱、前列腺,女性子宫)会影响操作,因为腹腔镜器械是直线器械(下图),反弧形的突出部位会导致低位超声刀头无法继续游离直肠前壁和男性前列腺的间隙,而右侧盆壁形成的反弧形也会导致低位直肠的右前侧分离困难。这种现象尤其在男性的肥胖的、壮硕的患者中出现(通常称为困难骨盆,过程像钻山洞、打隧道),而女性患者因为生产的原因,骨盆宽大(术中经常戏称宽如大海),一般不会出现分离困难,所以女性极低位保肛非常常见。另外使用的腹腔镜闭合器(用于离断直肠)宽度大概有1cm左右,这点浪费在保肛寸土寸金距离战中尤为可惜,此外由于目前闭合器的设计,往往无法和盆底的漏斗状形状贴合,浪费了直肠远端(尤其右侧壁)的长度,因此对于男性的困难骨盆,该种情况会直接导致低位或者极低位保肛困难,往往以挖肛门结束。3、经肛TATME手术外科医生们是不会向困难妥协的,既然从上向下分离比较困难,那是是否可以反其道而为之?从肛门进去,从屁股向上分离,最终和腹侧的手术组汇合,这就是目前比较流行的TATME手术。手术分为两组人马,腹侧的进行常规的分离,屁股侧的医生则把肛门扩开,经肛门放入腔镜器械,从肛门的内口处断掉直肠,然后沿着系膜边缘和腹侧组会师,最终将直肠从肛门拖出,取出肿瘤后,将直肠和肛门内口缝合或者用吻合器吻合。这种方式其实是解决了腹腔镜从上而下手术碰到的困难,经肛直视下离断肿瘤远端直肠,也可以帮助术中判断肿瘤下缘的安全距离,所以TATME手术适用于这种极低位直肠癌,特别适合男性、肥胖、骨盆狭窄等“困难骨盆”的病人。但是我们需要注意目前国内开展的TATME患者的适应症有扩大化的现象,即病人不都是极低位,不少都是距离肛门5-7cm的,这种类型的肿瘤除非有特殊情况,一般经腹侧就能完成手术,没有必要进行经肛手术。经肛的TATME手术的缺点也是有的,整个流程比较繁琐,上下需要两组人马,而且需要两套腹腔镜设备,准备时间长,对于手术量大、人手紧张的医院开展受限制。我们在临床的实践过程中发现上方的腹腔镜手术组往往能分到比较低的位置,经肛组往往只需要在离断肠管后稍微游离后就可以会师,于是又发展了采用经肛直视下免气腹的TATME术,该种方式更为简单,扩肛后直视下离断直肠,稍做分离即可游离末端直肠,完成手术。所以各位病友,有腹腔镜和TATME这两种手术方式,从理论上和技术上来说,基本上保肛是可以实现。每项技术的实施都是建立在前期的技术的发展上,不可能凭空出现一种保肛技术或者发明某些辅助装置一下子大幅度提高保肛概率,希望各位正确甄别网上的一些言论。此外需要注意的是保肛有利必然有弊,就是说保肛可能要付出代价。什么代价?即可能付出肿瘤的根治性这个代价,主要原因有几个:1、追求低位保肛导致离断肠管的下缘过于接近肿瘤下缘,导致剩余肠管有肿瘤残留。2、经肛手术是在直肠腔内操作,即使提前做了荷包封闭肠管,仍然有肿瘤细胞脱落种植的可能。3、肿瘤过于靠近盆底,经肛操作的层面非常重要,有可能因出血等原因层次不清,导致切入肿瘤导致复发。所以经肛手术的长期效果仍需要时间验证。肿瘤治疗的第一原则依然是肿瘤的根治性原则,在此原则基础上尽可能的保留功能,这是肿瘤治疗一直追求的目标。前面我谈了技术上保肛的做法,那么技术上如果可以保肛,但是我们为什么有时候不选择保肛?下面我谈谈哪些情况我们选择不保肛或者慎重保肛。1、肿瘤直接侵犯肛管、侵犯肛门内括约肌(齿状线)、或者侵犯提肛肌。肿瘤直接侵犯肛管是一定不能保肛的,阀门已经坏了,保肛也就失去意义了。如果肿瘤侵犯肛门的内口(或者紧贴)也不建议保肛,肿瘤的切除需要有一定的安全距离,像挖树一样,不能紧贴着树干把树刨掉,这样树根会残留。肿瘤侵犯肛门上方的提肛肌,这种盆底肌肉侵犯的,即使做过放化疗,肿瘤退缩后也不能保证保肛切除路径的肿瘤没有残留。所以采用连同肛门合并部分肛提肌的完整切除才能够尽可能保证肿瘤的根治性。2、女性患者肿瘤位于前壁,直接侵犯阴道后壁女性的直肠前壁肿瘤侵犯阴道后,即使是做放化疗后肿瘤退缩,如果做保肛手术,阴道和直肠间的间隙很难分离,要么肿瘤退化成疤痕,要么还有肿瘤残留,强行分离切除的话可能导致肿瘤的残留,或者保肛后因阴道的损伤导致术后的非常棘手的直肠阴道瘘(大便直接从阴道流出),比较合适的方式是直接切除肛门,并切除肿瘤侵犯的阴道后壁,保证肿瘤的根治性。3、高龄患者,肛门括约肌松弛,功能差正常的肛门需要良好的感知功能和排出功能。首先要感知到大便的到来,在直肠下段、肛门内口处粘膜有神经感受器,能够感知粪便的刺激,使人产生便意,这是正常排便控制的第一步。便意信号产生后,能够控制阀门憋住,等条件允许了,大脑指挥肛门括约肌(阀门肌肉)松弛,增加腹压增高,促使粪便顺利排出。但是低位直肠切除后,破坏了直肠的神经,一个是控制直肠和肛门肌肉运动的神经,导致排便变得不协调。另外一个是神经感受器被破坏,会出现大便已经排出来了才会感知到。所以低位直肠癌手术以后,几乎每个人都出现切除后综合症,症状包括大便出来了还不知道(大便失禁),大多数人一天不停地拉大便(大便次数频繁),但坐到马桶上有拉不出来,或者出来一小颗,起来后又想拉了(排便困难)。对于高龄体弱病人,随着年龄增大,肛门括约肌功会退化,变得松弛。如果低位保肛后,更容易发生大便次数异常频繁甚至大便失禁,据统计直肠癌低位保肛术后10%%的保肛患者的肛门功能差,甚至要求做造瘘手术,所以对于高龄患者极低位保肛还是需要慎重。好了,最后本文做总结,低位直肠癌是否进行保肛手术,需要根据肿瘤、病人以及手术医生的具体情况而定。不适合保肛的应当理解切除肛门的意义,避免纠结。适合并容易保肛的医生将会尽可能保肛,避免永久性肠造口。而位置极低的,可能需要经肛手术的,需要患者和医生详细沟通,了解保肛可能带来的风险,权衡利害后再进行手术治疗。
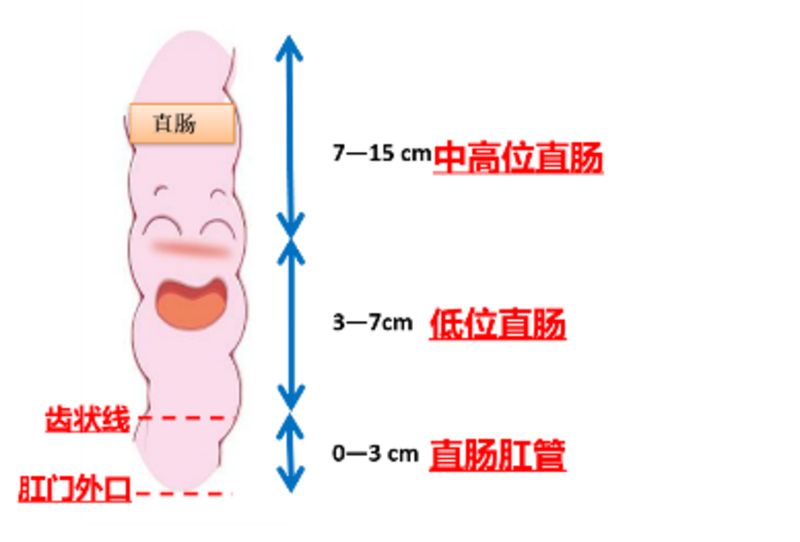 梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科740人已读
梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科740人已读 - 精选 息肉肠镜切除后(EMR/ESD)再补充手术和NOSES手术 ----天然的相互匹配、相得益彰
随着人们健康意识的增强以及内镜技术的提高,更多的早期结直肠癌得到诊治。在内镜治疗方面,根据病变直径的大小,选择内镜下黏膜切除术(EMR)或是内镜下黏膜剥离术(ESD)可完整的切除肿瘤组织,拓宽了内镜下治疗的运用,内镜下治疗成为继外科手术外另一新型治疗方式。 前期的文章已经说明恶性结直肠息肉的再补充手术的危险因素。低危组同时包括切缘阴性、中或高分化腺癌、无脉管癌栓和粘膜下浸润深度<1mm,在内镜下治疗后追加与不追加外科手术者远期预后相当。而高危组患者(无上述特征)包括垂直切缘阳性、粘膜下浸润深度大于1mm、脉管癌栓阳性、低分化腺癌、印戒细胞癌或黏液癌、肿瘤出芽(2或3级),建议行肠切除+淋巴结清扫术 本篇文章将重点讨论选择补充手术的方式选择。目前的常规手术的方式分为3种,开腹手术、腹腔镜手术、腹腔镜noses手术。开腹手术顾名思义就是直接打开腹部切除肿瘤及肿瘤部位,是腹腔镜普及前常规的手术方式,对于肿瘤较大、肿瘤外侵、多次手术后的患者较为合适,但是对于EMR或ESD术后的病人,因原有的肿瘤微小以及肿瘤已经移除,大的手术切口将会对病人造成困扰。常规手术手术切口15~20厘米,术后并发伤口感染、脂肪液化、腹壁疝的概率相应增加,此外,大切口意味着术后疼痛较为剧烈,术后早期活动受限,以及胃肠道功能的恢复缓慢,住院时间相应延长。腹腔镜手术属于微创手术范畴,统称为“打洞”手术,腹部打4-5个孔洞,在腹腔镜操作下进行肿瘤所在肠管的切除及淋巴结清扫,手术创伤较小,患者术后恢复快,术后体验感好。既往的大量的临床试验已经证实,腹腔镜手术对于结直肠癌的根治效果和既往的开腹手术相当,部分甚至还要优于开腹手术。目前该手术方式已经成为各大医院以及地方医院的主流手术方法,对于EMR及ESD术后的病人较开腹手术明显更为合适。不过腹腔镜手术仍然需要在腹部切一个3~5厘米的切口将肿瘤及所在肠管组织取出,切口的并发症的发生几率虽小,但也依然存在。 腹腔镜NOSES手术,称为腹腔镜经自然腔道取标本手术,该手术方式结合了无疤理念与常规微创设备,通过人体自然腔道(直肠、阴道)将手术标本取出,仅留下几个小孔,又称腹腔镜腹部无辅助切口手术。与传统的腹腔镜手术相比,NOSES手术的优势是避免了辅助的取标本切口,具有创伤更小、疼痛感更轻、腹壁功能更好、美容效果更佳、患者恢复更快、心理状态更好等多种优势。因此,该技术也被评价为“微创中的微创”,成为目前胃肠外科的关键技术之一。当然,任何手术都有它的适应症和适应人群,腹腔镜结直肠癌NOSES手术也是如此。分歧点主要在于该手术的特点--经自然腔道取标本,该特点可以说是NOSES手术最大的创新,也正是基于这种颠覆传统认知的创新,才带来了超乎寻常的微创优势,然而获益与风险总是相伴相行,潜在的风险在于无菌和无瘤原则。NOSES手术在术中开放了肠道自然腔道,并且经自然腔道进行取标本等操作,可能会增加了术区污染的机会,并且在取标本过程中,肿瘤细胞一旦脱落到体腔,还可能会造成腹腔的种植转移。基于以上问题,腹腔镜noses手术对于术中操作流程进行了严格的规定,并限制手术的适应症,借此弥补问题,发扬微创优势。目前经过前期广大外科实践者的开展和改进,无菌及无瘤的问题基本可以通过手术程序优化,手术技巧的改进,手术操作的配合来防治和解决。标准操作流程:1、术前充分的肠道准备,排尽大便2、标本拖出前准备,标本切除经肛们拖出,是高位直肠和乙状结肠癌行NOSES手术的主要方式。在肿瘤远端肠管闭合离断之前,远端肠管充分冲洗,在切开远端肠腔之前,腹腔内先放入碘伏纱条,围绕拟切开肠管似“围脖”一样保护、隔离断端。在切开肠腔之时,助手持吸引器,可迅速清理可能外溢的肠液。3、经腹壁Trocar放入无菌塑料保护套,经肛门伸入卵圆钳,经肠腔拖出体外。经塑料保护套自肛门把吻合器抵钉座塞入腹腔;再以卵圆钳钳夹荷瘤肠管的远端闭合端,把手术切除标本经塑料保护套拖出体外。4、,吻合后大量的生理盐水冲洗盆腹腔,减少盆腹腔污染可能。从目前临床结局来看,这些措施是安全的、可行的、有效的。我院与国内多中心资料汇总分析也表明,术后腹腔感染和吻合口瘘发生率并没有增加。对于无瘤的问题,理论上通过这些方法也可以很好的进行预防和控制。从短期临床预后来看,结果也是满意的;但是长期的临床结果,还有待时间验证。 再次回到本文的息肉癌变的补充手术上,目前腹腔镜noses手术的适合人群有较为严格的限制,医生需要为患者“量体裁衣”设计手术方案,不是每位患者都能做腹腔镜NOSES手术,这种术式适合肿瘤较小(肿瘤的大小<3cm)的早中期患者,过度肥胖的患者,因肠系膜比较肥厚,也不太适合该类手术。而息肉EMR/ESD术后,原发肿瘤已经切除或基本切除,对于肿瘤术中种植的顾虑可以基本排除,所以息肉肠镜切除后补充手术和NOSES手术天然契合和匹配,二者相得益彰。腹腔镜NOSES手术不是一个简单的手术,微创成功的关键是建立在术者既往成熟和熟练的腹腔镜操作技巧以及严格的无菌无瘤观念,故目前在较大的医院或中心开展。此外还需要充分的和患者沟通各种手术方式的优缺点,根据患者的具体需求,充分发挥各种手术的优势,使患者获得最大的获益。
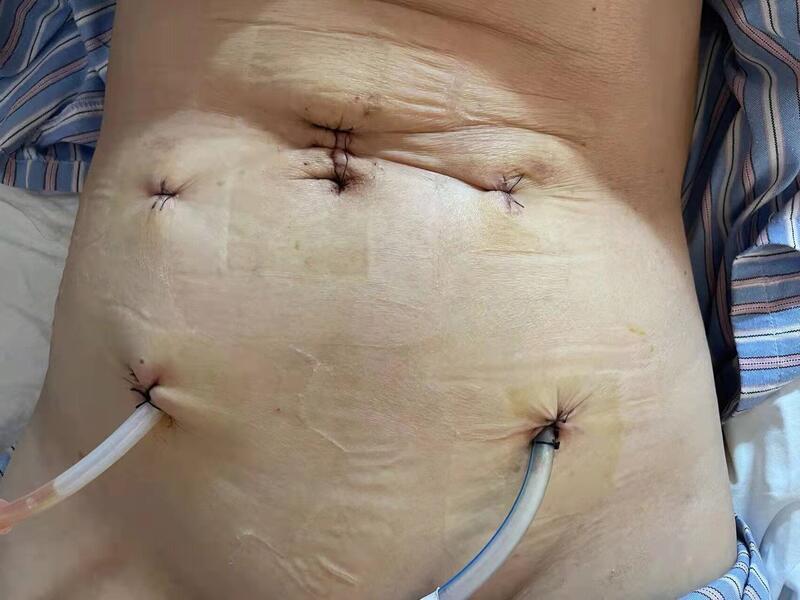 梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科1891人已读
梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科1891人已读 - 案例 TaTme+侧方清扫
治疗前 患者为40岁男性,初诊为距离肛门3.5cm直肠癌,局部病期较晚,肿瘤累及整个肠圈,并且合并有直肠周围双侧髂血管旁多发淋巴结转移,患者年纪较轻,有强烈的保肛和生存意愿。术前行新辅助放化疗,控制疾病的发展,经治疗患者直肠肿瘤及转移淋巴结明显缩小,成功实行腹腔镜下TaTME手术及双侧侧方淋巴结清扫术,彻底切除了直肠肿瘤和侧方的淋巴结转移,保住了肛门。 患者为男性极低位直肠癌,肿瘤下缘距离肛门仅有3.5cm,常规行保肛手术非常困难,虽然目前腹腔镜技术在直肠癌治疗中的保肛中的优势地位已经得以体现,然而对于极低位直肠癌(距肛缘小于5cm),由于病灶深入盆腔,尤其男性病人合并前列腺增生、骨盆腔狭窄、肥胖等因素将会导致手术视野难以充分暴露,势必降低肿瘤的根治效果和保肛概率。 治疗后 治疗后30天 患者为男性极低位直肠癌,肿瘤下缘距离肛门仅有3.5cm,常规行保肛手术非常困难,虽然目前腹腔镜技术在直肠癌治疗中的保肛中的优势地位已经得以体现,然而对于极低位直肠癌(距肛缘小于5cm),由于病灶深入盆腔,尤其男性病人合并前列腺增生、骨盆腔狭窄、肥胖等因素将会导致手术视野难以充分暴露,势必降低肿瘤的根治效果和保肛概率。 腹腔镜下TaTME技术可行性和安全性已被证实,近年来已经逐渐成低位直肠癌手术治疗的新技术热点。该手术采用经肛经腹的“上下协助”方式,经肛组直接从肛缘进入盆底,可以相对容易地完成低位直肠和系膜的完整游离;有效的暴露还有助于保护盆神经丛,增加对术后肛门和性功能保留。此外,常规经腹手术肿瘤的远侧切缘的判断上,术者既往是通过手术器械碰触或助手肛诊来“经验性”地判断,有可能导致远切缘距离不足。而TaTME可经肛直视下离断肿瘤远端直肠,使得远切缘更为精确可靠,以保证肿瘤根治效果。TaTME目前的手术适应证为中低位直肠癌,尤其是低位直肠癌;对于男性、前列腺肥大、肥胖、肿瘤直径&#62;4 cm、直肠系膜肥厚、低位直肠前壁肿瘤、骨盆狭窄、新辅助放疗引起的组织平面不清晰等“困难骨盆”的直肠癌病人。这些患者采用TATME可能更具优势。 该患者同时还合并双侧髂血管周围淋巴结肿大,中低位直肠癌侧方淋巴结转移率可达到23%,一旦发生侧方淋巴结转移则可定义为局部晚期直肠癌。目前术前新辅助放化疗,已使该类病人的存活率有所提高。但仍有多项研究指出,进展期直肠癌术前放化疗后接受直肠手术的局部复发率为7.2%~11.9%,其中侧方淋巴结复发占52.8%~64.6%。因此侧方淋巴结是直肠癌术后局部复发的重要原因,而新辅助放化疗难以消除所有的阳性侧方淋巴结,仍需要进行手术治疗。侧方淋巴结清扫虽然能够降低局部复发率,但难度较高,可能会增加手术相关并发症的风险,而腹腔镜技术因视野清晰,具有放大效果,在狭窄骨盆操作中有助于保护盆腔自主神经,术中的精细操作可减少术中的出血量,从而减少术后并发症的发生,该患者术后排便排尿功能正常,恢复良好。
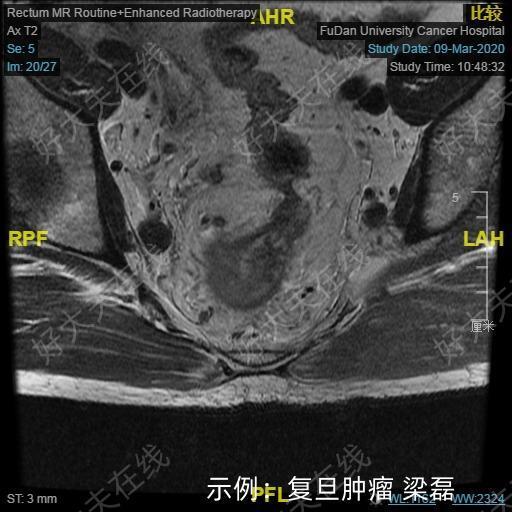 梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科1300人已读
梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科1300人已读 - 精选 老梁肠谈--结直肠癌的腹腔镜手术治疗
临床医疗工作中,经常会遇到患者或家属来咨询,目前结直肠癌手术治疗方式的一些问题,其中询问比较多的是结直肠癌的微创治疗的相关问题,下面就各个问题进行解答。复旦大学附属肿瘤医院大肠外科梁磊1、结肠癌发病情
梁磊 副主任医师 复旦大学附属肿瘤医院 大肠外科2552人已读





