周朋医生的科普号
- 精选 患者的福音:癫痫治疗界的“福尔摩斯”——立体脑电图(SEEG)
专家介绍:周朋,山东第一医科大学第一附属医院(山东省千佛山医院)神经外科副主任医师,医学博士,博士后,硕士研究生导师,从事神经外科临床工作十余年。专业特长:难治性癫痫的综合评估和外科治疗;一直致力于功能性神经疾病的诊疗,尤擅长于各种难治性癫痫的诊疗,在湖南最早开展大脑半球离断术、SEEG引导下致痫灶微创射频毁损术、迷走神经刺激术、机器人辅助双侧丘脑前核以及双侧海马脑深部电刺激术、胼胝体切开术、改良大脑半球切除术等治疗各种难治性癫痫,取得良好的手术疗效。同时擅长意识障碍、帕金森病、运动障碍等功能疾病的神经调控治疗;三叉神经痛、面肌痉挛等微血管减压治疗;神经内镜治疗高血压脑出血、脑肿瘤、垂体瘤等;脑积水、脑功能重建及康复治疗;参与国自然科学基金项目2项,主持省级及校级课题3项。发表论文十余篇,其中以第一作者和通讯作者发表SCI收录文章5篇。学术兼职:中国抗癌协会肿瘤光动力专业委员会青年委员;山东医师协会神经调控专业委员会委员;山东疼痛医学会癫痫专业委员会外科学组委员;山东疼痛医学会神经调控专业委员会委员;山东病理生理学会神经重症专业委员会委员兼秘书;山东研究型医院协会康复医学会常委;山东省健康管理协会神经调控专业委员会委员。警报!警报!大脑摩天大楼预警,有异常放电信号出现!总部已出现癫痫症状,请求支援!请求支援!”注意,这不是演习!这是癫痫发作时,病人脑内的“一场大战”。癫痫是常见的神经系统疾病,它的发作是由脑细胞异常放电造成。反复发作的癫痫,可导致认知功能下降、焦虑、抑郁等心理问题,提高患者过早死亡风险。合理规范的药物治疗,可使70%的发作得以控制,然而仍有30%的患者,药物治疗效果不佳。如何破解这一难题呢?我们请“福尔摩斯”先生出马,通过大脑内的蛛丝马迹,让“不安分”的脑细胞露出马脚,无处遁形。【侦探先生,姓甚名谁?】这位大名鼎鼎的“福尔摩斯”先生,正是立体脑电图技术(SEEG)。如大家所知,侦探先生来自大洋彼岸——它是近年来在国际上兴起的,一种用于识别癫痫发作脑区的微创手术。“福先生”根本不需要大动干戈地破坏“犯罪现场”,只需要头皮和颅骨2mm的微钻孔,就能将“探测器”——深部电极——放置在颅内的任何靶向部位。什么?不相信?你太小瞧侦探先生了。都2022年了,数字化技术早就渗透到各个领域。只要在术前设置好电极的路径,就能够有效地保证疗效。侦探办案,可不会翻箱倒柜地“拆家”。它可以精确地规避颅内动脉、静脉等大脑内的“重要家具”,最大限度地保护脑功能,大大降低手术风险。潜入靶向部位的侦探先生,具有“过目不忘”的强大能力。它可以进行大脑皮层和脑血管的三维重建,凡是被它看过一眼的结构,都可以被原原本本地还原出来。不仅如此,它还能识别大脑深处、常规头皮脑电无法检测到的癫痫发作部位。当“癫痫犯罪分子”出没时,就会赤裸裸地暴露在侦探的眼前,从而被精确定位。当然最厉害的是,侦探先生“身手了得”,如果治疗方案需要,它可以通过电极进行射频热凝治疗,直接“抓获”癫痫分子,实现疾病的微创外科治疗。【三顾茅庐,请他出马?】既然这位侦探——立体脑电图技术(SEEG)——有如此大的本领,那我们要如何才能请得动呢?别急别急,不是所有癫痫患者都需要这位先生帮助的。如果患有全面性癫痫的话,不好意思,先生的力量有限,不能为您提供帮助。但如果您满足以下条件:1、患有局灶性癫痫,使用两种或以上抗癫痫药物均无法有效控制发作。2、无法通过其他检查找到癫痫发作的起源。那么是很有希望通过立体定向脑电图技术帮忙的!首先,医生要针对患者的情况,进行详细的了解,包括疾病的病史,有无先兆,发作时的表现,持续时间、是否有意识丧失等等。了解外在的表现,能够大致明确癫痫的发作形式,为进一步定位癫痫病灶提供症状学的依据。接着,通过监测患者的头皮长程视频脑电监测——就是确保“犯罪分子”在活动,这样才能确保没有“冤枉它们”。获得至少2-3次发作,明确头皮脑电的传播形式,也就是了解它们的“犯罪规律”,才能为“侦探出马”提供充足的理由!最后,结合患者的影像学检查,例如头颅MRI、CT、PET等结果,明确患者是否有神经解剖方面的异常结构。排除了“自己人”作案后,由经验丰富的癫痫团队,根据患者的临床及术前评估结果确定电极的植入方案。以现在的技术,可以在先进的机器人辅助下,医生精确地把立体定向脑电图技术的电极——也就是侦探先生——送到“犯罪现场”进行侦察。在脑电监测系统下,电极可以记录癫痫发作期间的脑电活动,而医生也可以同步监测发作临床表现。根据监测结果,决定采取热凝或其他外科治疗,最终将这些“肇事”细胞绳之以法。圆满完成任务的电极,可以在局麻下取出,通常仅需10-15分钟。【善后工作,是谁来做?】刚才我们提到,可以利用SEEG植入的电极,对致痫病灶进行射频热凝治疗。这就是SEEG引导下射频热凝术。简单来说,这项技术是在医生评估后,决定让侦探先生化身“美少女战士”——代表月亮消灭你——直接对致痫病灶进行射频热凝毁损。它的优点是精准、微创、无痛苦,可以治愈大约7-10%癫痫,超过80%的病例发作能明显减少。但是,由于目前SEEG电极的直径为0.8mm,长2mm,能毁损的范围实在是有限。对于非常小的癫痫灶是可以达到治愈目的的。而对于大的发育畸形或其他比较广泛的病灶,只能缓解,不能治愈,最终的治疗还是需要开颅手术的。另一种“善后”的方式,就是“迷走神经刺激术”,简称VNS手术。它是将电子刺激器植入左侧锁骨下,通过刺激迷走神经,达到治疗调控癫痫的目的。对于耐药性难治性癫痫,如果异常放电部位双侧广泛性,又不适合开颅切除致痫灶手术,最佳的治疗方案,就是采用这种“电子”药物,配合抗癫痫的药物,进行综合治疗。VNS手术疗效确切肯定,安全稳定性高、副作用少。术后减少发作频率占75.5%,10%的患者完全停止发作,17%的患者发作次数减少90%以上。根据患者的不同发作情况,随时进行调控最适合患者的刺激参数,达到最佳的效果。
 周朋 副主任医师 山东省千佛山医院 神经外科161人已读
周朋 副主任医师 山东省千佛山医院 神经外科161人已读 - 学术前沿 《中国中枢神经系统恶性胶质瘤诊断和治疗共识 》
《中国中枢神经系统恶性胶质瘤诊断和治疗共识 》(本共识由中华医学会神经肿瘤专业委员会的22名来自神经外科,神经影像学,神经病理学,放射学和神经肿瘤学领域的专家编写而成)n前言 脑胶质瘤是中枢神经系统(CNS)最常见的肿瘤,其中以恶性者(2007年WHO中枢神经系统肿瘤分类 III,IV级)多见。虽然CNS恶性胶质瘤的预后取决于多种因素和诊治措施,但是,一般III级者生存2-3年,IV级(如胶质母细胞瘤)1年左右。近来,欧美等国先后制订了有关胶质瘤处理的指南或推荐,对规范和提高CNS胶质瘤的诊治很有助益。为此,中华医学会神经外科分会肿瘤专业组牵头,组织国内有关专家,按偱证医学五级分类,随机对照研究“CONSORT”,以及指南“AGREE”程序,多人针对某一问题进行磋商,评估文献的证据质量,达成推荐级别。经反复讨论和修改,首次制订了“中国中枢神经系统恶性胶质瘤诊断和治疗共识”(以下简称“共识”),供广大临床医务工作者参考和应用,希望有助规范和推动我国CNS恶性胶质瘤的诊治,更好地为广大病人及其家属服务。胶质瘤为起源于神经胶质细胞的肿瘤,是最常见的原发性颅内肿瘤。 WHO中枢神经系统肿瘤分类中将胶质瘤分为Ⅰ-Ⅳ级,Ⅲ、Ⅳ级为恶性胶质瘤,占所有胶质瘤的77.5%。近30年,原发性恶性脑肿瘤发生率逐年递增,年增长率约为1.2%,老年人群尤为明显。一般认为恶性胶质瘤的发生是机体内部遗传因素和外部环境因素相互作用的结果,具体发病机制尚不明了。胶质瘤临床表现主要包括颅内压增高及神经功能缺失的症状及体征。目前,恶性胶质瘤主要依靠MRI和CT影像学诊断,通过肿瘤切除术或活检术明确病理学诊断,分子、基因水平的病理学诊断研究正逐步深入。对恶性胶质瘤的治疗采取以手术治疗为主,结合放疗、化疗等疗法的综合治疗。手术主张安全、最大范围地切除肿瘤,而功能MRI、术中MRI、神经导航等技术的应用促进了该目的的实现。放疗可杀灭或抑制残余肿瘤细胞,延长生存。替莫唑胺(TMZ)同步放疗联合辅助化疗已成为新诊断胶质母细胞瘤(GBM)的标准方案。2. 恶性胶质瘤的诊断恶性胶质瘤的临床表现没有特异性,以神经系统功能缺失伴颅内压增高症状为主。影像学诊断方面强烈推荐MRI平扫加增强为主,CT为辅。MRI的表现是:平扫通常为混杂信号病灶,T1WI为等信号或低信号,T2WI为不均匀高信号,伴有出血、坏死或囊变,瘤周水肿及占位效应明显。肿瘤常沿白质纤维束扩散。增强时呈结节状或不规则环状强化。CT平扫示密度不均匀,常见出血、坏死或囊变,瘤周水肿及占位效应均较明显。增强为显著不均匀强化,不规则或环状强化。推荐MRI特殊功能检查(MRS、PWI、DWI、DTI)、PET和SPECT检查等,主用于鉴别诊断、术前评估和疗效评价。3.恶性胶质瘤的病理诊断及生物学标记强烈推荐严格按照2007年《WHO中枢神经系统肿瘤分类》,对恶性胶质瘤进行病理诊断和分级。为配合胶质瘤病人的治疗、疗效观察及判断预后,强烈推荐各级医院根据实际情况,开展选择性的分子生物学标记,如GFAP, Olig2, EMA, p53, MGMT, Ki67和1p/19q LOH。4.恶性胶质瘤的手术治疗强烈推荐对于局限于脑叶的原发性高级别(WHO III~IV级)或低级别(WHO II级)胶质瘤应争取最大范围安全切除肿瘤。基于胶质瘤膨胀性浸润性的生长方式及血供特点,推荐采用显微神经外科技术,以脑沟、脑回为边界,沿肿瘤边缘白质纤维束走向作解剖性切除,以最小程度的组织和神经功能损伤获得最大程度的肿瘤切除,并明确组织病理学诊断。对于:(1)优势半球弥漫浸润性生长、(2)病灶侵及双侧半球、(3)老年患者(>65岁)、(4)术前神经功能状况较差(KPS<70)、(5)脑内深部或脑干部位的恶性脑胶质瘤、⑹ 脑胶质瘤病,推荐酌情采用肿瘤部分切除术、开颅活检术或立体定向(或导航下)穿刺活检。肿瘤部分切除术具有比单纯活检术更高的生存优势。活检主要适用于邻近功能区皮质或位置深在而临床无法手术切除的病灶。活检主要包括立体定向(或导航下)活检和开颅手术活检。立体定向(或导航下)活检适用于位置更加深在的病灶,而开颅活检适用于位置浅表或接近功能区皮质的病灶。 强烈推荐于手术后早期(<72小时)复查MRI,以手术前和手术后影像学检查的容积定量分析为标准,评估胶质瘤切除范围。高级别胶质瘤的MRI的T1WI增强扫描是目前公认的影像学诊断“金标准”;低级别胶质瘤宜采用MRI的T2WI或FAIR序列影像。在不具备复查MRI条件的单位,推荐于术后早期(<72小时)复查CT。为了实现最大范围安全切除恶性脑胶质瘤,推荐采用以下影像导引外科新技术如常规神经导航、功能神经导航(functional neuronavigation)、术中神经电生理监测技术(例如,皮层功能定位和皮层下刺激神经传导束定位)、术中MRI实时影像(intraoperative imaging)神经导航。可推荐:荧光引导显微手术、术中B超影像实时定位。5.恶性胶质瘤(WHO III-IV)放射治疗原则建议术后2-4周左右尽快开始放疗。强烈推荐常规分割(1.8-2.0Gy/次,5次/周)6-10MV X线的外照射,标准放疗总剂量为54-60Gy,分割30-33次(I级证据)。在一定的剂量范围内,增加肿瘤照射剂量并不能获益。近距离放疗增加剂量以及分割方式的改变对生存率无影响。分割立体定向放射疗法(FSRT)/立体定向放射外科(SRS)适用于常规外照射后的推量或作为复发肿瘤治疗的选择方式之一,此治疗对体积较小的肿瘤有优势。不推荐X-刀或Y-刀作为恶性胶质瘤术后首选的治疗方式。虽然GBM可能广泛播散,但仍推荐局部放疗。目前的影像技术无法确定肿瘤的真正边界,因此在确定放疗靶区时应综合所有影像学上显示的肿瘤及相关水肿,并外扩足够的边界。推荐对于强化的高级别胶质瘤,最初的临床靶体积(CTV)为强化的肿瘤加上FLAIR像或T2像上异常显示并外扩约2cm,缩野推量时,仅包括强化肿瘤外2cm。推荐应用3D计划设计的多野照射。与常规放疗相比,三维适形放疗可更好地保护正常脑组织。对于GBM强烈推荐TMZ 75 mg/m2化疗并同步放疗,接6个周期的TMZ辅助化疗。 在放疗中和放疗后应用替莫唑胺,显著延长了病人的生存,这一治疗在O6-甲基鸟嘌呤-DNA甲基转移酶(MGMT)基因启动子甲基化的病人中最明显(参见化疗章节)。I/II期试验初步显示了TMZ在治疗 WHO III 级肿瘤的作用,但还没有针对Ⅲ级肿瘤的相关试验。因此,可推荐TMZ 75 mg/m2化疗并同步放疗。假性进展指放疗或放化疗后,影像学出现酷似肿瘤进展的表现,它与与放疗剂量有关,与肿瘤进展无关。多见于治疗结束后2个月内,多无临床症状和体征,和传统概念的放射性坏死相比,即使不予治疗也可缩小或保持稳定。MGMT低表达者假性进展发生率明显高于高表达者。TMZ同步放/化疗后假性进展的发生率增加,出现假性进展的时间提前。如仅影像学表现,患者无临床症状,可随访观察;当短期内增强病灶增大,经影像学检查(MRS, PET/CT)无法鉴别时,应活检或手术。6.新诊断恶性胶质瘤的化疗 对于新诊断的GBM, 强烈推荐TMZ同步放疗联合辅助化疗方案:放疗的整个疗程应同步化疗,口服TMZ 75 mg/m2,疗程42天。放疗结束后4周,辅助TMZ治疗,150mg/m2,连续用药5天,28天为一个疗程 ,若耐受良好,则在以后化疗疗程中增量至200mg/m2,推荐辅助TMZ化疗6个疗程。TMZ用于恶性胶质瘤病人有以下益处:1)延长生存时间;2)延长肿瘤无进展期;3)对生活质量没有明显的负面影响;4)较低的早期不良事件发生率。无条件用TMZ的GBM者对GBM建议ACNU(或其它烷化类药物BCNU、CCNU)90mg/m2,D1,VM-26 60mg/m2,D1-3,4-6周1周期,4-6个疗程。新诊断的间变性胶质瘤(WHO Ⅲ级):推荐放疗联合替莫唑胺(同多形性胶质母细胞瘤)或应用亚硝脲类化疗药物:(1)PCV方案(洛莫司汀+甲基苄肼+长春新碱):8周为一个疗程,不超过6个疗程。口服洛莫司汀(CCNU)110mg/ m2,D1;每日口服甲基苄肼(PCB)60mg/m2,D8-21;静脉给药长春新碱(VCR)1.4mg/ m2(最大剂量为2mg),D8,D29。(2)ACNU方案(见上)。局部瘤腔植入的含卡莫司汀(BCNU)的生物可降解聚合物(Gliadel Wafer, 美国Guilford公司)在一项随机对照的III期临床试验中显示出对新诊断的恶性胶质瘤病人的生存益处(Ⅰ级证据)。由于该移植片尚未在我国上市,故还没有其对国人安全性和有效性的报道。由于尚无大规模的随机对照研究的结果支持,并且费用高,技术要求也高,目前不建议推广动脉化疗和辅助自体骨髓移植。推荐有条件的单位尽快开展MGMT蛋白的免疫组化检测或MGMT基因启动子的甲基化PCR检查,以便更好地开展恶性胶质瘤的个体化化疗。间变性少突胶质细胞瘤和间变性少突-星形细胞瘤患者,若有染色体1p 19q的联合缺失,不但对化疗敏感,而且生存期也明显延长。以贝伐单抗为代表的靶向治疗目前正在研究中。7.恶性胶质瘤的随访和复发的治疗强烈推荐以MRI检查为主的定期随访。放疗后2-6周行MRI检查,以后2-3年内每2-4个月MRI检查一次,三年后每3-6个月一次。对复发患者,应该根据复发部位、肿瘤大小、颅内压情况以及患者基本情况综合考虑。局部复发推荐再手术;不适合再手术的患者,可推荐放射治疗和/或化疗;如果以前接受过放疗不适合再放疗者,推荐化疗;化疗失败者,推荐改变化疗方案和/或包括分子靶向治疗的研究性治疗。弥漫或多灶复发者,推荐化疗和/或包括分子靶向治疗的研究性治疗。晚期患者,推荐给予对症支持治疗。
周朋 副主任医师 山东省千佛山医院 神经外科2049人已读 - 医学科普 高血压脑出血的微创治疗的福音-----神经内镜治疗
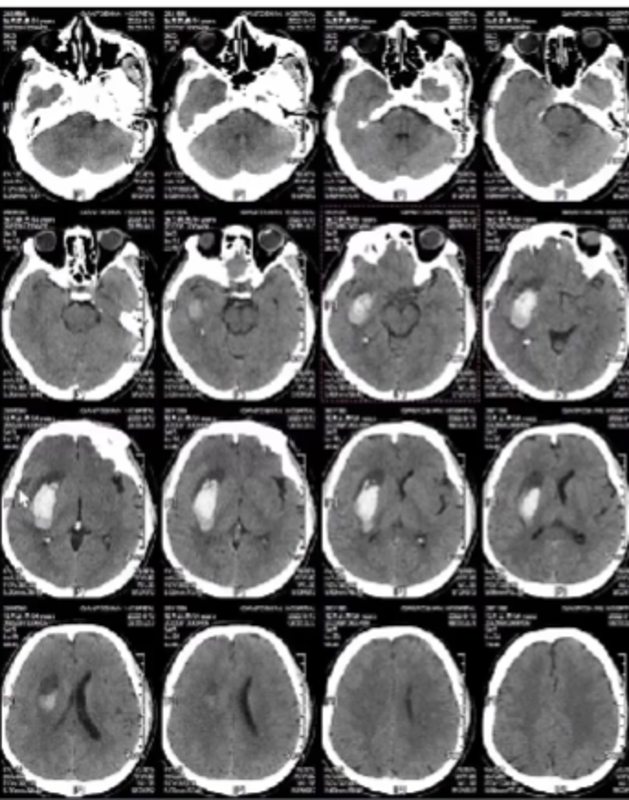
高血压性脑出血是高血压病的严重并发症之一,其中中国的发病率占所有脑卒中的19%-48%[1],高血压性脑出血病死率和致残率极高,对其进行积极干预非常重要。神经内镜是近年治疗高血压性脑出血的常用手段,具有创伤小、疗效好的优势,但对于此类手术的具体术中操作及如何进行围手术期精细化管理,则尚有可探讨之处。近日,在“急重三人行:重在有术”活动中,山东大学齐鲁医院黄齐兵主任、山东第一医科大学第一附属医院汪建军教授、山东第一医科大学第一附属医院周朋博士齐聚云端,围绕神经内镜治疗高血压性脑出血的具体策略以及围术期管理的注意事项展开精彩讨论。本期为您整理相关精华内容,希望对读者的临床实践有所裨益。从病例看神经内镜手术治疗脑出血的具体策略周朋博士分享了数例神经内镜治疗脑出血病例的体会。病例1因“突发左侧肢体活动障碍12小时”入院,有高血压病史,头颅CT提示右侧基底节区团块状高密度影(图1)。与家属沟通后导航下设计手术入路,中线旁开3厘米,发际内弧形切口,选择路径上血肿最远点退后5毫米作用为靶点,切开头皮及硬膜后,导航引导经皮层穿刺靶点,内镜下清除血肿。术后CT提示血肿清除满意(图2)。图1患者手术前头颅CT图2患者术后CT病例2因“突发意识不清,右侧肢体活动障碍2小时”入院,头颅CT提示左侧基底节区团块状高密度影,选择神经导航引导经颞入路内镜血肿清除,同样清除血肿满意,患者预后好(图3)。图3患者术前及术后头颅CT病例3为37岁年轻女性,因“突发意识不清6小时”入院,头颅CT提示脑干及四脑室内高密度影(图4),靶点定位为血肿左侧,行导航+微型神外手术机器人系统血肿钻孔引流,术后5天头颅CT提示血肿吸收良好(图5)。图4患者术前头颅CT图5患者术后5天头颅CT周朋博士总结手术经验指出,微创精准脑出血手术需要选择合适病例及合适手术时机。手术技巧包括准确的定位、应用多种影像引导技术、术前阅片仔细等。术中应行个体化穿刺,力求精准穿刺(血肿中心部),建议初学者采用脑回入路,熟悉后采用脑沟入路。穿刺时需要避免多次穿刺,调整穿刺方向与地面垂直,可减少误差。术中应采用有序的血肿清除方向及顺序,先清除底部再摆动套筒,避免机械性损伤,选用合适的通道(直径越细、损伤越小),还应避免盲目电灼止血,对活动性出血必须精准可靠有效止血。尼卡地平助力围术期精细化管理改善脑出血患者预后不仅需要仔细的手术操作,也离不开精细的围术期管理。周朋博士分享的《2022年美国心脏学会(AHA)/美国卒中学会(ASA)自发性脑出血患者管理指南》[2]即推荐指出,脑出血围术期管理中,降压关键是早期、快速、强化、平稳,6小时内将收缩压降至140mmHg,且急性期保持平稳控压。黄齐兵主任分析神经内镜的术中治疗策略时指出,神经导航在此类手术中具有重要的作用,通过直接穿刺将穿刺导管置于血肿最正中位置,有助于减少术中止血需求,同时降低术后再出血风险。高血压脑出血围术期管理除了强调术中的操作外,术前急诊室管理、术后血压管理缺一不可,例如急诊室中我们需要第一时间关注患者气管插管和胃肠减压的需求,以降低误吸带来的各种风险。术后血压波动则会带来再出血等诸多问题,只有整体系统管理、平稳控制血压才能精细化管理好患者。汪建军主任认为,近年随着研究进展,临床医生已认识到,精准+微创的手术治疗理念给患者带来的改善作用。神经导航技术的使用是大势所趋。就目前临床经验而言,内镜手术感染率并不高于微创穿刺,可能与微创穿刺手术时间较长、且存在异物长期引流有关,因此不需过度忧虑神经内镜手术的感染风险。除了手术以外,院前、术前、术中术后管理同样值得重视。既往围术期降压多采用硝普钠,但其需要避光使用,过度的降压作用往往还会给患者带来肾功能损伤等损害。随着围术期管理理念不断更新,临床更推崇使用可以快速降压、容易滴定剂量的降压药物,尼卡地平即满足了此要求。研究提示,尼卡地平可快速起效,达峰时间短,小剂量即可快速降压[3]。且药物作用平稳,在治疗开始后的3小时内就能够帮助患者实现更平稳的血压控制[4]。总结神经内镜与显微神经外科技术、神经导航、术中超声等技术相结合,使得神经内镜手术充分发挥了定位准、创伤小、疗效好的优势。静脉降压药物尼卡地平具有迅速平稳降压的优势,有助于精细化管理围术期患者血压,是神经内镜治疗后的脑出血患者的围术期降压药物优选。
 周朋 副主任医师 山东省千佛山医院 神经外科57人已读
周朋 副主任医师 山东省千佛山医院 神经外科57人已读 - 医学科普 得了高血压,要不要吃阿司匹林?
很多高血压患者都在用阿司匹林,这个药呢,不是降压药,但是在预防心梗方面挺重要。大家对阿司匹林的误解也很多,有些人觉得高血压就得吃阿司匹林,不该吃的乱吃;有些人又担心阿司匹林会吃出来胃出血,该吃不敢吃。 阿司匹林在心血管疾病的治疗和控制地位非常重要,但并不意味着所有的高血压患者都要吃阿司匹林。 什么人需要吃阿司匹林? 根据 2010 年《中国高血压防治指南》,有以下这些情况的高血压患者,推荐每天应用 100 mg 阿司匹林: 有心绞痛、心肌梗死病史; 有脑血栓形成、短暂性脑缺血发作病史; 有增加血栓风险的血管炎病史(比如闭塞性周围动脉粥样硬化)。 吃阿司匹林胃肠道反应大的人,也可以用氯吡格雷(75 mg/d)代替。 没有上述情况的高血压患者,如果有以下情况,也推荐服用小剂量阿司匹林(每天 75~100 mg): 有高血压导致的器官损害,比如,左心室肥厚,颈动脉斑块,肾功能异常等; 有 2 型糖尿病。 如果经医生评估,10 年内发生缺血性心血管疾病的风险> 10 %,也可以服用小剂量阿司匹林进行预防。 服用阿司匹林的注意事项 可能大家也了解阿司匹林有一定的出血风险,所以需要长期服用阿司匹林的患者有以下注意事项: 1. 在医生指导下服用阿司匹林,一般医生会在血压控制比较稳定(< 150 / 90 mmHg)后才让患者服用阿司匹林。如果在血压没有控制好的情况下擅自服用,可能增加脑出血的风险。 2. 因为长期应用阿司匹林可能增加消化道出血的风险,所以应用前最好进行消化系统的检查,排除危险因素,采取相应的措施。比如有幽门螺杆菌感染的患者,在用阿司匹林前,最好先根治幽门螺杆菌。 3. 有活动性胃溃疡、严重肝病、出血性疾病的患者,禁用阿司匹林。 希望大家能够合理用药,如果医生没有推荐,不要擅自使用。如果医生告知你需要用阿司匹林,也不要因为担心出血的风险而不敢用。
周朋 副主任医师 山东省千佛山医院 神经外科2888人已读 - 学术前沿 高血压最新指南
时隔不到一年,加拿大高血压教育计划(CHEP)再次更新高血压防治与评估指南。这次更新后的指南有5点值得关注: 1. 血压测量工具首选全自动血压计; 2.检测血脂参数不再强调空腹采血; 3. 对于不具有高血钾危险因素的患者,增加饮食中钾摄入有助于降低血压; 4. 伴稳定性心绞痛的高血压患者(无心衰、心梗或冠脉旁路手术病史者),b受体阻滞剂或钙通道阻滞剂均可作为初始治疗选择; 5. 新指南中最值得关注的是将不久前结束的SPRINT研究结论引入该指南,推荐将≤120 mmHg作为部分高危患者(如年龄≥75岁者)的降压目标值。 一、血压测量与高血压诊断 在血压测量与高血压诊断方面,CHEP新指南继续将诊室血压≥140/90 mmHg作为高血压的诊断界值,130-139/85-89 mmHg为正常高值;诊室血压测量工具首选全自动血压测量计,血压≥135/85 mmHg则视为增高;应用动态血压监测时,若清醒时段血压≥135/85 mmHg、或24小时平均血压≥130/80 mmHg,可诊断为高血压;患者家庭自测血压≥135/85 mmHg可诊断高血压;首次就诊时若患者表现为高血压急诊或亚急症即可诊断为高血压;其他患者需要重复测量方能确立诊断;但初次就诊时血压≥180/110 mmHg可直接诊断高血压。 初诊高血压患者常规检测的项目包括:尿液分析、血液生化检查(血钾、血钠、肌酐等)、空腹血糖和(或)糖化血红蛋白、血脂检测(包括总胆固醇、LDL-C、HDL-C、非HDL-C、甘油三酯,不再要求空腹血样检测)、标准12导联心电图。尿白蛋白排泄量也应作为患者的检测项目之一。 若患者具备以下≥2项因素时,需考虑肾血管性高血压:年龄>55岁或<30岁的患者突发高血压或高血压恶化;腹部血管杂音;应用≥3种药物仍不能控制血压;应用ACEI或ARB治疗后血肌酐升高≥30%;并存其他动脉粥样硬化性血管疾病(特别是吸烟或有血脂异常者);血压骤升导致反复发作的肺水肿。 下列患者需要筛查原发性醛固酮增多症:高血压伴无明确原因的低血钾(
周朋 副主任医师 山东省千佛山医院 神经外科6810人已读 - 学术前沿 颅内动脉瘤血管内介入治疗中国专家共识
颅内动脉瘤是颅内动脉血管由于先天异常或后天损伤等因素导致局部的血管壁损害,在血流动力学负荷和其他因素作用下,逐渐扩张形成的异常膨出。人群中颅内动脉瘤的患病率约为2%~7%,任何年龄均可发病,40~60岁常见,但其发生率存在明显的地域及种族差异。一项经动脉脑血管造影研究提示亚洲人群中颅内动脉瘤患病率约为2.5%~3.0%。颅内动脉瘤一旦破裂出血,致死致残率极高,其中10%~15%的患者来不及就医直接猝死,首次出血病死率高达35%,再次出血病死率则达60%~80%,幸存者亦多有残疾。 自ISAT研究结果公布后,近10余年来颅内动脉瘤血管内介入治疗发展迅猛,随着修饰弹簧圈、辅助球囊、颅内动脉瘤治疗专用支架以及血流导向装置等的出现,血管内介入治疗颅内动脉瘤的疗效更为确切。介入治疗已成为部分颅内动脉瘤首选的治疗方法。为了规范颅内动脉瘤的血管内介入治疗,中华医学会神经外科学分会神经介入学组组织专家经数次讨论,制定了《颅内动脉瘤血管内介入治疗中国专家共识》(以下简称“共识”),旨在提高各级医师对颅内动脉瘤血管内介入治疗的认识,使之更系统、更规范、更安全、更有效。 一、颅内动脉瘤的诊断 未破裂动脉瘤大多数缺乏特异性临床症状,多为偶然发现,少数因头痛、眼睑下垂等症状被发现。因此无症状的未破裂动脉瘤,诊断较为困难。是否在人群中进行颅内动脉瘤的筛查存在争议。但对于高危患者进行无创筛查亦是合理的。 推荐意见: (1)对于有家族史和(或)患有与动脉瘤发生相关遗传性疾病的人群,特别是女性、年龄>30岁、重度吸烟或伴有高血压病的患者建议进行颅内动脉瘤筛查; (2)怀疑aSAH的患者应行头颅CT平扫检查,如不能诊断则须行腰椎穿刺检查; (3)对于CT不能确诊的aSAH患者行核磁共振检查(液体衰减反转恢复序列、质子密度成像、弥散加权成像或梯度回波序列)是合理的,如果核磁共振检查阴性,仍需进一步行腰椎穿刺检查; (4)CTA可被用于aSAH病因学诊断;如果CTA检查阴性,推荐进行DSA检查; (5)全脑DSA是诊断颅内动脉瘤的金标准。旋转造影和三维重建(3D-DSA)技术可提高动脉瘤检出率,并且可以准确显示动脉瘤形态以及与邻近血管的关系; (6)首次DSA检查阴性的SAH患者,推荐2~4周后再次行DSA检查。 二、颅内动脉瘤血管内介入治疗适应证 破裂出血的颅内动脉瘤患者病死率高达26%~51%,发生aSAH患者的生存率可能与年龄、性别和人种密切相关。动脉瘤一旦发生破裂出血,容易发生再次破裂出血(24 h内再出血发生率为4%~13.6%),发生再出血的患者中80%以上的患者预后不良,并且再出血发生越早其预后越差。因此,动脉瘤一旦破裂应紧急手术治疗。 推荐意见: (1)发生破裂出血的动脉瘤均应尽早进行病因治疗,以降低动脉瘤再次破裂出血风险; (2)症状性未破裂动脉瘤也应尽早治疗,以避免症状继续加重,危及生命; (3)对于直径≥5 mm的无症状未破裂动脉瘤建议进行干预。如动脉瘤直径10年,伴有aSAH病史,有家族史或需长期口服抗凝、抗血小板药物的动脉瘤患者推荐积极干预; (4)未治疗的未破裂动脉瘤患者,建议其动态随访,随访过程中发现动脉瘤进行性增大、形态改变,建议进行干预; (5)由于患有未破裂动脉瘤导致患者心理障碍,严重影响工作生活的可适当放宽干预指征,采取更加积极的治疗策略; (6)动脉瘤的治疗方案(夹闭或介入),应依据患者特点和动脉瘤的特点等多因素考虑后制定; (7)对于从技术上既可以开颅夹闭又可行介入治疗的动脉瘤患者,推荐行血管内介入治疗; (8)后循环动脉瘤患者、高龄患者(>70岁)、自发性aSAH评分较低(WFNS分级Ⅴ/Ⅵ)患者以及处于脑血管痉挛期患者应优先考虑介入治疗。 三、颅内动脉瘤血管内介入治疗策略 医学发展的微创化甚至是无创化治疗的趋势,推动了血管内治疗已成为当前颅内动脉瘤的重要治疗手段,血管内治疗颅内动脉瘤也相继经过了球囊、微弹簧圈、液态栓塞材料、支架以至血流导向装置的历程,治疗理念发展的目标在于为动脉瘤血管内治疗提供最简单、最安全、最经济的方法。遗憾的是,颅内动脉瘤的复杂性及个体差异极大。因此,制定个体化的颅内动脉瘤治疗方案是推动神经介入发展的一个最为重要原因。 推荐意见: (1)对于颅内动脉瘤的血管内介入治疗,推荐在全身麻醉下进行; (2)血管内介入治疗颅内动脉瘤建议术中应用肝素抗凝,如采用支架治疗动脉瘤,推荐行抗血小板药物准备; (3)颅内动脉瘤的介入治疗应以保持载瘤动脉通畅的重建性治疗为首选,闭塞载瘤动脉的非重建性治疗作为部分难治性动脉瘤的可选方法; (4)颅内动脉瘤首选单纯弹簧圈栓塞治疗,如有困难可合理选择微导管(导丝)辅助、多导管技术、球囊辅助或支架辅助等多种技术; (5)对破裂宽颈动脉瘤的血管内介入治疗,可采用支架辅助栓塞技术,但应考虑到可能增加并发症发生率; (6)支架辅助栓塞技术可能促进动脉瘤的愈合,降低动脉瘤的复发率; (7)颅内动脉瘤的介入治疗应尽可能致密栓塞,水凝胶弹簧圈的应用可以显著降低动脉瘤复发率; (8)动脉瘤明显复发应积极行再次干预,复发动脉瘤的再次血管内介入治疗相对安全。 四、aSAH后脑血管痉挛的血管内介入治疗 脑血管痉挛(CVS)是aSAH致死、致残的重要原因,严重影响此类患者的预后。aSAH后造影显示,30%~70%的患者会出现脑血管痉挛,通常在出血后3 d开始出现,2~4周逐渐消失。虽经全力救治,仍有15%~20%的患者死于脑血管痉挛。因此,CVS的早期诊断与治疗非常关键。 推荐意见: (1)aSAH后脑血管痉挛发生率高,处理破裂动脉瘤后,引流蛛网膜下腔积血并启动尼莫地平治疗是预防aSAH后脑血管痉挛的有效手段; (2)症状性脑血管痉挛经药物治疗无效或脑血管痉挛期aSAH患者突然出现神经功能缺损,推荐行脑血管造影检查和(或)血管内介入治疗,包括球囊成形术和(或)动脉内抗痉挛药物灌注术。 五、血管内介入治疗后影像学随访策略 颅内动脉瘤血管内介入治疗后长期稳定性如何是目前亟待明确和解决的重大问题与挑战。颅内动脉瘤患者由于遗传、血流动力学、吸烟、酗酒以及高血压病等危险因素,新发及多发动脉瘤的可能性大。因此,对于颅内动脉瘤介入栓塞后的患者应终身随访,以防动脉瘤复发和新生动脉瘤。 推荐意见: (1)动脉瘤介入治疗后的随访应遵循规范化和个体化,推荐在治疗后6~12个月行DSA影像学随访; (2)动脉瘤存在远期复发和新生等问题,接受介入治疗的颅内动脉瘤患者推荐行长期影像学随访; (3)CE-MRA或高场强的TOF-MRA(≥3.0T)可以取得与DSA类似的影像学结果,建议作为动脉瘤介入治疗后的无创随访手段,如检查结果不确切,建议进一步行DSA检查。 六、血管内介入治疗颅内动脉瘤的资质认证 随着我国神经介入事业的飞速发展,越来越多的人员开始从事神经血管介入工作。但是各机构在硬件条件、技术水平上存在显著差异,治疗效果也有明显区别。血管内治疗例数多的机构其患者病死率较低,将患者转入相应医学中心可以改善患者的预后。 推荐意见: (1)严格执行国家卫生计划生育委员会制定的《神经血管介入诊疗技术管理规范》,落实神经介入机构和医师的考核和资格认证制度,对拟从事神经介入的医师进行严格培训,使其能胜任颅内动脉瘤的血管内介入治疗; (2)有资质的神经介入医师每年至少参加一次相关的继续教育培训,以保证知识更新; (3)病例数较少的医院(动脉瘤介入栓塞病例<10例/年)接收患者后建议由经验丰富的医师或中心指导行血管内介入治疗,或尽早将患者转移到综合实力较强的、经验丰富的大型医学中心(动脉瘤介入栓塞病例>35例/年)。 七、小结 颅内动脉瘤的血管内介入治疗非常复杂,材料和技术发展迅速,治疗理念不断更新。本次撰写的共识是对该领域的阶段性认识,因此需要定期更新。临床医生在处理患者时应参考本共识,以使颅内动脉瘤的血管内介入治疗更合理规范,患者更多获益。本共识仅代表参与编写及讨论专家的观点,不具备法律效力,解释权在本共识编写委员会。
周朋 副主任医师 山东省千佛山医院 神经外科3062人已读 - 就诊指南 微小动脉瘤治不治?
对颅内未破裂动脉瘤进行治疗,虽然可避免出血造成的灾难性后果,但事实上,绝大部分颅内动脉瘤患者终身都不会破裂。同时,无论开颅手术还是血管内介入治疗,都并非绝对安全。那么,如何准确预测动脉瘤的风险就成为关键。 被手术患者越来越多 近年来,由于神经影像学的进步和普及,越来越多的无症状或症状轻微的颅内未破裂动脉瘤(UIAS)被检出,对其自然风险的评价和干预措施安全性的评级,引起了医师和患者的高度重视。预防性治疗虽然可避免动脉瘤破裂出血造成的灾难性后果,但绝大部分患者的UIAS终身不会破裂。同时,无论是开颅手术还是血管内介入治疗动脉瘤,均并非绝对安全。因此,若对所有颅内未破裂动脉瘤均进行积极处理,则是一种过度医疗行为。这会使许多患者承担不必要的医疗风险。 对于评估和治疗UIAS的关键问题是: 一、如何准确预测某一特定病例是否存在动脉瘤破裂的风险。 二、能否保证治疗措施的安全性。 目前在UIAS破裂风险的预测指标中,最重要的是动脉瘤的大小。 所有的相关性研究均认为,越小的UIAS破裂的风险越低,而这部分微小动脉瘤的治疗难度和风险相对较高。所以对于颅内未破裂微小动脉瘤(mUIAS)治疗的风险和获益需要着重讨论。 随诊重点看大小变化 目前关于mUIAS的概念尚未统一。大多数文献将其定义为最大直径≤3mm的颅内动脉瘤。有文献报道,至少有>2%的成年人患有UIAS,但尚缺乏mUIAS患病率的确切数据。一项基于尸检和人群研究的荟萃分析显示,UIAS中最大直径
周朋 副主任医师 山东省千佛山医院 神经外科2.1万人已读 - 就诊指南 神经指南:中国脑积水规范化治疗专家共识
一、脑积水概念和分类颅内蛛网膜下腔或脑室内的脑脊液异常积聚,使其一部分或全部异常扩大称为脑积水。单纯脑室扩大者称为脑内积水,单纯颅内蛛网膜下腔扩大者称为脑外积水。脑积水不是一种单一的疾病改变,而是诸多病理原因引起的脑脊液循环障碍。脑积水是由脑脊液循环障碍(通道阻塞),脑脊液吸收障碍,脑脊液分泌过多,脑实质萎缩等原因造成。临床中最常见的是梗阻性病因,如脑室系统不同部位(室间孔、导水管、正中孔)的阻塞、脑室系统相邻部位的占位病变压迫和中枢神经系统先天畸形。按流体动力学分为交通性和梗阻性脑积水;按时限进展分为先天性和后天性脑积水,急性和慢性脑积水,进行性和静止性脑积水;按影像学分为单纯性、继发性和代偿性脑积水;按病理生理分为高压力性、正常压力性、脑萎缩性脑积水;按年龄分为儿童和成人脑积水。 二、脑积水的诊断1.临床症状和体征:头颅及前囟增大(婴幼儿),颅内压增高的临床症状和体征(头痛、恶心、呕吐、视乳头水肿),脑组织受压引起进行性脑功能障碍表现(智能障碍、步行障碍、尿失禁)。 2.脑室穿刺测压:高于正常值(小儿40-110mm H2O,成人80-180mm H2O)。成人正常压力脑积水的脑室内压力在正常值范围内。临床常以患者侧卧位腰穿测蛛网膜下腔压力代表脑室内压力,梗阻性脑积水严禁做腰蛛网膜下腔穿刺测压。 3.头颅影像学检查: (1)梗阻性脑积水:头颅X线片为颅骨内板可见指压痕(慢性病例)。CT见脑室扩大,双额角径或颅内径(Evans指数)>0.33是诊断脑积水的标志性指标;额角变锐<100°;颞角宽度>3mm;脑室边缘模糊,室旁低密度晕环;基底池,脑沟受压/消失。MRI为矢状位T1可显示导水管梗阻,幕上脑室扩大;胼胝体变薄,向上拉伸;穹窿、大脑内静脉向下移位、第三脑室底疝入扩大的蝶鞍。T2显示脑脊液样的指纹状高信号向脑室外延伸到脑组织,间质水肿在脑室角周围明显;脑室内脑脊液形成湍流;导水管流空消失。增强T1显示软脑膜血管淤滞,类似于脑膜炎改变。心电门控相位对比MRI电影为在导水管中无明显脑脊液流动。推荐影像学检查:3DCISS序列可减少脑脊液流动伪影,更好显示脑室轮廓及透明隔,心电门控相位对比MRI电影。 (2)正常压力脑积水:CT见脑室扩大伴额角变钝。MRI有脑室扩大;额角颞角扩大不伴海马萎缩;基底池、外侧裂扩大,脑沟正常;部分病例在质子密度像及常规自旋回波序列可消失导水管流空现象;脑脊液电影可消失脑脊液流速增加。推荐影像学检查是心电门控相位对比MRI电影。 (3)蛛网膜下腔增宽(脑外积水):CT见双侧额部(前部半球间裂)蛛网膜下腔增宽≥5mm;脑池增宽;轻度脑室扩大;增强CT显示静脉穿过蛛网膜下腔。MRI有蛛网膜下腔增宽伴穿行血管;在所有序列,蛛网膜下腔内为脑脊液信号;推荐影像学检查:多普勒超声显示静脉穿行蛛网膜下腔;MRI排除慢性硬膜下积液;增强CT或MRI排除基础病因。 4.其他特殊检查:神经电生理检查,MRI的脑脊液动力学检查等。 三、脑积水的治疗目的为预防或治疗因颅内压增高或脑组织结构的病理改变引起的神经功能损伤,原则是解除病因和解决脑室扩大兼顾,综合考虑患者的个体因素,采取个体化治疗。 1.手术适应证:(1)新生儿和儿童脑积水为脑室扩大并有颅内压增高、脑功能损害的临床表现。(2)无症状且脑室大小稳定不再增大的儿童脑积水,要考虑儿童认知功能有无损害,积极手术治疗对改善儿童神经功能有明确益处。(3)颅内出血后和脑脊液感染继发脑积水,在血性脑脊液吸收后,有脑脊液感染者采用静脉(脑室内或鞘内用药要根据中国药典和药品说明书)用抗生素,待脑脊液感染控制后(接近或达到正常脑脊液指标),可行分流术。(4)肿瘤伴发的脑积水,对伴有脑积水的第三和第四脑室内肿瘤,如估计手术不能全部切除肿瘤,或不能解除梗阻因素,做术前脑室-腹腔分流术有助于肿瘤切除术后安全渡过围手术危险期。(5)伴有神经功能损害的正压性脑积水。(6)脑外积水的处理原则是狭义的脑外积水见于1岁以内的婴幼儿,原因不明,表现为双额蛛网膜下腔增宽,前囟张力正常或轻度饱满。如无颅内压增高的表现,绝大多数患儿在l岁半以后积液消失,无需特殊治疗。 2.手术禁忌证:(1)颅内出血急性期。(2)颅内感染,有脑脊液感染或感染病灶。(3)头皮、颈部、胸部、腹部皮肤有感染。(4)腹腔内有感染。 3.手术方式的选择原则:(1)V-P分流术适合于大多数类型的脑积水。(2)L-P分流术适合于交通性脑积水和正压性脑积水,有小脑扁桃体下疝的患者为禁忌证。(3)脑室-心房(V-A)分流术常用于不适合做V-P分流术者,如腹腔内感染,有严重呼吸、循环系统疾病者为禁忌证。(4)第三脑室底造瘘术适合于非交通性和部分交通性脑积水患者。对婴幼儿(尤其是<l岁的婴儿)和严重脑室扩大的患者,由于成功率低和极易引起严重的硬膜下积液,选择此类手术要谨慎。因脑室内条件所限(如出血、感染、隔膜等)无法放入分流管的患者。(5)其他分流术方式包括透明隔造瘘术,托氏分流(肿瘤切除后做脑室-枕大池分流)。 四、分流术后的常见并发症及处理措施在神经外科疾病的治疗中,分流手术的并发症发生率最高,主要有分流感染(包括颅内或腹腔内感染,切口或皮下感染)、分流管阻塞、分流管断裂、颅内或腹腔内分流管异位、脑脊液过度引流(引起硬膜下血肿或积液,裂隙脑室综合征)、脑脊液引流不足、颅内出血、癫痫等。 (1)感染:术后常见的有颅内感染、切口感染、腹腔内感染、分流管皮下通道感染等。一旦有感染,应先拔出分流管,再进行抗感染治疗,可行脑室外引流或腰穿持续引流,在有效控制感染后,重新做分流术。 (2)过度引流:可表现为裂隙脑室综合征、硬膜下积液或硬膜下血肿。在治疗积液或血肿的同时,应更换高一级压力的分流泵(压力固定型分流管)或调高压力(可调压型分流管)。 (3)引流不足:患者临床表现无明显改善,脑室无缩小。首先检测分流系统是否通畅,如果发现有阻塞,应更换分流管。如果分流管通畅,应调低设定压力(可调压型分流管)或更换低一级压力的分流泵(压力固定型分流管)。长期卧床可致引流不足,应鼓励患者半坐位或站立活动。 (4)分流管阻塞:常见阻塞部位和原因为颅内分流管位置不佳(如靠近脉络丛、紧贴脑室壁)、分流泵内红细胞或脑组织积聚、腹腔内大网膜包绕分流管等。判定分流管阻塞的一般方法是按压头皮下分流泵储液囊,能快速回弹说明分流管通畅,不能回弹或回弹缓慢说明分流管脑室端阻塞。分流管腹腔端阻塞的判定比较困难,可以做腹部B超判定有无腹腔内包块,有包块提示大网膜包裹分流管。处理方法:做分流管调整术或更换分流管。 (5)分流管断裂:常见断裂部位:分流管和泵连接处和皮下走行区。用手触摸和行X线片检查,可判定分流管断裂部位。可用腹腔镜将滑入腹腔内的分流管取出。 (6)其他少见并发症:包括分流管进入肠道、膀胱、阴道、胸腔等,头部分流管皮下积液(因硬膜切口过大和脑皮层薄),分流管处皮肤破溃、感染,颅内出血(分流管颅内盲穿所致),帕金森样反应(在正常压力脑积水分流术后偶见,多巴胺药物有效)。 五、术后随访要在术后不同时间(术后24h内、术后2周、术后3、6、12个月)以及症状有变化、根据病情需要应该做头颅影像(CT或MRI)检查。L-P分流应行腰椎X线平片检查,判断腰大池段的位置。对分流术的疗效评价是一个长期和综合分析的过程,要结合患者脑积水的类型、手术方式、术后影像学、术后并发症、临床症状和体征、运动功能、认知功能、神经电生理(如肌张力)、排尿功能、日常生活能力等诸多方面对患者进行术后短期疗效和长期随访的评价。 六、特发性正常压力性脑积水1.概念:特发性正常压力性脑积水(idiopathic normal pressure hydrocephalus,iNPH)是以痴呆、步态不稳和尿失禁为临床三主征的综合征,伴随脑室扩大但脑脊液压力正常,且无导致上述症状的疾患存在。 2.临床表现: (1)步态障碍:发生率为94.2%-100%。典型的三联征为步幅小、抬腿困难和步距宽,走路缓慢且不稳,有时会跌倒,尤其在起身站起或转向时更明显。引流一定量的脑脊液后,步态改善的特征性表现为步幅的增大及转向时所需步数的减少,其他方面则无明显改善。 (2)认知功能障碍:发生率为69%-98%。轻度患者可有额叶相关功能如注意力、思维反应速度、语言流利程度、执行能力和记忆力的障碍。在记忆障碍方面,回忆记忆障碍要比识别记忆障碍相对严重。重度患者可表现为全部认知功能的障碍。少数者也可有行动笨拙及书写困难的表现。分流术后言语记忆和思维反应速度障碍的改善较明显。 (3)排尿功能障碍:发生率为54.0%-76.7%。患者膀胱内压力测定时,显示膀胱机能亢进。 (4)其他临床表现:包括也可见上肢运动功能减退,表现为抓物上抬时因指尖抓力的减退而导致抓起动作缓慢。CSF引流测试可使上举动作得到改善。其他神经系统表现有运动迟缓、运动技能减退、过伸强直、眉心反射、撅嘴反射、掌颏反射出现频率较高。约88%的患者有精神症状,其中包括易疲劳、不耐心、情绪不稳定、瞌睡、冷淡。 3.辅助诊断方法: (1)CT和MRI检查:均可见脑室扩大,外侧裂及脑沟的增大,是脑萎缩的表现,大脑凸面的脑沟和蛛网膜下腔变窄。一些患者可有脑萎缩存在,海马萎缩和海马旁沟增宽均较轻,这一特点有助于和阿尔茨海默病的鉴别。有研究发现:大脑凸面蛛网膜下腔变窄而外侧裂增宽(在MRI的冠状位像上更确切),具有重要的价值。 (2)CSF引流测试:该测试是通过腰穿引流一定量的CSF后观察临床症状有无改善的一种方法,也是诊断NPH的有效方法之一。每次引流CSF为30-50ml,如果临床症状呈进行性加重则有必要至少在1周后重复CSF引流测试,引流量可比首次多。对于CSF单次引流测试阴性的患者,可考虑进行CSF持续外引流测试,控制性引流量为500ml/3d。 (3)CSF动力学测试(脑脊液容量负荷测试):通过向蛛网膜下腔注射正常生理盐水,可测定CSF流出阻力(outflow resistance,Ro)及CSF流出传导力(outflow conductance,Cout)。但由于Ro值在不同单位测定,结果不是恒定的;而且Ro值和术后症状改善程度之间,还没有相关性的研究结果;此外Ro和Cout测定,缺乏标准化的数值。因此,此方法为非强制性测试方法。 4.诊断分类和标准:典型的临床表现和影像学所见,是诊断iNPH的必备条件。将iNPH分为2个诊断级别为可能性(possible)和很可能性(probable)。 (1)可能性iNPH的诊断标准:起病年龄≥60岁,缓慢起病并逐渐加重,有时症状可波动性加重或缓解;临床上有典型步态障碍、认知功能障碍和尿失禁三联征表现中的至少2种症状;头颅CT或(和)MRI检查显示脑室增大(Evans指数>0.3),并且无其他引起脑室增大的病因存在,脑室周围可有/无低密度(CT扫描上)或高信号(MRI的T2加权像上)征象,大脑凸面脑沟变窄;腰穿(侧卧位)或脑室内ICP监测证实ICP≤200mm H20,CSF常规和生化检查正常;临床、影像学和生化学检查排除可能引起上述临床表现的神经系统和非神经系统疾患存在;有时可能同时伴有帕金森病、阿尔茨海默病和缺血性脑血管病存在;既往无可能引起脑室增大的自发性或外伤性颅内出血(包括蛛网膜下腔出血、脑室内出血、各种类型的颅内血肿)、脑膜炎、颅脑手术病史,无先天性脑积水病史。 (2)很可能性iNPH的诊断标准:符合术前可能性iNPH的诊断标准,同时符合下列标准之一者:CSF引流测试后症状改善;CSF持续引流测试后症状改善;诊断性脱水治疗后症状改善;Ro测定或ICP监测异常。 5.手术治疗: (1)常用分流手术方法有脑室-腹腔分流术(V-P)、脑室-心房分流术(V-A)和腰池-腹腔分流术(L-P)。V-P分流是最常用方法,疗效肯定。L-P分流术近几年逐渐受到重视,建议多做L-P分流术。 (2)分流管装置的选择,采用可调压分流管治疗的疗效可能更好,因为可以术后在体外根据患者的状态来逐步调节设定的压力,解决分流不足或过度分流的问题,一般是先设定一个稍高的压力,然后根据临床症状渐渐将压力调低。如果使用固定压力分流管,建议使用中压型(50-110mm H2O)分流管(建议用抗虹吸型)。 (3)部分患者可做第三脑室底造瘘术,但不建议首选此方法。 注本专家共识仅供临床医师在诊治过程中参考,不具备法律功效,共识中观点也需要随着诊治技术的进步不断完善,同时共识不排斥尚未列入共识内的个体化成功的诊治经验。 共识专家组名单 鲍南(上海儿童医学中心神经外科) 陈国强(清华大学玉泉医院神经外科) 陈谦学(湖北省人民医院神经外科) 更·党木仁加甫(新疆医科大学第一附属医院神经外科) 窦长武(内蒙古医科大学附属医院神经外科) 贺晓生(第四军医大学西京医院神经外科) 梁玉敏(上海交通大学附属仁济医院神经外科) 鲁晓杰(无锡市第二人民医院神经外科) 毛颖(复旦大学附属上海华山医院神经外科) 石祥恩(首都医科大学附属北京三博脑科医院神经外科) 孙涛(宁夏医科大学附属医院神经外科) 王贵怀(首都医科大学附属北京天坛医院神经外科) 王汉东(南京军区南京总医院神经外科) 王茂德(西安交通大学医学院第一附属医院神经外科) 肖庆(清华大学玉泉医院神经外科) 游潮(四川大学华西医院神经外科) 于炎冰(北京中日友好医院神经外科) 余新光(解放军总医院神经外科) 岳树源(天津医科大学总医院神经外科) 詹仁雅(浙江大学第一附属医院神经外科) 詹升全(广东省人民医院神经外科) 张赛(武警后勤学院附属医院神经外科) 张亚卓(北京市神经外科研究所) 张玉琪(清华大学玉泉医院神经外科)
周朋 副主任医师 山东省千佛山医院 神经外科1921人已读 - 学术前沿 皮肤软组织扩张器在头皮缺损中的应用
神经外科手术时,对切除巨大肿物后造成的头皮全层缺失进行修复是一个常见问题。既要寻找足够的自体的皮肤来覆盖创面,对于头部这种暴露部位又要求覆盖创面的皮肤颜色、质地等尽量与原来组织相同。扩张器的出现很好的解决了这一问题,可用扩张出的皮肤和软组织加以修复,其最大优点是修复后的头皮均长有毛发,并且瘢痕在毛发的遮挡下基本无从发现。一、原理将皮肤软组织扩张器植入病变附近正常皮肤软组织下,通过间断向扩张囊内注射液体以增加扩张器容量,使其对表面皮肤软组织产生压力,通过扩张机制对局部的作用使组织和表皮细胞的分裂增殖及细胞间隙拉大,从而增加皮肤面积,取出扩张囊后,可用新增加的皮肤软组织进行组织修复及器官再造。头皮扩张术适应于头皮局限性病变或缺损, 面积不超过头皮1/2 的病变, 包括外伤性头皮缺损、 头皮肿瘤和斑痣、 瘢痕性秃发和脂溢性秃发等。通过周密计划, 细心实施组织扩张术最大可修复50%的头皮缺损。二、手术基本方法1. 皮肤扩张器一期植入术术前测量病变范围,根据病变范围及部位选择合适形状和容量的扩张器。手术分两期, 行一期手术前, 对最终形成的扩张皮瓣应有初步设计, 一般于缺损区(或病变区)与正常头皮交界处作切口, 也可垂直于扩张区作切口, 可减少注水对切口的张力, 早期注水扩张。放置扩张器于拟定位置, 距其边缘外1 cm 标记剥离范围, 切开头皮至帽状腱膜下钝性剥离至预定范围。 剥离腔内无出血后, 放置负压引流管。 扩张器注入生理盐水少许证实无渗漏后,带水置入。注水阀内置, 稍远离扩张囊缝合固定, 乳突部和头顶是放置注水阀的理想部位, 如扩张器放置于竖直面(如额部) , 注水阀应置于上方牢固固定, 可预防扩张器注水充盈后受重力作用而下滑。在切口处将帽状腱膜与其下骨膜固定数针, 减少扩张器对切口的张力, 再分两层缝合头皮。缝合后再次注水, 确保导管通畅。术毕加压包扎, 术中、 术后预防性应用抗生素。2. 常规注水扩张 术后3 d 拔除引流管后即可开始少量注水, 以减少死腔, 预防血肿形成。扩张器注水每次为扩张器额定容量的10%~ 20%。头皮扩张不宜太急, 以免毛囊缺血坏死, 影响术后毛发生长。在切口拆线后, 视头皮松紧程度, 每周注水1~ 2 次, 注水至所需扩张面积后如条件充裕可放置4~ 6 周再行二期手术, 能减轻皮瓣回缩。3. 二期扩张皮瓣转移修复手术 切开头皮后,取出扩张器,参照术前已设计的切口, 边切边试行转移并缝合定点, 最后确定形成的皮瓣和修复的面积。 使用2 枚以上扩张器时, 取出扩张器后, 每形成一个皮瓣即定位缝合, 然后再形成下一个皮瓣, 依次切除病变。若一次扩张形成的皮瓣难以全部修复时, 不可勉强, 可再置扩张器接力扩张。 术后需保持扩张皮瓣适当张力。皮瓣转移后, 创腔置负压引流管。 为防止术后瘢痕增宽及皮瓣远期挛缩, 皮瓣下的帽状腱膜层及包膜需缝合至稳定结构, 如邻近的腱膜和颅骨骨膜, 分两层缝合头皮, 以最大限度减少切口张力。皮瓣转移后, 对多余部分不必去除, 以避免损害皮瓣血运, 小的 “猫耳” 畸形一般不需处理, 多可自行消失。三、基本原则和注意事项1. 扩张器的选择一般优先考虑使用容积较大的扩张器,扩张器底部直径需超过缺损长径的2 倍才能提供足够的组织来覆盖缺损和供区, 而与扩张器的形状无关。长方形(圆柱形)的扩张器能够提供更多可利用的组织。据报道长方形的扩张器可多扩出38% , 而圆形的只有25% 。2. 扩张头皮面积的预测简单直接测量法, 经扩张器表面的距离为S, 其直线距离为L , 则扩张皮瓣的长度为S- L。同法测其宽度, 长×宽得其面积。3. 扩张皮瓣设计的原则①充分舒展扩张的皮肤组织; ②减少辅助切口, 切口于隐蔽位置, 顺毛发生长方向; ③皮瓣长轴顺血管走行方向, 且尽量包含轴型血管; ④皮瓣远端携带的未扩张皮肤长度一般不超过3~5 cm; ⑤遵循常规皮瓣设计的原则, 强调反复的逆行试样设计。 重建阶段, 应先按缺损和扩张头皮设计好皮瓣, 再取出扩张器。首选推进皮瓣, 旋转和易位皮瓣亦可选用。4.扩张器注射壶的放置方法注射壶可内置或外置。壶内置时每次注液需穿刺皮肤,扩张后期有时不易找到注射壶或注射壶渗漏时不便处理;壶外置时可避免注液时穿刺皮肤,但可引起感染,需在扩张期间加强护理。第二期手术伤口愈合后,应采取防止疤痕增生变宽、对抗皮瓣挛缩的措施,如弹力外套、颈托、支架等。术后早期扩张皮瓣变硬,并有回缩的趋势,一般术后6个月能够软化恢复自然弹性。5.扩张器的植入要点和注意事项①手术部位的选择应靠近病变部位。②腔穴应足够容纳扩张器和注射壶,连接管不可折叠。③避免切口与扩张器长轴平行,否则切口在扩张时会变宽。④手术中对注射壶进行穿刺操作时,建议采用外径等于或小于0.7mm的注射针;如需多次穿刺时,应尽量选择在不同的位置进行(1mm2内穿刺数应≦1次),避免由于过度穿刺导致注射壶渗漏。四、手术并发症1.血肿:负压吸引;向扩张囊内注入其容量20%的生理盐水。2.扩张器外漏:切口的选择应距扩张器1-2 cm ,并间断缝合皮下组织 , 在切口与扩张器之间形成一个“隔离带” ; 或,与扩张器主轴垂直的切口 。皮下腔隙的剥离范围应略大于扩张器 , 以防止放置扩张器时折叠成角 。3.术后感染4.扩张皮瓣坏死:防治方法 :① 扩张器应尽量埋植于深层筋膜下 , 增加皮瓣中央区厚度。 ②术中缝合时 , 保持皮瓣一定张力。 ③ 术中尽可能保留具有血供的包膜 ,必要时可“ # ”字形划开以增大皮瓣面积。 ④ 术后包扎既要有一定的张力 , 同时又不能阻碍血运。 5.扩张皮瓣回缩:防治方法:①延长扩张时间 ,② 选择较大容积的扩张器 , 并遵循“充分扩张 , 宁多勿少”的原则。缺损 1cm2需预计扩张器容量 : 头部为4 mL 。6.扩张器漏7.注射壶翻转,导管折叠。五、扩张器结构目前临床上应用的扩张器主要是由硅橡胶材料制成的可控扩张器,由扩张囊、注射壶及连接导管三部分组成。①注射壶直径约1~2cm,基底有金属片以防止穿刺过深或穿破,壶内有特制的单向或双向活瓣,液体注入后能自行关闭,不致从针孔外溢。②连接导管直径约3mm,长约5~15cm不等。③扩张囊是扩张器的主体,按形状可分为圆形、椭圆形、肾形、半月形、矩形、圆柱形等,有10ml到800ml的多种不同规格。作者:周朋,哈医大四院神经外科 E-mail:fzsf999@yahoo.com.cmphone:15846340580
周朋 副主任医师 山东省千佛山医院 神经外科5672人已读 - 医学科普 肺癌脑膜转移
脑膜转移 (meningeal metastases),又称脑膜癌病(meningeal carcinomatosis,MC)、癌性脑膜炎,是恶性肿瘤细胞广泛转移浸润脑膜、蛛网膜下腔的一类疾病,是恶性肿瘤严重并发症之一。【流行病学】 脑膜癌病发病率低,约占颅内肿瘤3%,MC原发灶国内以肺癌最多,其次为胃癌、乳腺癌、恶性淋巴瘤等。我国以肺癌转移最多见,肺癌引起的脑膜癌发病率约2%[1]。【病理生理学】癌肿转移脑膜主要通过血液和淋巴。、【临床表现】 最常见症状包括头痛、四肢乏力、视物模糊、意识改变、癫痫等,本例患者具有上述症状。 MC临床表现缺乏特异性。MC可先于原发肿瘤之前出现神经系统症状,早期可只表现顽固性头痛,20%~40%的MC原发灶隐匿,找到原发肿瘤有助于诊断; 总结脑膜癌病人的临床表现:主要为脑部症状,如头痛、呕吐、颈项强直、脑膜刺激征、症状性癫痫发作、意识障碍及精神症状;其次表现为动眼、三叉、外展、舌下神经等脑神经麻痹症状;还有颈、腰、下肢疼痛等脊神经根受损症状,部分病例出现肢体无力现象。 其临床特征可以归纳为:①肺癌患者出现顽固性头痛、呕吐、颅神经或脊神经功能障碍,伴有不同程度的脑膜刺激征;头颅或脊髓部位的磁共振成像(MRI)除脑部有病灶外,尚可见到柔脑膜有不规则占位性病变;脑脊液中可能找到癌细胞,且癌细胞病理与患者的肺癌病理相同;脑脊液中与肺癌相关的肿瘤标志物升高;脑脊液细菌培养阴性,能排除其他原因引起的脑脊膜病变;Wnq胸部肿瘤防治工作组 临床上对肺癌患者若出现颅内压增高及脑膜刺激征的表现即使CT及MRI检查无明显异常也应高度警惕脑膜癌病的可能.【诊断】 脑膜转移诊断较困难。 CSF细胞学检查是确诊MC的主要方法,但疾病早期和单次CSF阳性率低。重复腰穿、送检更多的CSF标本和及时处理标本等有助于进步阳性率,但仍有10%患者CSF细胞学持续阴性,因此阴性结果不能排除MC。 脑脊液中找到恶性肿瘤细胞是诊断的金标准,但阳性率不高。在一些临床研究中,第1次腰穿的细胞阳性率为50%,3次腰穿的阳性率为85%~90%,但仍有10%~15%的患者漏诊,提高阳性率可采取多次穿刺送检,有报告反复穿刺送检第5次才找到癌细胞。 脑膜癌病人的脑脊液检查均有一定程度的改变,主要为压力增高、白细胞增多、蛋白增高、糖含量下降、氯化物降低。脑脊液细胞学检查所见与一般恶性肿瘤相似,胞核明显增大,胞浆比例大于正常,核染色深,胞浆呈强嗜碱性,多为蓝色,可见空泡;核呈圆形或卵圆形,多为一个核,少数为多核,部分可见核仁及司状分裂。腺癌细胞还可见印戒样细胞,恶性黑色素瘤细胞胞浆内含黑色素颗粒。 核磁共振成像增强扫描对于诊断有帮助,而诊断率不高,Yousem等[2]报道肿瘤的软脑膜蛛网膜转移的MRI阳性率为31.4%,主要是与临床表现结合进行诊断。其他可通过脑脊液LDH和CEA异常升高辅助诊断。 脑膜癌临床表现复杂,除了脑膜刺激征外,还有其他脑神经、脊神经或脊神经根症状。头颅CT、磁共振成像、脑电图、脑脊液常规检查对这一疾病又无诊断价值,故临床极易误诊为中枢神经系统感染、蛛网膜下腔出血、癫痫、脑梗死等。所以,当以这些疾病治疗效果欠佳时,临床医生应考虑脑膜癌的可能,并及时进行脑脊液细胞学检擦够对不能确诊的病人,应反复多次作检查如能在脑脊液中找到癌细胞,即可确诊。【治疗】 治疗手段包括全身化疗、鞘内治疗、局部放射治疗等。Wnq胸部肿瘤防治工作组 鞘内化疗已成为脑膜转移的主要治疗方法,鞘内化疗可选择的药物很少,主要是甲氨蝶吟、阿糖胞苷和噻替哌3种。同时,鞘内大剂量多次给化疗药物,会产生较重的神经系统毒性。 全身化疗的作用和开发有效的鞘内治疗药物是当前研究的焦点。 随着分子靶向药物的广泛应用,有报道易瑞沙治疗肺腺癌引起的脑膜癌疾病控制率达到60%,并能延长患者生存期[1,4]。 有报道患者脑膜转移应用吉非替尼和VM-26+DDP方案治疗后,患者自感头痛症状减轻,症状改善明显,生存期已超过1年。提示明易瑞沙联合VM26、顺铂同时治疗肺癌脑转移有明确的效果,患者耐受性好,可以为NSCLC脑膜转移的治疗开辟了一个新思路。 局部放疗能缓解症状但不能治疗整个蛛网膜下腔的肿瘤,而全脑全脊髓放射治疗易伴高死亡率和严重的骨髓抑制[3],目前临床上较少采取。 用20%甘露醇静脉快速滴注难以缓解头痛症状。关于肺癌脑/脑膜转移的治疗更加复杂,除脑转移灶的治疗外,还要兼顾到脑膜病灶的治疗。鞘内化疗是脑膜转移的主要治疗办法,但大多效果较差。【预后】 脑膜癌病情进展迅速,预后差,生存期短,未经治疗的患者中位生存时间为4~6周,且对治疗反应率较低,约为20%,治疗后中位生存期仅为3~4个月,一般生存期4~6个月。 MC为肿瘤晚期,预后极差。朱海青等报道MC确诊后生存期为6~14个月,其中多数在数月内死亡。 脑膜癌均恶性肿瘤晚期,预后差,目前尚无满意的治疗方法。但只能缓解症状、延长生存期。【参考文献】 1 Sudo J, Honmura Y. Meningeal care inomatosis in patients with lung cancer,Nikon kokyuki Gakkai Zasshi, 2006,44:795799. 2 Yousem DM, Patrone PM, Grossman RI. Leptomeningeal metastases; MRI evaluation.J Comput Assist Tomogr,1990,14:255261. 3 De Angelia LM, Diagnosis and treatment of leptomeningeal metastasis.Educational Book Am Soc Clini Oncol,2002:369374. 4 Carcinomatous meningitis from nonsmall cell lung cancer responding to gefitinib.Int J Cin Oncol,2006,11:243245.
周朋 副主任医师 山东省千佛山医院 神经外科4648人已读





