李祥攀医生的科普号
- 精选 头颈部肿瘤放疗(喉、下咽、口腔、鼻窦、鼻咽癌)
简介头颈部肿瘤包括颈部肿瘤、耳鼻喉科肿瘤以及口腔颌面部肿瘤三大部分,占全身恶性肿瘤的4.45%。头颈肿瘤的发病依次为喉(32.1%)、甲状腺(19.6%)、口腔(16.1%)、鼻咽(14.9%)、鼻腔副鼻窦(6.6%)、大涎腺(4.2%)、口腔(3.3%)、眼(1.52%)、下咽(1.5%)。在性别上,除甲状腺肿瘤女性(14.2%)明显多于男性(5.40%)外,其余以男性居多。头颈部所发生的肿瘤,其原发部位和病理类型之多,居全身肿瘤之首。同时,头颈部重要器官比较集中,解剖关系复杂,治疗方法各异。按部位, 因生活环境不同及致病因素的不同,我国各地头颈部肿瘤的发病情况也不同。譬如鼻咽癌在两广地区发病较高,而甲状腺肿瘤以沿海和内陆缺碘地区发病较高。治疗对于晚期颈部转移性癌的诊断,多依靠询问其它部位患肿瘤史,并可借助于CT、MR、颈部细针穿吸活检等方法明确诊断。应采用以手术为主,术前、术后新辅助或辅助放化疗的综合疗法。 放射治疗在肿瘤的综合治疗中占有重要的地位,在所有恶性肿瘤的治疗中,约70%的病人需要放射治疗的参与。近年来,随着科学技术的发展,医学影像学、计算机技术、多叶准直器等与加速器技术密切结合,三维适形放疗、调强放疗、图像引导放疗等精确放疗技术相继应用于临床,使得放射治疗学得到迅速的发展,特别是头颈部恶性肿瘤,如鼻咽癌、口咽癌、喉癌、下咽癌及鼻腔、鼻窦恶性肿瘤等,精确放疗不但提高了疗效,而且显著地降并发症。 所谓适形调强放射治疗,是指利用各种物理手段,根据肿瘤靶区的形状,通过调节和控制X射线在照射野内的强度分布,产生不同剂量梯度,对肿瘤靶区给予致死性的高剂量照射,而对肿瘤周围正常组织控制在耐受剂量以下的一种放射治疗技术。首先,是对肿瘤靶区达到三维适形的照射;其次,是使肿瘤靶区和邻近敏感器官可以获得照射剂量强度的调节。其追求的目标是尽可能提高放疗的增益比,即最大限度地将放射线剂量集中到肿瘤病灶内,而使周围正常组织和器官少受放射治疗的损害。 头颈部恶性肿瘤的调强放射治疗能够提高靶区剂量,同时减少周边临近重要器官的照射剂量,尤其能够保存大部分腮腺功能。临床研究显示,当腮腺受照射平均剂量小于26Gy时,有望保存大部分腮腺功能。所以,头颈部恶性肿瘤的调强放疗也被称为“保腮放疗”。降低腮腺受照射剂量和保存腮腺功能是其最重要的目的之一。有研究证实,鼻咽癌是头颈部肿瘤中最适宜应用调强放射治疗的恶性肿瘤。鼻咽癌也是一种放疗可以治愈的肿瘤,其5年生存率可达80%以上。头颈部恶性肿瘤放疗注意事项 放疗前注意事项 1.诊断明确,包括病理、CT、MRI,甚至PET/CT影像学检查。 2.口腔处理:洁齿,处理龋齿、残根,拆除金属齿冠,待拔牙创面愈合后才能开始放疗。 3.戒烟酒。 4.不吃烟熏、腌制食品。 5.育龄妇女问清月经史,如合并妊娠,需终止妊娠后再放疗。 6.做好个人卫生,剪短头发。 放疗中注意事项 1.给予高蛋白、高维生素饮食。忌辛辣及烟酒等刺激性食物,忌长期食用腌制食品。宜多食新鲜的蔬菜水果,新鲜的鱼类、虾类,主张多食蘑菇类食品。尤其多食豆类食品(豆浆或豆腐),饮绿茶。鸡、鸭、牛、羊肉等肉类食品都可以进食。2. 注意口腔卫生,用含氟牙膏刷牙,每天至少3次。每天坚持口腔锻炼,起床后及睡觉前都要张开大口50次。口腔黏膜反应较剧烈影响进食时,可给予输液及相关对症治疗。 3.保护射野皮肤勿受理化刺激,防晒,保持干燥,尽可能不碰水,放疗后可涂搽专用的放射防护药膏(放疗前4小时禁用)。 放疗后注意事项 1.定期复查复查时间可根据医嘱,原则上第1~2年建议每3个月复查1次,第3年后每年复查1~2次。对于接受过化疗的患者,放疗结束后休息3周,至医院检查决定是否进一步的化疗。休息期间每周检查一次血常规,若白细胞低于正常,建议到附近医院予以纠正。 2.防治感冒及头颈部感染以免诱发颈部急性蜂窝组织炎,如出现局部红肿,可去医院对症治疗。 3.注意口腔卫生放疗后2~3年内勿拔牙,必须拔除时,一定要告知口腔科医生有面颈部肿瘤放疗史。放疗后牙齿可能逐渐松动,牙冠头脱落,一般需三年以上才能拔牙。 4.保护射野皮肤免受理化刺激 防晒,保持干燥。放疗后照射区域的皮肤变黑症状一般能在1-2个月内缓解。放疗后照射区域头发脱落属于正常现象,可以很快长出新的头发。放疗后喉咙疼痛,痰多症状可能要维持1-2个月才能有所恢复。放疗后口干很难恢复,因为唾液腺受到损伤,唾液分泌明显减少,需要自己多饮水。鼻腔粘膜干燥,容易出血,少量血丝不必惊慌,若出血次数多,量大则需及时至医院检查。放疗后可能无法食用干硬的食品,要进食软食、半流食。放疗后颈部照射区域皮肤纤维化,变硬。5.已婚妇女3年后再考虑生育。6.加强营养,生活规律,精神愉快复查需要随时携带的东西:病历本,出院小结,治疗前及治疗的MRI或CT片。放疗结束后2~6个月可能出现颜面部、颈部皮肤肿胀,不必惊慌,这是放疗导致的淋巴回流不畅引起的,3-6个月才能逐渐恢复正常。但若出现呼吸困难应及时去医院急诊就诊,请医生紧急处理。
李祥攀 主任医师 武汉大学人民医院 肿瘤中心4478人已读 - 典型病例 肺腺癌化疗无效,靶向治疗后肺原发肿瘤明显缩小,肺内播撒病
http://www.jianshu.com/p/5b97577c0fc6?utm_campaign=hugo&utm_medium=reader_share&utm_content=note&utm
李祥攀 主任医师 武汉大学人民医院 肿瘤中心8484人已读 - 典型病例 艾坦治疗经典病例:宫颈癌手术放化疗后复发,免疫治疗无效
http://www.jianshu.com/p/43d9c152fd7c?utm_campaign=hugo&utm_medium=reader_share&utm_content=note&utm
李祥攀 主任医师 武汉大学人民医院 肿瘤中心1930人已读 - 典型病例 复发胶质瘤 抗血管生成治疗
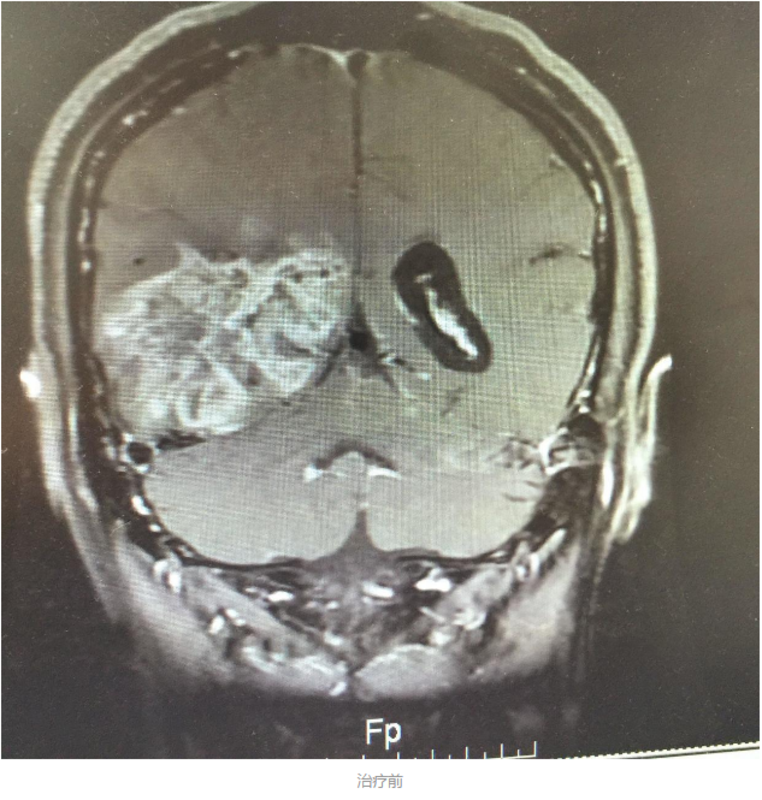 李祥攀 主任医师 武汉大学人民医院 肿瘤中心949人已读
李祥攀 主任医师 武汉大学人民医院 肿瘤中心949人已读 - 典型病例 食管癌,肿瘤近全消
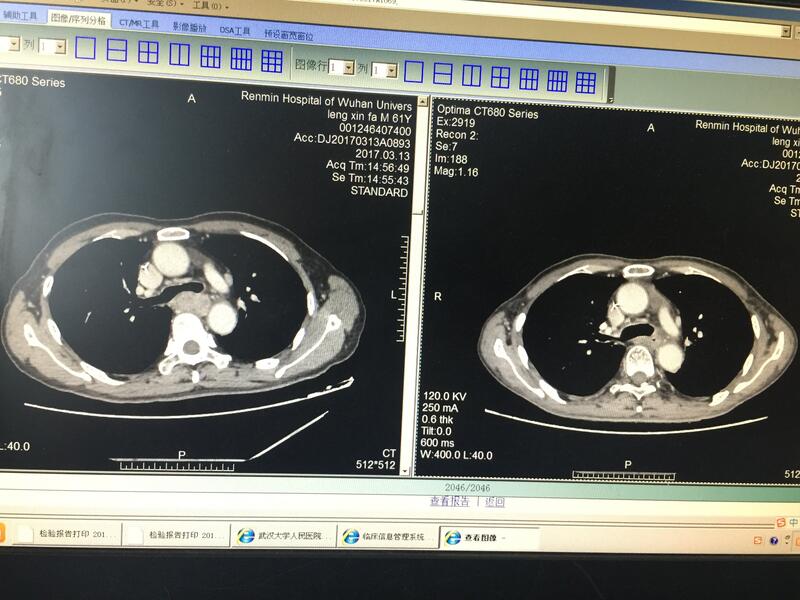 李祥攀 主任医师 武汉大学人民医院 肿瘤中心1405人已读
李祥攀 主任医师 武汉大学人民医院 肿瘤中心1405人已读 - 典型病例 宫颈癌肝转移,艾坦控制病灶
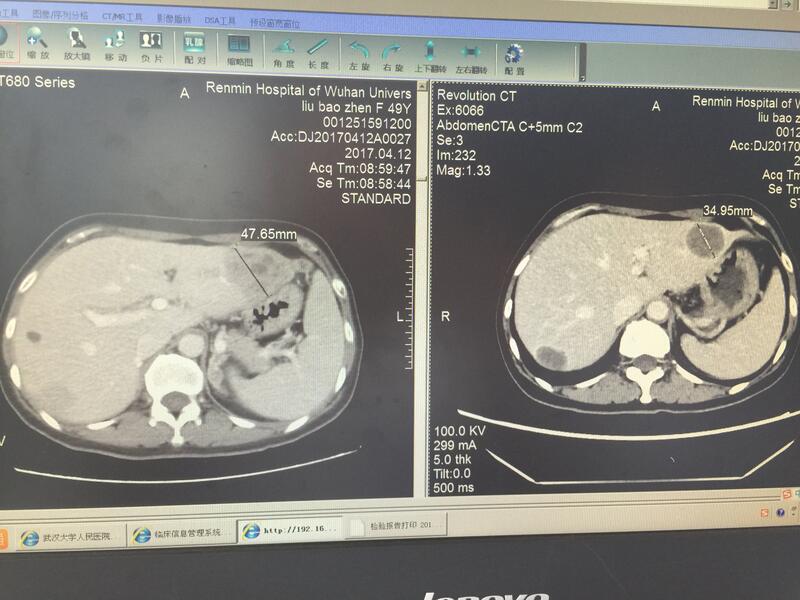 李祥攀 主任医师 武汉大学人民医院 肿瘤中心1458人已读
李祥攀 主任医师 武汉大学人民医院 肿瘤中心1458人已读 - 学术前沿 ASCO指南:I 到 IIIA 期NSCLC辅助治疗
继2007年ASCO公布早期NSCLC辅助治疗后,根据关键临床试验长期随访数据、靶向和免疫药物辅助治疗临床试验、ⅠB期中较大体积肿瘤亚组分析,ASCO于2017年4月24日在JCO上再次对指南进行更新
李祥攀 主任医师 武汉大学人民医院 肿瘤中心1315人已读 - 学术前沿 EGFR治疗转移性结直肠癌的发展历程
近几十年来转移性结直肠癌(mCRC)的生存明显改善,依立替康、奥沙利铂、卡培他滨、靶向VEGF和EGFR的治疗、瑞格非尼以及TAS102等药物功不可没,中位生存超过30个月。日本的Miyamoto教授在Int. J. Mol. Sci杂志上发文,详述了mCRC治疗主力军EGFR靶向治疗的发展历史,耐药机制以及针对耐药的新药研发。 抗EGFR抗体的临床进展 西妥昔单抗和帕尼单抗均作用于EGFR胞外区域,抑制下游RAS-RAF-MEK-ERK通路。二药与FOLFIRI或FOLFOX联合治疗野生型RAS mCRC有效,二药区别在于蛋白特征和种属差别,此外西妥昔单抗还可通过介导抗体依赖细胞毒作用发挥抗肿瘤作用。ASPECCT研究显示帕尼单抗作用不逊于西妥昔单抗,二者对化疗耐药KRAS外显子2野生型mCRC的OS相似,不过帕尼单抗组的3/4级低镁血症发生率更高。 RAS状态对抗EGFR治疗的影响 最初拟采用EGFR表达作为抗EGFR治疗的预测标志,然而事与愿违,BOND研究显示EGFR强度与客观治疗反应(ORR)无关。后来发现KRAS基因外显子2中12和13密码子突变可致抗EGFR治疗耐药,突变导致RAS-RAF-MEK-ERK途径的结构性活化。40%的mCRC可检测到KRAS突变,原发灶与转移灶间突变一致性很高。 现在已证实KRAS外显子3、4或NRAS外显子2、3、4的低频突变也可介导抗EGFR治疗耐药,因此无RAS突变患者才更可能从治疗中获益。PRIME研究中无KRAS外显子2突变的患者中17%有上述低频突变,患者对帕尼单抗缺少治疗反应,PFS和OS更差,CRYSTAL和OPUS研究也证实了这一结果。 KRASG13D 突变 临床前研究和回顾性研究显示 KRASG13D突变患者可能获益于西妥昔单抗治疗,De Roock报告此种患者与其它KRAS突变患者相比,西妥昔单抗治疗可延长OS。CRYSTAL和OPUS的荟萃分析显示 KRASG13D 突变亚组患者接受西妥昔单抗+化疗与化疗相比,能改善PFS和治疗反应率。鉴于此进行了二项前瞻性II期研究,但未能证实西妥昔单抗单药或与依立替康联合在KRASG13D突变mCRC中的活性。因此目前并不常规推荐 KRASG13D突变患者进行抗EGFR治疗。 一线抗EGFR治疗与贝伐单抗治疗 一线是贝伐单抗还是抗EGFR抗体与化疗联合更佳的争论一度甚嚣尘上,FIRE-3、CALGB/SWOG 80405和PEAK研究直接对二者进行了比较。FIRE-3研究中比较FOLFIRI+贝伐单抗和FOLFIRI+西妥昔单抗,西妥昔单抗组的OS更长,但二组的PFS几乎一致,PEAK研究比较了FOLFOX+帕尼单抗和FOLFOX+贝伐单抗,结果与FIRE-3类似。 CALGB/SWOG 80405 研究未证实西妥昔单抗或贝伐单抗与化疗联合在PFS和OS上孰优孰劣,不过西妥昔单抗组的治疗反应率更高。一项meta分析显示一线EGFR抑制+化疗在OS和ORR上较贝伐单抗+化疗获益更多。PARADIGM研究正在进行中,比较帕尼单抗+ FOLFOX与贝伐单抗+FOLFOX。 原发肿瘤位置是mCRC的预后和预测标志 野生型RAS mCRC的原发肿瘤位置的预后和预测作用也是探讨热点。CRYSTAL研究回顾性分析显示右半肿瘤采用FOLFIRI+西妥昔单抗治疗的PFS和OS明显差于左侧,左侧肿瘤在FOLFIRI基础上加入西妥昔单抗能明显改善PFS、OS和ORR,而右半肿瘤加入西妥昔单抗的获益有限。 FIRE-3研究中比较的是FOLFIRI+西妥昔单抗和FOLFIRI+贝伐单抗,结果左半肿瘤西妥昔单抗治疗的OS优于贝伐单抗,PFS和ORR无显著差别;右半肿瘤无论是OS还是PFS、ORR均无显著差别。多元分析显示原发肿瘤部位与治疗模式间存在明显的相互作用。 上述结果证实了原发肿瘤位置的预后和预测作用,右半肿瘤在西妥昔单抗治疗中获益不多,而左半肿瘤则明显获益,差别可能源于分子/遗传学/胚胎/流病学的差别。例如右半结肠癌与BRAF突变、DNA甲基化、过突变的CMS亚型相关,需要进一步的分子和遗传学分析研究。 抗EGFR治疗耐药机制 RAS野生型 mCRC初始对抗EGFR治疗有反应者,大部分最终会因抗EGFR治疗耐药而疾病进展,几个标志和途径与耐药发生相关。EGFR活化后的二个主要下游效应途径是RAS-MAPK和PI3K-AKT-mTOR,与细胞生长和增殖有关。 ctDNA研究发现抗EGFR治疗对几乎检测不到的低频KRAS突变克隆具有选择作用。BEAMing技术在极小量ctDNA中就可检测到体突变,Morelli采用该技术研究发现抗EGFR治疗耐药后,最初为KRAS野生型的患者中44%发生获得性突变,非典型KRAS密码子61和146突变更常见,其中35%原本就具有低频突变克隆,说明在未治疗的原发肿瘤中即已存在耐药突变,这就要求更敏感的突变检测技术以选择最可能获益抗EGFR治疗的患者。 第二种耐药机制是EGFR的胞外区域(ECD)发生突变,阻止药物与受体结合。虽然抗EGFR耐药后的继发EGFR突变极少见,但Montagut等发现获得性EGFR突变S492R,并证实其与西妥昔单抗耐药相关。S492R位于EGFR的ECD,形成大的侧链干扰西妥昔单抗结合,该研究中一例EGFRS492R突变患者在西妥昔单抗耐药后对帕尼单抗仍有治疗反应,体外研也究证实了这一结果。 一些新型EGFR抑制剂能克服EGFR ECD耐药突变,Sym004是二种抗EGFR单抗的混合物,靶向EGFR ECD不同表位,介导快速的EGFR内聚化和降解。临床前研究显示卓越的抗肿瘤活性。MM-151是三种单抗混合物,能同时与不同的EGFR表位结合,保证其抗肿瘤作用的充分实施。 PI3K/AKT/mTOR途径活化也是EGFR抑制剂耐药的重要机制, PIK3CA 突变发生率10%–20%,主要位于外显子20和9,结构性活化下游信号。回顾性研究显示PIK3CA突变预测抗EGFR治疗耐药的结果互有矛盾,另有一系统综述则显示 PIK3CA突变 与抗EGFR治疗耐药可能相关,表现为PFS减少趋势和明显的OS缩短。 RAS 和BRAF 野生型mCRC抗EGFR治疗耐药的可能机制还包括 c-MET和 ERBB2畸变,通过旁路机制致获得性耐药。以往研究显示c-MET和其配体HGF既有原发也有继发耐药,全外显子和ctDNA检测均可诊断c-MET 异常,一旦发现可在对抗EGFR治疗有反应的患者中尽早启动c-MET抑制治疗。ERBB2基因扩增加是另一个抗EGFR治疗耐药的获得性驱动改变,因此联合抗EGFR 和ERBB2治疗可能有获益。 结直肠癌中的BRAF突变 EGFR介导的MAPK途径由RAS活化,BRAF 在此途径中亦发挥重要作用,5%-10% 的mCRC存在BRAF体突变,V600E最常见,导致MAPK途径结构性活化,并不依赖RAS活性 。BRAF突变与RAS突变相互排斥, BRAFV600E 突变结直肠癌具有近端、高龄、女性、MSI 、CIMP、高级别和粘液性癌等特点,BRAF 突变与mCRC不良预后相关,同时BRAF具有预测作用,患者不能从抗EGFR治疗中获益,因此不推荐BRAF突变患者使用西妥昔单抗和帕尼单抗。 联合BRAF抑制剂的治疗 BRAF 突变多见于黑色素瘤,超过60%,因此抑制BRAF激酶活性可使黑色素瘤患者获益,威罗非尼和达拉非尼治疗黑色素瘤的反应率为50%,然而BRAF抑制剂单药治疗 BRAFV600E突变mCRC无效。临床前研究显示BRAF抑制剂与其上游受体抑制剂联合能改变BRAF突变mCRC的疗效,临床研究评估亦显示结果改善。 尽管联合治疗能在最初阻止BRAF突变mCRC获得性耐药的发生,但最终还会发展为继发耐药,MAPK途径基因的改变,包括KRAS扩增、BRAF扩增和MEK1突变都可能与肿瘤耐药相关。ERK抑制剂具有抑制MAPK途径的能力,能克服现已鉴定的所有BRAF突变mCRC的获得性耐药,这说明ERK抑制剂可能是未来BRAF突变mCRC的主要治疗选择。 结语 EGFR靶向药物直接作用于癌症细胞,其作用受RAS-RAF-MEK-ERK途径的多种耐药突变影响,现有多个研究正在尝试明确哪种治疗疗效最佳。液体活检和NGS技术有助于鉴定、监测抗EGFR治疗耐药的预测标志。进一步明确抗EGFR耐药机制有助于研发更有效的治疗策略以克服获得性耐药。 参考文献 http://www.mdpi.com/1422-0067/18/4/752/htm 【文章来源:肿瘤资讯微信公众号】
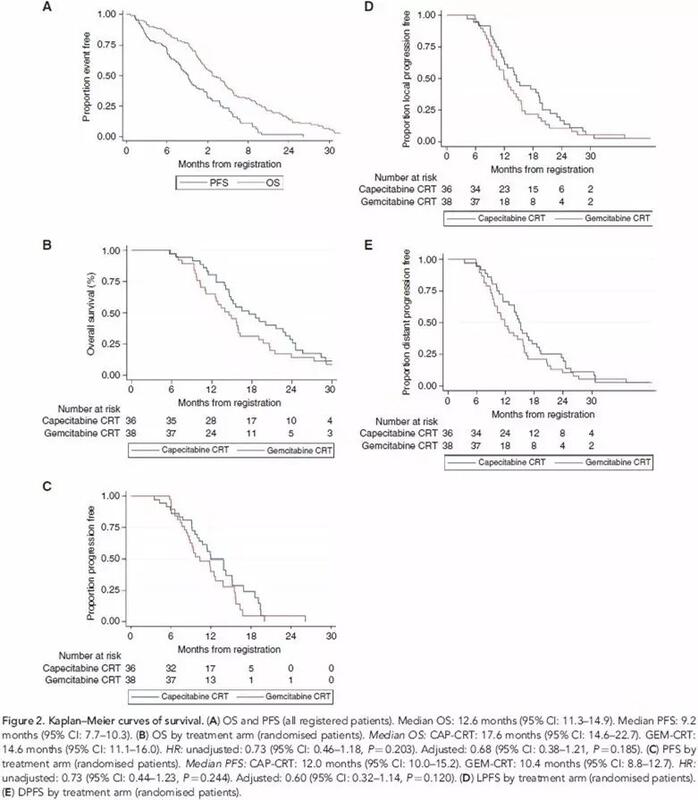
李祥攀 主任医师 武汉大学人民医院 肿瘤中心3990人已读 - 学术前沿 晚期胰腺癌化放疗用药如何选择:吉西他滨 vs 卡培他滨
导读 在最常见的十种恶性肿瘤中,胰腺癌的生存率几乎垫底。胰腺癌不仅诊断困难,大多数患者确诊时已经扩散,而且确诊后患者的5年生存率仅有5%。 临床前证据表明胰腺癌是一种系统性疾病,在这些患者中系统性治
 李祥攀 主任医师 武汉大学人民医院 肿瘤中心7120人已读
李祥攀 主任医师 武汉大学人民医院 肿瘤中心7120人已读 - 医学科普 补充维生素D和钙,不会改变老年女性癌症风险!
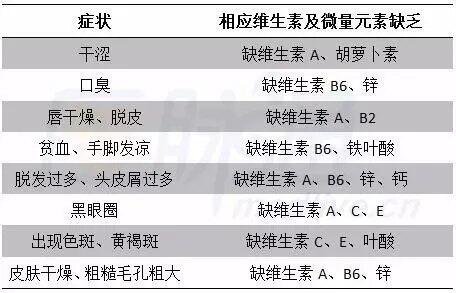
导读 一项发表在JAMA上的近期研究提示,对于绝经后健康的老年女性来说,补充维生素D和钙不会改变老年女性癌症风险! 维生素也好,维他命也罢,一个带着“生”字,一个带着“命”字,听起来就好厉害的样子。打开“万能”的百度,搜索维生素与疾病、维生素与健康、甚至维生素与肿瘤,会发现维生素几乎是万能的!不可否认,我们应该警惕身体给我们的一些细微的警告,重视微量元素的补充,比如下面一些情况就可能与相应的维生素缺乏有关: 之前有证据表明,低维生素D状态可能增加癌症风险。那么,对于老年女性来说,维生素D3和钙补充剂会降低她们的癌症风险吗? 在一项纳入2303例健康绝经后女性的随机临床试验中,其中这些女性的平均基线血清25-羟基维生素D水平为32.8ng/mL,在超过4年的随访期间,维生素D3和钙补充剂与安慰剂相比较,并未显著降低所有类型癌症的风险。 这意味着,维生素D3和钙补充剂在健康的老年女性中不会显著降低癌症风险。 主要研究 为了确定维生素D3和钙补充剂是否会降低老年女性癌症风险,来自美国Creighton大学的研究人员开展了一项随机临床试验,近期发表在JAMA杂志上。 这项临床试验在31个农村县开展,是一项长达4年(2009年6月24日——2015年8月26日的随访时间)、双盲、安慰剂对照、以人群为基础的随机临床试验。 一共有2303名≥55岁的健康绝经后女性被随机分组,1156名女性分到治疗组,1147人接受安慰剂。治疗持续时间为4年。 治疗组(维生素D3+钙剂)接受维生素D3 2000IU/d和钙1500mg/d;安慰剂组接受相同剂量的安慰剂。 该项研究的主要结局是所有类型癌症(不包括非黑素瘤皮肤癌)的发病率,应用Kaplan-Meier生存期分析和比例风险模型进行评估。 主要结果 在2303名(平均年龄,65.2岁[SD,7.0];平均基线血清25-羟基维生素D水平,32.8ng/mL[SD,10.5])随机分组女性中,2064名(90%)女性完成了研究。 在第1年时,血清25-羟基维生素D水平在维生素D3+钙剂组中是49.5ng/mL,安慰剂组为31.6ng/mL。 新确诊的癌症在109名参与者中被识别,包括维生素D3+钙剂组的45名(3.89%),安慰剂组的64名(5.58%),差异为1.69%(95% CI,-0.06%-3.46%;P=0.06)。 超过4年的Kaplan-Meier发病率在维生素D3+钙剂组和安慰剂组分别为0.042(95% CI,0.032-0.056)和0.060(95% CI,0.048-0.076),P=0.06。在未调整的Cox比例风险回归中,风险比为0.70(95% CI,0.42-1.02)。 与研究相关的可能不良事件包括肾结石和血清钙水平升高(表1)。 总之,在血清25-羟基维生素D基线平均水平为32.8ng/mL的健康绝经后老年女性中,相比于安慰剂来说,第4年时,维生素D3和钙补充剂并未显著降低所有类型癌症的风险。为了评估维生素D在癌症预防上的可能作用,进一步的研究是必要的。 文献来源: [1]Effect of Vitamin D and Calcium Supplementation on Cancer Incidence in Older Women: A Randomized Clinical Trial.JAMA 2017 Mar 28;317(12):1234-1243 [2]Garland CF, Garland FC. Do sunlight and vitamin D reduce the likelihood of colon cancer?Int J Epidemiol. 1980;9(3):227-231. 【文章来源:医脉通肿瘤科微信公众号】
 李祥攀 主任医师 武汉大学人民医院 肿瘤中心1542人已读
李祥攀 主任医师 武汉大学人民医院 肿瘤中心1542人已读





