科室介绍 查看全部
科室医生 查看全部
科普·直播义诊专区 查看全部
- 精选 颈内动脉血泡样动脉瘤的诊治1例报告并文献复习
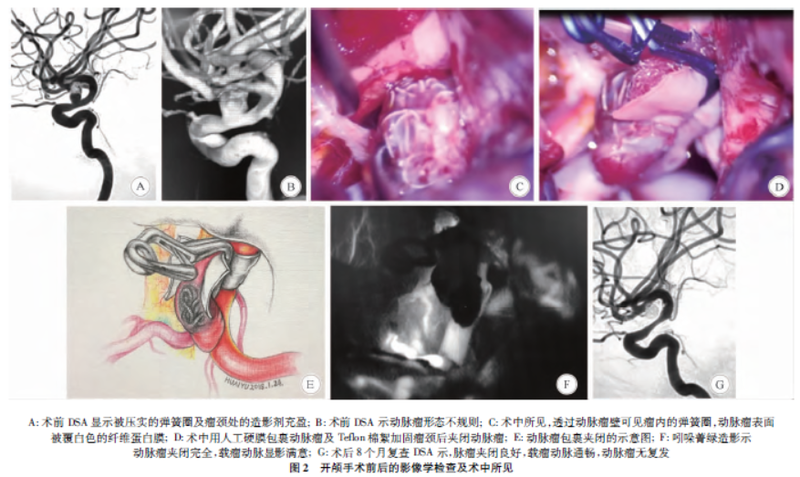
颈内动脉血泡样动脉瘤的诊治1例报告并文献复习2021-11-15 来源:临床神经外科杂志 作者:王智,尹萍,江元龙,丛宸,高雪婷,王炳昊,徐勇刚,哈尔滨医科大学第四临床医学院微创神经外科血泡样动脉瘤临床较少见,是一种极具挑战性的脑血管病变。尽管其有手术及血管内治疗多种方法作为治疗选项,但至今尚无公认的最佳治疗手段。哈尔滨医科大学第四临床医学院微创神经外科于2017年3月收治1例颈内动脉床突上段血泡样动脉瘤患者。患者先诊断为右侧颈内动脉动脉瘤行单纯弹簧圈栓塞治疗;术后1个月复查DSA诊断为血泡样动脉瘤,再行开颅动脉瘤包裹夹闭术,取得良好的效果。本研究对患者的临床资料进行回顾性分析,并结合相关文献复习,探讨血泡样动脉瘤的诊断与治疗经验。1.临床资料 1.1临床表现 患者,男,49岁;入院前7h无明显诱因,突发剧烈头痛、头晕伴恶心、呕吐,急送当地医院就诊,头部CT检查示蛛网膜下腔出血(图1A);转入我院进一步诊治。查体:意识清楚,语言流利,Hunt-Hess分级Ⅱ级,Fisher分级Ⅲ级;双侧瞳孔等大同圆、对光反射灵敏,脑膜刺激征阳性,四肢肌力V级,肌张力正常,病理征阴性。头部CTA检查示右侧颈内动脉床突上段动脉瘤(图1B);进一步行DSA检查示动脉瘤略有增大,但形态无明显变化(图1C)。 1.2血管内治疗 考虑到动脉瘤在CTA与DSA上显影的差异,结合患者当时的经济状况及对破裂动脉瘤支架辅助术后使用双抗的担心,决定先按囊性动脉瘤采用单纯弹簧圈栓塞治疗。患者全麻、全身肝素化后,将6F导引导管送入右侧颈内动脉,Traxcess14微导丝导引Headway21支架微导管越过动脉瘤颈,头端到达大脑中动脉M1段近端备用。再将Headway17微导管塑形后顺利到达动脉瘤内,依次向动脉瘤内填入MicroPlex103/6Cosmos(Microvention Company)等5枚弹簧圈后,以1.5/4的Hypersofthelical收尾,即刻DSA示动脉瘤接近完全栓塞且弹簧圈稳定,载瘤动脉通畅(图1D)。术后患者无神经功能缺失症状,出院前复查头部CTA(图1E),显示弹簧圈稳定、动脉瘤栓塞满意。尽管治疗效果满意,但仍然不能排除血泡样动脉瘤(blood blister-like aneurysm,BBA),故建议患者1个月后复查血管造影。 1.3手术治疗血管内治疗术后1个月,复查全脑血管造影发现动脉瘤内弹簧圈被压实,动脉瘤颈增大,且形态不规则(图2A、B),符合血泡样动脉瘤的诊断条件之一。鉴于血泡样动脉瘤的诊断逐步明确,结合患者的意愿及经济状况,决定行动脉瘤包裹夹闭术。术前行压颈训练,提示代偿良好。全麻后,为防止术中出血,首先在颈部显露右侧颈内动脉,预留临时阻断带。 右侧常规翼点入路,准备在硬脑膜外磨除右侧前床突;但由于脑组织张力高,而改为硬脑膜下操作,行终板造瘘释放脑脊液。终板造瘘后脑松弛良好,重新回到硬脑膜外,磨除右侧前床突,返回硬脑膜下操作。显露右侧颈内动脉前壁动脉瘤,见局部组织粘连明显,透过白色的纤维蛋白膜可见动脉瘤内的弹簧圈(图2C)。仔细分离动脉瘤周围的粘连组织,切开硬膜环,充分显露载瘤动脉近端。取生物型硬脑膜补片(商品名Ⅱ型脑膜建,广东冠昊生物技术有限公司),剪裁成0.8cm×4.0cm大小,剪裁标准应超出动脉瘤颈并且不影响其近远端的分支;将“粗糙面”朝向内侧,在眼动脉与颈内后交通动脉之间包裹载瘤动脉及动脉瘤。为防止瘤颈与载瘤动脉的分离及复发,瘤颈两侧各放置少许Teflon棉絮包裹加固,并用一标准弯形动脉瘤夹平行载瘤动脉将硬脑膜补片、Teflon棉絮及动脉瘤颈一并夹闭(图2D、E)。术中吲哚菁绿(ICG)造影示动脉瘤夹闭完全,载瘤动脉显影满意(图2F);神经电生理监测显示体感诱发电位及运动诱发电位均未见异常。术后患者无神经功能缺失症状。术后8个月,复查DSA显示脉瘤夹闭良好,载瘤动脉通畅,动脉瘤无复发(图2G);患者无神经系统症状及体征。2.讨论.2.1血泡样动脉瘤的定义及诊断 血泡样动脉瘤是指大部分位于颈内动脉床突上段无分叉部位的前壁或上壁,体积微小、基底较宽、呈半球状或尖锥状凸起的动脉瘤;其瘤壁比较脆弱且无明显的瘤颈,约占颅内动脉瘤的0.3%~1%。通常情况下,血泡样动脉瘤限于颈内动脉。然而,也有研究发现,这种类型的动脉瘤可见于Willis环周围的任何部位,特别是大脑中动脉、前交通动脉和椎-基底动脉。血泡样动脉瘤的病理基础为假性动脉瘤而非真性动脉瘤,病因可能与动脉夹层、血流动力学及动脉粥样硬化有关。血泡样动脉瘤是位于颈内动脉背侧、无分叉部位的微小、宽基底及瘤壁脆弱的动脉瘤。1969年首先由Sundt和Murphey报道。现代神经外科时代由Nakagawa等进一步描述,认为与颈内动脉分支无关的囊性动脉瘤极其罕见。虽然以往的文献对血泡样动脉瘤已有定义,但Peschillo等对血泡样动脉瘤的定义重新归纳如下:(1)动脉瘤小于3mm,24h内的蛛网膜下腔出血;(2)位于无分叉部,Willis环的近端;(3)短期内可增大;(4)动脉瘤壁脆弱,术中及术后出血率高;(5)形态上呈圆锥形或宽颈,并具有夹层或非囊状动脉瘤的外观;(6)最初的血管造影常被漏诊。 目前血泡样动脉瘤的影像学诊断标准尚无定论,马廉亭认为诊断“血泡样动脉瘤”的金标准只有两条:一为手术切除动脉瘤后病理检查证实为瘤壁菲薄的假性动脉瘤;二为直视手术中裸眼或显微镜下通过菲薄的瘤壁可看清瘤腔内流动的血液涡流。国内方亦斌等提出了6条诊断标准,(1)动脉瘤位于ICA床突上段向前方突出;(2)无分支;(3)最初动脉瘤较小(最大直径<10mm);(4)与SAH出血部位相符合的动脉瘤;(5)2周内复查血管影像(CTA、MRA、DSA)发现动脉瘤快速生长;(6)动脉瘤或载瘤动脉有不规则的壁。在具备1~4条诊断标准的前提下,符合5条或6条的任意一条即可诊断为血泡样动脉瘤;其中第5条和第6条是明确诊断的重要依据。由于血泡样动脉瘤在影像学上无诊断的金标准,仅凭影像学表现常难与呈囊状的真性动脉瘤加以鉴别。 这也是本例患者首次介入治疗时选择单纯弹簧圈栓塞治疗的原因之一,幸运的是术后没有放松警惕,而要求患者早期复查。因此,对于血泡样动脉瘤的诊断标准应适当放宽,以便做出正确的治疗选择,避免出现灾难性后果;对位于颈内动脉非分支部位的动脉瘤,宁可考虑是血泡样动脉瘤。对血泡样动脉瘤通常描述为浆果样外观,手术中裸眼或显微镜下通过菲薄的瘤壁可看清瘤腔内流动的血液涡流。也有文献报道,术中见动脉瘤仅被一层白色的纤维蛋白膜外膜和血肿覆盖。这与本例患者的术中所见有相似之处。对于血泡样动脉瘤的术中所见,随着发病时间的不同,特别是介入栓塞后一段时间的患者,其可能并非典型的浆果样外观。 2.2血管内治疗与手术治疗 颈内动脉床突上段血泡样动脉瘤无论是采用介入或手术治疗,治疗的难度均很大、风险高,是对神经外科医生的挑战。这种复杂性病变常需要多次治疗,并且再次出血的发生率极高。手术治疗和血管内治疗孰优孰劣,目前尚无定论。Peschllo等对334例血泡样动脉瘤患者(手术治疗114例、血管内治疗199例、联合治疗19例)的荟萃分析显示,治疗的效果与Hunt-Hess分级和Fisher分级有明确的关系。 对于Hunt-Hess分级≤3的患者,血管内治疗组及手术组的预后良好率分别为84.9%和70.0%;而对于Hunt-Hess分级≥4的患者,血管内治疗组与手术组的预后良好率分别为40.7%和59.1%。如果对患者Hunt-Hess分级不进行分组处理,总体的预后良好率及预后不良率:血管内治疗组分别为78.9%和21.1%,手术组分别为67.4%和32.6%。对于Fisher分级≤2的患者,血管内治疗组及手术组的预后良好率分别为88.8%和77.1%;Fisher分级≥3的患者,血管内治疗组及手术组的预后良好率分别为61.1%和61.4%。 术中血管内治疗组及手术组并发症的发生率分别为10.5%和24.1%;血管内治疗组最常见的并发症是血栓事件(33.3%)及血管痉挛(19%),手术组最常见的并发症是动脉瘤破裂出血(81.5%)。血管内治疗组与手术组的术后并发症发生率分别为21.1%和35.7%。荟萃分析结果表明,血管内治疗的致残率及死亡率似乎更低。Shah等纳入36篇文献对256例261次治疗的血泡样动脉瘤患者(手术治疗133例、血管内治疗119例及联合治疗4例)的荟萃分析显示,手术治疗的即刻动脉瘤闭塞治愈率比血管内治疗高(88.9%vs63.9%),近期随访手术治疗也优于血管内治疗(88.4%vs75.9%);而血管内治疗的并发症率比手术治疗稍低(26.2%vs27.8%),故尚无法确定哪种治疗方案具有绝对优势;作者指出,血泡样动脉瘤较为少见,治疗具有挑战性,预后差。 开颅手术可能得到较好的术后即刻和长期的闭塞率,但血管内介入治疗更为安全,并且也可能带来较好的治疗效果。治疗方法选择需结合患者的意向、动脉瘤特点和不良预后的风险效益比。 2.3血管内治疗血泡样动脉瘤的血管内治疗常采用单纯弹簧圈栓塞、单支架辅助弹簧圈栓塞、多支架辅助弹簧圈填塞、覆膜支架和血流导向装置(FD)等。目前,血管内治疗的要点在于对载瘤动脉的重建,而不是单纯的瘤内栓塞。一些栓塞技术及材料的改进,如动脉瘤栓塞时的“铆钉”技术的应用,结合金属覆盖率较高的支架,有利于载瘤动脉内膜的修复,降低了术后复发率。覆膜支架理论上在保持病变动脉通畅的情况下隔离了动脉瘤,从而达到治愈的目的;已经有很多成功的病例报道。但覆膜支架的顺应性较差,输送支架过程中牵拉容易损伤血管壁引起术中出血;另外血泡样动脉瘤的载瘤动脉血管条件复杂,支架释放后贴壁不良易产生内瘘。同时血泡样动脉瘤多毗邻眼动脉、后交通动脉及脉络膜前动脉等分支动脉;如果定位不准确,会引起支架段血管侧支的闭塞;也有可能引发明显的炎症反应导致内膜增生并致血管狭窄。因此,在血泡样动脉瘤治疗过程中,选择覆膜支架治疗需慎重考虑。FD治疗血泡样动脉瘤具有较高的有效性。闫亚洲等经筛查最终纳入14篇文献(均为病例回顾性分析研究),共115例患者(120个血泡样动脉瘤),采用单个或重叠FD治疗。结果显示:完全闭塞率为69%,复发率为13%,再出血率为8%;手术相关并发症发生率和病死率分别为29%和11%,长期预后良好率为86%。亚组分析显示,与重叠FD支架治疗血泡样动脉瘤相比,单FD支架治疗的预后更好(P=0.02);但两者治愈率和手术相关并发症发生率的差异无统计学意义(均P>0.05)。作者指出FD治疗血泡样动脉瘤是安全、有效的,单FD支架治疗的预后比重叠FD支架更好;高金属覆盖率的FD需要更加强调抗血小板治疗,但过度的抗血小板治疗可能增加出血的风险。2.4手术治疗虽然血管内治疗血泡样动脉瘤,特别是FD的应用展示了良好的发展前景,但仍需要大量的病例观察进一步证实。目前在经济欠发达地区FD的应用还受到限制,手术治疗仍然是重要的选择。手术治疗常采用开颅平行载瘤动脉直接夹闭动脉瘤,载瘤动脉缝合、动脉瘤孤立术、颅内外血管吻合后动脉瘤夹闭或孤立术及包裹加固动脉瘤夹闭术。Szmuda等对297例患者(手术117例、血管内治疗180例)的荟萃分析显示,单纯夹闭术的死亡率为12.5%,致残率18.5%,术中出血率58.3%,术后出血率12.9%;包裹夹闭术的死亡率为10.4%,致残率15.0%,术中出血率3.7%,术后出血率6.9%。血泡样动脉瘤直接夹闭常需要牺牲部分载瘤动脉,对于动脉瘤体较小、载瘤动脉条件较好、无明显动脉粥样硬化的血泡样动脉瘤,直接夹闭动脉瘤,重塑载瘤动脉的可能性是存在的。载瘤动脉缝合及搭桥后动脉瘤孤立术的操作难度相对较大,手术时间长,可作为备选治疗方式。血泡样动脉瘤包裹联合夹闭术的操作相对简单、快捷,不会造成载瘤动脉的狭窄,目前被认为是一种有效的治疗方式。包裹材料的选择目前尚无统一标准,常常是依据术者的习惯和理解。由于有包裹联合夹闭术后出现动脉瘤增大及再出血的报道,是否与包裹材料的选择有关并无定论。常用的包裹材料有人工硬脑膜补片、肌肉片及自体筋膜等,剪裁的宽度应尽量超出动脉瘤颈而不影响分支血管,长度应适度,方便操作;过长部分可在夹闭成功后适当修剪。夹闭过程中应及时调整动脉瘤夹释放的位置,避免夹闭不全或夹闭过度导致的瘤颈残留及载瘤动脉狭窄。 丰育功等曾报道2例采用自体硬脑膜包裹血泡样动脉瘤并取得成功的患者。本研究选择脑膜建是考虑其具有较好的柔顺性,0.3~0.7mm的厚度有利于包裹后充分及均匀的贴敷在血管及动脉瘤颈壁,同时其粗糙面与病变区域的接触,加之动脉瘤颈部位用Teflon棉絮加固,可加速动脉瘤颈周围的粘连,可能对预防血泡样动脉瘤的复发有效果。本例患者术后随访复查DSA显示,载瘤动脉形态稳定,动脉瘤无复发。 本研究将对其继续随访,观察长期的治疗效果。对于血泡样动脉瘤的治疗,无论是介入及手术治疗均面临极大的挑战;血泡样动脉瘤的特点决定了术中极易发生动脉瘤的破裂。因此,术前充分的评估及准备尤为重要,包括与患者家属的充分沟通。正确的诊断及侧支循环代偿情况的评估是介入及手术成功的关键。对于一些非典型的颈内动脉床突上段非分叉部位的小而无动脉瘤颈的动脉瘤,也应警惕血泡样动脉瘤的可能。DSA检查的3D和动态影像对于明确诊断及了解前交通动脉的侧支循环非常必要;术中的神经电生理监测可为术者提供有意义的信息。 依据这些信息,一旦术中动脉瘤发生破裂,可以决定临时阻断载瘤动脉的时间或是否进行颅内外血管吻合。为了尽快控制出血,本例患者在开颅术前常规显露同侧颈动脉,以备临时阻断用。通过3DDSA充分评估动脉瘤的指向非常必要,瘤顶指向外侧方的动脉瘤在分离颈动脉池的早期容易破裂;瘤顶指向上方的动脉瘤常与额叶粘连,在牵拉额叶时极易破裂,因此常需要在软膜下解剖分离、显露动脉瘤颈并安全地控制颈内动脉。瘤顶指向内侧的动脉瘤虽然早期不易破裂,但术者的视野受限,常需要应用开窗动脉瘤夹进行动脉瘤的夹闭。另外尚需要对术中有可能用于搭桥的桡动脉应用超声及Allen试验进行评估,显微吻合器械及可能用到的包裹材料都应在开颅前准备齐全。尽管手术及介入均可面临术中动脉瘤破裂的风险,但由于充分的术前准备及术中精细操作,开颅手术对术中动脉瘤破裂局面的控制较介入相对容易掌控。血泡样动脉瘤的介入治疗常需要在双抗及肝素化条件下进行;因此如术中发生动脉瘤破裂常会带来灾难性的后果。充分的术前评估及准备,选择合适的治疗策略及材料,术中轻柔操作,同样也非常重要。一旦术中出现动脉瘤破裂,患者常首先出生命体征的改变;此时需要迅速中和肝素,在无球囊导引导管的情况下可压迫同侧颈总动脉及必要的降血压处理。如果是微导管突破动脉瘤,应该保持微导管现有的位置,避免回撤,快速弹簧圈填塞于载瘤动脉外之后,缓慢回撤微导管瘤内填充,填塞的弹簧圈常为哑铃型;最后将半释放的支架完全释放覆盖动脉瘤。由于目前的微导管及弹簧圈比较柔软,另外操作医生对血泡样动脉瘤的高度重视和谨慎,术中微导管及弹簧圈刺破动脉瘤的情况极少出现;而血泡样动脉瘤的破裂常出现在操作的其他环节,包括血管造影阶段及支架释放阶段。因此,必要的球囊止血及覆膜支架补救方法,应该在术前充分考虑。介入术中血泡样动脉瘤破裂的开颅手术补救,包括直视下开颅手术夹闭及必要时的搭桥手术,但时间上往往不允许。因此,复合手术室内完成血泡样动脉瘤的处置,对于提高治疗的安全性可能具有较好的前景。本研究通过对本例血泡样动脉瘤患者的诊治过程总结分析及结合文献复习,得出以下几点经验。(1)血泡样动脉瘤的诊断应适度放宽;(2)在血管内治疗与手术治疗均获技术成功的同等条件下,术后血管内治疗患者的恢复要优于手术治疗;(3)手术治疗对术中出血等危机的处置具有优势,术中出血死亡的可能性极小;(4)对于血泡样动脉瘤的治疗选择,应采用医生最熟悉的技术,同时兼顾患者的意愿及经济状况;(5)无论采用何种血管内治疗方法,术后均需要尽早复查;(6)开颅动脉瘤包裹加固后夹闭操作简单、费用低,是治疗血泡样动脉瘤的一种有效方法;(7)血流导向装置可能具有良好的应用前景,特别是对未破裂血泡样动脉瘤的治疗。总之,颈内动脉床突上段血泡样动脉瘤是一种特殊类型的复杂动脉瘤,术前应综合考虑患者的年龄、Hunt-Hess分级、动脉瘤的指向及经济状况等因素制定治疗方案;了解血泡样动脉瘤的演变过程,充分的术前准备是手术成功的关键。 来源:王智,尹萍,江元龙,丛宸,高雪婷,王炳昊,徐勇刚.颈内动脉血泡样动脉瘤的诊治1例报告并文献复习[J].临床神经外科杂志,2020,17(05):505-510.
 王智 主任医师 哈尔滨市第一医院 神经外科94人已读
王智 主任医师 哈尔滨市第一医院 神经外科94人已读 - 精选 带你了解神经外科手术全过程
开颅手术由神经外科医生进行; 一些人接受了颅底手术的额外培训。神经外科医生可以与头颈部,耳科,眼部肿瘤和重建外科医生合作。特别是如果患者的情况复杂。 手术前会发生什么? 在医生办公室,您将与神经外科医生一起检查手术并有时间提问。签署同意书并完成文书工作,以告知外科医生您的病史(例如,过敏,药物,麻醉反应,既往手术)。手术前几天,您将进行相应的检查(例如,心电图,胸部X光检查和血液检查),以确保您在安全的情况下接受手术治疗。 重要的是,您通常至少在手术前1周停止使用所有非甾体类抗炎药(Naproxen,Advil等)和血液稀释剂(香豆素,肝素,阿司匹林,Plavix等)。此外,在手术前1周和手术后2周戒烟,忌咀嚼烟草和饮酒,因为这些活动会导致出血问题。 如果计划进行影像引导手术,将在手术前安排MRI。基准点(小标记)可以放在前额和耳后。标记有助于将术前MRI与图像引导系统对齐。基准点必须保持在原位,并且在手术前不能移动或移除,以确保扫描的准确性。 手术前一晚半夜12点后不要进食或饮水。 手术的早晨 淋浴使用抗菌肥皂。穿着刚洗过的宽松衣服,病号服统一发放。 穿平底鞋,背面封闭。 如果您有指导在手术当天早晨服用常规药物,请用少量水漱口,提前2小时。 去除化妆品,发夹,接触,身体穿孔,指甲油等。 将所有贵重物品和珠宝留在家中。 带上药物清单,包括剂量和通常服用的时间。 提前列出对药物或食物过敏的清单。 患者在手术当天早晨住院。护士将解释术前过程并讨论您可能遇到的任何问题。麻醉师会与您交谈,解释麻醉的影响及其风险。 手术期间会发生什么? 根据所治疗的潜在问题,手术可能需要3到5个小时或更长时间。 步骤1:为患者做好准备 您将躺在手术台上并进行全身麻醉。一旦你睡着了,你的头部被放置在一个3针颅骨固定装置中,该装置连接到桌子上并且在手术期间保持头部绝对静止。 .患者的头部放置在一个三针颅骨夹中,在精细的脑部手术过程中,头部绝对保持头部。沿着皮肤切口线。 如果使用图像引导,您的头部将在红外摄像机中注册,以将“真实患者”与从MRI扫描创建的3D计算机模型相关联。该系统用作GPS,以帮助计划开颅手术并定位病变。仪器由相机检测并显示在计算机型号上。 步骤2:做皮肤切口 头皮的切口区域用防腐剂制备。皮肤切口通常在发际线后面进行。使用头发保留技术,其中沿着所提出的切口仅仅2.5厘米宽的区域被剃毛。有时整个切口区域可能会被刮。 步骤3:进行开颅手术,打开颅骨 将皮肤和肌肉从骨头上抬起并向后折叠。接下来,用钻头在头骨上制作小钻孔。钻孔允许进入称为开颅器的特殊锯。与使用拼图类似,外科医生切割骨窗的轮廓。将切开的骨瓣抬起并移除以暴露称为硬脑膜的大脑保护性覆盖物。骨瓣安全地放在一边,并在手术结束时更换。 .使用称为开颅器的特殊锯切割开颅手术。移除骨瓣以显示大脑的保护性覆盖物,称为硬脑膜 步骤4:暴露大脑 打开硬脑膜以暴露大脑。牵开器可用于轻轻打开大脑和头骨之间的走廊。神经外科医生使用称为放大镜的放大眼镜或手术显微镜来观察精细的神经和血管。 .打开硬脑膜并向后折叠以暴露大脑。 第五步:纠正问题 封闭在骨头内侧,大脑不能轻易移到一边进入并修复问题。神经外科医生使用各种非常小的器械在大脑深处工作。这些包括长柄剪刀,解剖器和钻头,激光器和超声波吸气器(使用细水射流来打破肿瘤并吸取碎片)。在某些情况下,诱发电位监测用于刺激特定的颅神经,同时在大脑中监测反应。这样做是为了在手术期间保持神经的功能。 步骤6:关闭开颅术 在移除或修复问题后,移除任何牵开器,并用缝合线闭合硬脑膜。将骨瓣放回原位,用小板和螺钉固定在颅骨上。小板和螺钉保持永久性以支撑该区域,有时它们可以在您的皮肤下感觉到。可以将排水管放置在皮肤下几天以从该区域移除血液或流体。将肌肉和皮肤缝合在一起。将柔软的消毒棉垫敷料放在切口上。 .更换骨瓣并用小板和螺钉固定到头骨上。 手术后会发生什么? 手术后,当患者从麻醉中醒来时,患者将被带到恢复室,在那里监测生命体征。呼吸管(呼吸机)通常保持在原位,直到患者完全从麻醉中恢复。接下来,患者将被转移到神经科学重症监护室进行密切监测。 患者经常被要求移动您的手臂,手指,脚趾和腿。护士会用手电筒检查你的瞳孔,然后问一些问题,比如“你叫什么名字?”。 手术后可能会出现恶心和头痛。药物可以控制这些症状。根据脑外科手术的类型,可以给予类固醇药物(控制脑肿胀)和抗惊厥药物(以防止癫痫发作)。 根据手术和任何并发症,住院时间从2-3天或2周不等。
陈磊 主治医师 哈尔滨市第一医院 神经外科3432人已读 - 北京院感防控16条措施
一、加强通风消毒 1.摘除医疗机构建筑物门口处设置的防风保温隔帘,加强门急诊、病房等公共区域通风换气。 2.加强通风系统管理。使用集中空调的应关闭回风,加大新风。如出现新冠肺炎疑似或确诊病例,要立即停用集中 通风系统并进行终末消毒,采取安全替代措施保证室温。 3.医疗机构应加强各科、各室通风换气。医护人员应指导住院患者酌情开窗通风,保持空气清新。 4.严格落实消毒规范。加强发热门诊、急诊、候诊大厅、厕所和走廊、电梯等公共区域清洁消毒和病房终末消毒。 二、严格人员管控 5.严格落实体温监测要求。所有进入医疗机构的人员必须做到100%测量体温,发热人员100%进行登记并引导到发热门诊就诊。 6.严格落实就诊人员信息登记要求。督促就诊人员如实填写姓名、身份证号、在京居住地、手机号码等基础信息。 7.严格落实住院患者症状监测要求。空床较多的医院,应主动调整住院床位安排,减少多名住院者同处一室的情况。 科室要加强排查,每天上下午各为患者测量一次体温,对出现发热或呼吸道症状患者,及时组织检查诊断,发现疑似病例要立即采取隔离、报告和排查等相关措施。 8.严格落实探视人员管理要求。疫情期间,要对医院探视做出利于院感防控的调整,尽量采取视频方式探视。确需探视的,严格限定人数和时间,人数限1 人,时间控制在30分钟以内。有发热或呼吸道症状的人员,在未排除新冠病毒 感染情况下,不得安排进病房探视。 9.严格落实陪护人员管理要求。疫情期间,医疗机构应尽量减少陪护人员。因病情需要确需陪护的,应固定1 名陪 护人员,实行一患一护,做好信息登记,明确活动区域,督促其佩戴口罩、严格执行手卫生,并与患者一同开展体温和呼吸道症状监测。 10.严禁医务人员、医疗辅助人员等穿工作服进休息室、在污染区饮水、就餐,避免无防护条件下交谈。 11.严格落实全员培训要求。医疗机构应结合院感防控的普遍要求和本次疫情特点,面向卫技人员、管理人员和保安、保洁、护工等辅助人员开展全员培训,不留空白,不留死角,提高全员防控院感的技能。 三、严防院内交叉感染 12..尽量避免与他人接触。为防止医务人员因社交而将感染风险带入医疗机构,所有医务人员应主动婉拒和谢绝非必须的交往交流聚会活动,保证家人安全、同事安全、患者安全和医院安全。外地返京医务人员应主动向所在医疗机构报告,并居家隔离观察14 天。目前仍在湖北的医务人员应继续执行当地和本市有关规定,暂缓返京。 13.控制门急诊大厅等公共空间人员密度。导医和保安人员保持适宜数量,有效疏导人员,避免1 米以内近距离接触。 14.严格落实1 米线间隔要求。加强挂号、候诊、缴费、检查、取药等排队区域引导,推行电子支付方式。落实慢病 患者长期处方规定,明确诊断并需要长期用药的,按照《北京市卫生健康委员会北京市医疗保障局关于新型冠状病毒感染的肺炎疫情期间门诊开药有关问题的通知》要求执行。 15.严控人员聚集。严格控制各类人员到其他科室、部门走动,尽量使用电话、视频等方式研究部署工作、沟通解决问题。不在狭小封闭空间召开多人参加的会议。 16.严控集体用餐。落实分时段就餐,加大就餐座位间距,宜同向排列,避免面对面就餐,就餐时应尽量避免交谈交流。提倡为临床一线工作人员送餐。严格控制住院患者及陪护人员到食堂就餐的区域、时间,做到合理分区、限流。
陈磊 主治医师 哈尔滨市第一医院 神经外科4129人已读
问诊记录 查看全部
- 发现右锁骨上区神经鞘瘤术后复发1天。 患者1天前发现右锁骨上区神经鞘瘤术后复发。现在就是疼。辅检:... 希望王智老师给做手术总交流次数6已给处置建议
- 脑卒中 王主任您好。我在2019年9月19日晚因头部碰伤出总交流次数2已给处置建议
- 脑干血管瘤 脑干血管瘤总交流次数4已给处置建议
- 右侧三叉神经鞘瘤术后癫痫近十七年 患者十七年前因右侧三叉神经鞘瘤 第一,我想问问王智主任有没有更好的办法来给治疗。
第...总交流次数15
- 癫痫 癫痫接下来需要怎么做总交流次数29
总访问量 430,604次
在线服务患者 291位
科普文章 15篇








