科室医生 查看全部
科普·直播义诊专区 查看全部
- 精选 肺癌RET基因突变
2020年9月4日,美国Blueprint Medicines宣布FDA加速批准普拉替尼用于治疗成人转移性RET融合阳性非小细胞肺癌。 约同一时间,普拉替尼的中国上市申请获国家药品监督管理局受理,并被纳入优先审评。今年3月24日,普拉替尼胶囊(普吉华)正式获批上市,适应症是:用于既往接受过含铂化疗的RET基因融合阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的治疗。普拉替尼成为国内第一个治疗RET突变肿瘤的靶向药。
马德华 主任医师 浙江省台州医院东院区 心胸外科3725人已读 - 精选 原位腺癌和微浸润腺癌患者的长期预后
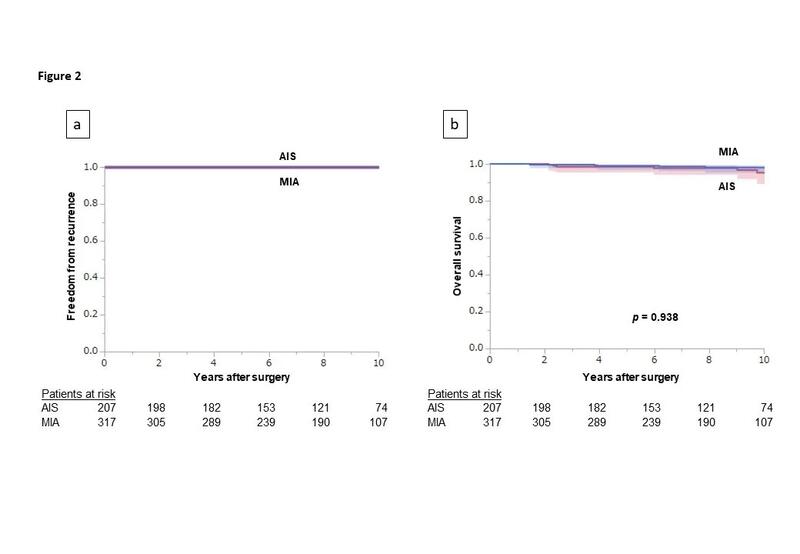
简介:WHO对肺肿瘤的分类将原位腺癌(AIS)和微浸润腺癌(MIA)定义为无组织浸润成分或组织浸润成分有限的癌症。AIS或MIA患者术后5年无复发的可能性已显示为100%。这项研究旨在分析术后5年以上的AIS或MIA患者的预后。 方法:我们回顾了1998年至2010年间4768例行肺癌切除术的患者的病理结果。其中,包括524例行AIS根治性切除术的患者(207例,占39.5%)和MIA(317例,60.5%)。此外,我们还分析了继发原发性肺癌的术后复发,生存率和发展情况。 结果:在纳入的患者中,女性为342例(65.3%),非吸烟者为333例(63.5%),肺叶切除术后为229例(43.7%)。平均病理总肿瘤直径为15.2±5.5mm。术后中位随访期为100个月(范围:1-237)。AIS或MIA病例均未观察到肺癌复发。估计AIS / MIA病例术后10年的疾病特异性生存率分别为100%/ 100%(p = 0.72),总生存率分别为95.3%/ 97.8%(p = 0.94)。术后10年异时性原发性肺癌的估计发病率分别为AIS 5.6%和MIA 7.7%(p = 0.45),且与EGFR突变状态无关。 结论:尽管应关注发展为异时性继发性肺癌的可能,但其在切除AIS和MIA后5年以上复发的风险非常低。这一发现增强了将AIS和MIA与其他肺腺癌区分开来的临床价值。 自2015年世界卫生组织(WHO)发布第四版肺肿瘤分类以来,就已经正式定义了原位腺癌(AIS)和微浸润性腺癌(MIA)。(BAC)肿瘤大小在3厘米或更小且没有任何侵袭,因此被重新命名为AIS。以前被归类为BAC混合腺癌且浸润不超过0.5 cm的肿瘤被重新命名为MIA。这些定义基于国际肺癌研究协会,美国胸科学会和欧洲呼吸学会认可的多学科小组的建议,目的是更好地了解疾病并改善患者护理。定义AIS和MIA的分类的概念是,由于AIS的组织学浸润前性质和MIA的侵入性成分有限,因此在完全切除肿瘤后,它们应具有100%或接近100%的无复发可能性。 确实,许多报告都描述了切除AIS或MIA后的良好无复发生存(RFS)状态。据我们所知,AIS或MIA手术后5年内未报告复发。但是,只有少数小型研究报告了长期(> 5年)结果。最近,美国国家肺部筛查试验显示,低剂量螺旋计算机断层扫描(CT)可以降低选定患者的肺癌死亡率。由于使用低剂量CT筛查的患病率不断上升, 包括AIS和MIA在内的分期肿瘤将被更频繁地发现。为了更好地管理AIS和MIA,评估这些类型肿瘤的手术后长期效果非常重要。在本研究中,我们旨在阐明完全切除后AIS和MIA的长期预后。 材料和方法 患者收集和组织学评估 在1998年至2010年间,在日本东京国立癌症中心医院接受手术切除的4,768例肺癌患者中,我们回顾性收集了3,170例肺腺癌患者的数据。 对于每个手术,从经支气管或经胸膜注射(处于充气状态)对切除的标本进行固定,依次切成5毫米厚的切片,并进行宏观福尔马林检查。接下来,从所选的组织块上切下连续的4 ?m厚切片,并根据需要用石蜡切片法,苏木精和曙红,Elastica-van Gieson以及高碘酸-席夫(Schiff)染色制备制备标本。 两名以上的病理学家根据世界卫生组织第四版《肺肿瘤分类》对所有适用于腺癌病例的幻灯片进行了组织病理学评估。因此,将腺癌的侵袭性成分定义为:1)除鳞状上皮以外的组织学亚型(即,乳头状,腺泡状,微乳头状和/或实体状);2)肿瘤细胞浸润肌成纤维细胞基质;3)淋巴,血管,胸膜和空域入侵;4)散布在空气空间中。AIS在组织学上被定义为小的(≤3 cm)局限性腺癌,其生长仅限于沿既有的肺泡结构的肿瘤细胞(纯粹的鳞状细胞生长),并且缺乏基质,血管或胸膜浸润。不存在腺泡,乳头状,实性或微乳头状等侵入性模式。MIA在组织学上被定义为小(≤3 cm)的孤立性腺癌,主要表现为在最大尺寸上呈血型且≤5 mm浸润。AIS和MIA的代表性组织学图如图1所示。在最大尺寸上测量了浸润的大小。当有多个病灶时,通过累加侵袭性成分的百分比并将其乘以总肿瘤直径来估计侵袭的大小。通过肉眼检查来测量肿瘤的总大小。如果肉眼检查和显微镜检查之间的大小有差异,则优先考虑显微镜检查的结果。 在排除了具有其他肺癌,同步浸润性肺癌或不完全切除的当前或先前治疗史的病例后,我们最终收集了524例,包括AIS(207例,39.5%)和MIA(317例,60.5%)。完全切除定义为所有宏观肿瘤组织的切除和显微分析后的切缘没有肿瘤细胞。在患有多个AIS或MIA的患者中,我们收集了MIA侵袭性成分最大或AIS肿瘤总直径最大的肿瘤数据。 所有临床信息均摘自患者的病历。收集患者的手术年龄,性别,吸烟习惯,肿瘤位置,手术步骤,肿瘤大小和亚叶切除术的边缘距离(如果有)。 EGFR突变评估 如果有标本,则使用高分辨率熔解分析检测到两个常见的表皮生长因子受体(EGFR)突变,即第19外显子的缺失(Ex19del)和第21外显子的密码子858的点突变(L858R)。 病人随访 我们记录了术后常规随访期间的肿瘤复发情况。随访评估包括身体检查,血液分析(包括癌胚抗原),胸部X线摄影以及胸部和腹部CT。每当患者出现提示复发的症状或体征时,都将使用脑磁共振成像,颈部,胸部和腹部的正电子发射断层扫描和/或骨闪烁显像进行进一步评估。根据这些评估结果诊断出肿瘤复发。随访一直进行到2020年3月。 放射学上,异时性继发性原发性肺癌(SPLC)的定义如下:所有结节的合并/肿瘤比(CTR)均大于0.5的多个新的肺结节被定义为初始原发性肺癌的复发性病变,而其他多个 新的肺部新结节被定义为SPLC。CTR是固体成分大小(合并)与肿瘤总直径之比。与先前手术切除的边缘分开发展的单个新结节被认为是SPLC。这些定义是基于日本临床肿瘤学小组(JCOG)进行的研究中使用的协议。 当对新的肺部病变进行组织学评估时,确定新病变是SPLC还是复发是基于两名以上病理学家对最初切除的肿瘤和新的肺部病变的比较。 统计分析 数据以均值,中位数或计数和百分比表示。为了对AIS / MIA与性别,肿瘤位置,手术程序,吸烟习惯和SPLC发生率之间的关系进行统计分析,使用了Pearson检验。视情况使用学生t检验或Mann-Whitney U检验比较AIS和MIA组中变量的平均值。使用Kaplan-Meier方法估算了总生存期(OS),肺癌特异性生存期(CSS)和无复发率以及SPLC的发生率,并使用 对数等级测试。所有测试均为双面测试,p值
 沈建飞 副主任医师 台州医院 心胸外科2901人已读
沈建飞 副主任医师 台州医院 心胸外科2901人已读 - 精选 AAH AIS MIA IAC 是什么意思
肺部磨玻璃影是肺科疾病中的一个常见名词,在今天越来越多地被提及。影像学磨玻璃结节相对应的四种病理诊断:不典型腺瘤样增生(AAH)、原位腺癌(AIS)、微浸润腺癌(MIA)和浸润性腺癌(IAC)。前两种诊断恶性程度较低,可以靠体检诊断,是早期诊断的重点。1.不典型腺瘤样增生(AAH):这是纯的磨玻璃结节,往往认为这是一种偏良性的增生结节。2.原位腺癌(AIS):纯磨玻璃密度中出现实变影在病理上就属于AIS。用大小来区分AAH和AIS,AIS一般均>5mm,AAH≤5mm, AAH和AIS个过程是连续的,从不典型增生到原位癌没有明确界限。 3. 微浸润腺癌(MIA):孤立性、以鳞屑样生长方式为主且浸润灶≤5 mm的小腺癌。CT在混合密度结节中可见到肿瘤内局部增粗血管可被强化。 4.浸润腺癌(IAC):这是一种恶性度高的肺癌。当MIA继续生长可致肺泡塌陷,形成不规则的巢状结构,间质有浸润,当浸润的实变灶>5mm或完全呈一个实性软组织密度的局灶性结节。CT增强扫描可发现分叶状实性结节可有强化或在结节边缘部分出现肿瘤微血管征,可出现胸膜凹陷征。在结节的周边还可出现细毛刺征。 对肺结节随访期间,一旦出现实性病灶,结节增大,或兼有肿瘤血管征这时,应停止随访,建议手术切除,以免延误早期肺癌的诊诊治
马德华 主任医师 浙江省台州医院东院区 心胸外科3.3万人已读
问诊记录 查看全部
- 肺结节术后1月 肺结节术后一个月突然漏气,3月14做的手术,术后3天拔管出院... 已经插管了,我就是问医生别的问题,总交流次数56已给处置建议
- 肺癌 2020年11月,体检CT上有结节,但体检报告未报告。
20... 详见病例最后部分总交流次数26已给处置建议
- 左肺上叶GGN,考虑AAH或AIS 左肺上叶GGN,考虑AAH或AIS,建议 沈医生您好。
上周去恩泽面诊过您,根据三维重建情况,...总交流次数4已给处置建议
- 三年前右肺结节手术切除, 肺结节诊断总交流次数34已给处置建议
- 肺结节 做肛周脓肿手术时候,做了肺部ct 我这个严重吗,要手术吗,多看看我的片子,我这个恶性...总交流次数36已给处置建议










