精选内容
-
关于门静脉血栓
按照Virchow三定律的原则,即血栓的形成与血管内皮损伤、血流动力学改变及血液高凝状态有关。按照这种原则,门脉海绵样变性、门脉高压是血栓形成的高危因素,并且,血管搭桥、曲张静脉结扎、脾脏切除、内镜下
郝献华医生的科普号 2024年01月28日
2024年01月28日 53
53
 0
0
 2
2
-
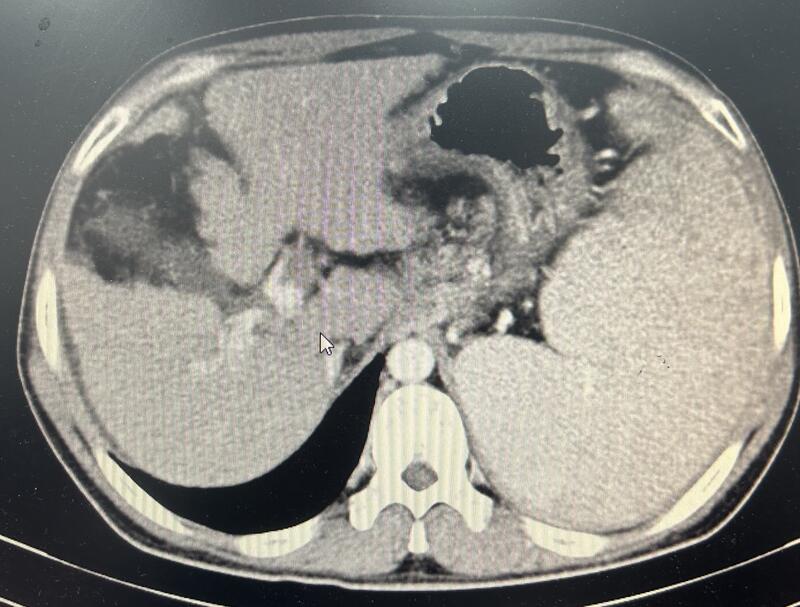
脾动脉主干栓塞联合脾微波消融治疗巨脾并门脉血栓案例分享
患者青年男性乙肝肝硬化重度脾亢门脉高压套扎治疗期间出现门脉血栓。行脾动脉主干栓塞后抗凝治疗及脾微波消融治疗。治疗后门脉血栓明显减少,继续抗凝治疗。治疗前巨脾并门脉血栓。脾动脉主干栓塞后行脾微波消融及利伐沙班抗凝治疗。脾门高密度为脾动脉主干弹簧圈。脾微波消融治疗后脾脏可见大片坏死。治疗后门脉血栓明显减少。点评:巨脾重度脾亢门脉高压并门脉血栓是临床比较难处理的情况,因为门脉高压及重度脾亢会限制我们抗凝和溶栓治疗的使用。但是如果不积极干预,门脉血栓会逐渐进展导致难以逆转并发症发生。我们采取先脾动脉主干弹簧圈栓塞降低门脉压力提高抗凝治疗的安全性后,给予小剂量抗凝治疗,同时通过脾消融进一步纠正脾亢,慢慢达到既降低门脉压力和纠正脾亢又逐渐消除门脉血栓的目的。这个方案还可以纠正脾动脉盗血从而改善肝功能,值得临床进一步尝试和验证。
 吴宇旋医生的科普号
吴宇旋医生的科普号 2023年02月15日
2023年02月15日 355
355
 0
0
 1
1
-
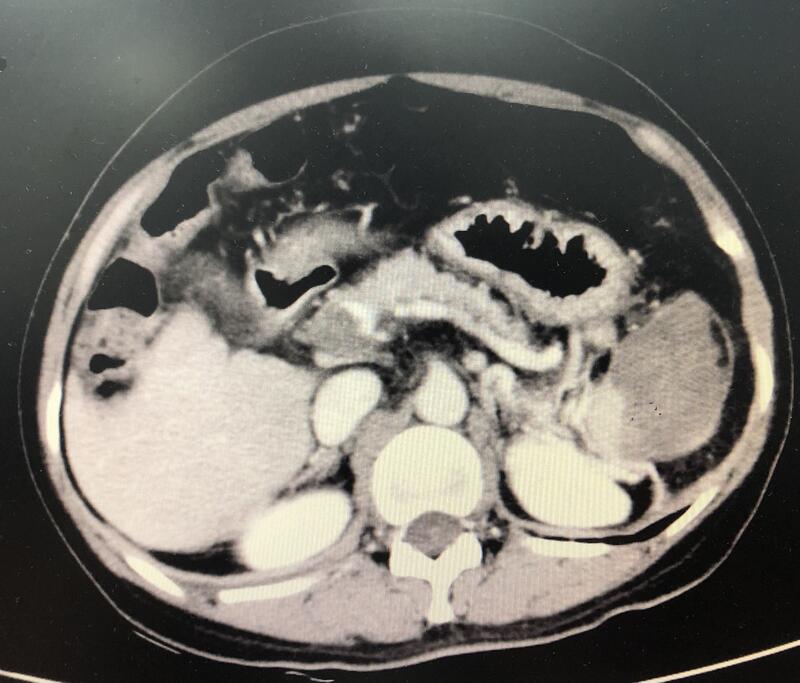
口服利伐沙班治疗门脉血栓案例分享
患者中年女性肝硬化多年,因腹胀进一步检查发现门脉血栓,内镜提示食管静脉曲张。门脉主干血栓冠状位提示门脉主干血栓堵塞约90%管腔。本拟行经肠系膜上动脉溶栓治疗,患者因为来例假暂停介入手术,先改口服利伐沙班治疗。两周复查门脉血栓基本消失。门脉血栓基本消失。提示:目前对于门脉血栓的治疗包括抗凝治疗,经肠系膜上动脉溶栓经皮经肝穿刺门脉溶栓及经tips通道溶栓均有不少报道。此案例仅抗凝就获得满意疗效,或许提示我们对于类似患者未必需要一开始就给予太多积极的介入手段干预。个人认为经肠系膜上动脉溶栓简单便宜风险较低可以作为抗凝之外的首选。经皮经肝穿刺门脉途径溶栓应该谨慎选择。tips通道途径溶栓优于经皮经肝的途径溶栓但除非合并消化道出血的患者也应该慎用。
 吴宇旋医生的科普号
吴宇旋医生的科普号 2022年09月02日
2022年09月02日 443
443
 0
0
 1
1
-
Rex手术的“前世今生”
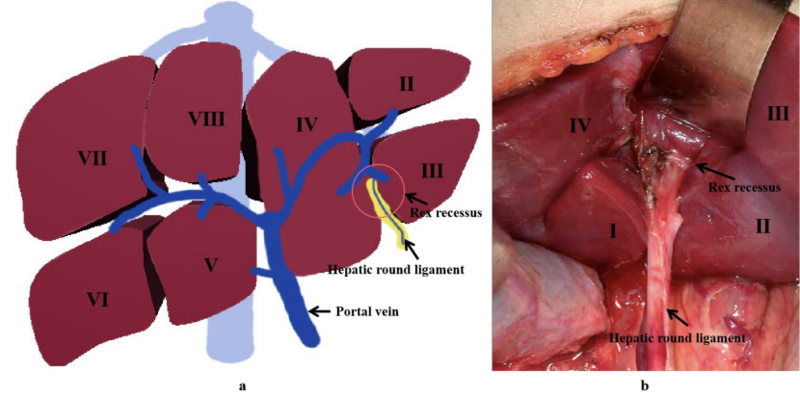
当我刚在医院工作时,如果有人问:“什么是Rex手术?”我肯定无言以对。因为在医学院教科书上根本没有这样一种术式,现在刚进医院的年轻医生,跟我当时一样,也是不知道什么是Rex手术,为什么叫Rex手术。即使我工作多年后,并且将Rex手术治疗小儿肝外门脉高压作为自己的研究方向后,我依然不明白为什么叫Rex手术。因为它的发明人不叫Rex,而是叫DeVilleDeGoyetJ。当我检索了很多英文文献后,在一篇比较老旧的文章上,我发现了“Rexrecessus”这个词所指代的意思就是Rex手术分流入肝内的部位,才明白Rex手术是以解剖部位Rex隐窝(Rexrecessus)来命名的。因此,我给它做了一个定义:Rex手术就是指通过搭桥或转位分流血管的方式,将肝外门静脉血液分流入Rex隐窝(Rexrecessus)内的肝内门静脉左支,实现门静脉血液重新分流进入肝脏的目的。其之所以被称为Rex手术是因为肝外门静脉血液分流入肝内门静脉的部位在肝脏Rex隐窝内(肝脏第III和IV段间,肝圆韧带根部,图1)。2008年我们开始在国内实施Rex手术至今已开展了14年,但Rex手术是怎么出现?又是如何发展的呢?我希望通过本文谈谈它的前世今生。1990年,deVille在比利时布鲁塞尔给3岁肝硬化女孩实施肝移植后出现门静脉血栓,他创造性的将颈内静脉作为搭桥血管,将其移植在肠系膜上静脉和门静脉左支之间治疗该部分肝移植后肝外门脉高压患者,该手术通过重建门脉血流,成功缓解了肝外门脉高压的症状。该案例被其发表在1992年的Transplantation杂志上。此后,deVille报道了采用该手术治疗肝外门静脉血栓的几个个案。1999年,deVille才在欧洲外科杂志(EurJSurg)上系统报道了该方法治疗儿童EHPVO。同年,德国移植外科医生A.M.Stenger在Chirurg杂志上将该手术方法称为MesentericoportalerRex-Shunt(deVille称其为Mesenteric-to-leftportalveinbypass)。2000年,美国移植外科医生Superina在美国小儿外科杂志(JPediatricSurg)上称该术式为Rexshunt。此后,为了方便,将肠系膜上静脉-门静脉左支分流术称为Rexshunt或meso-Rexshunt。中文翻译为Rex手术、Rex分流、Rex分流手术或肠-门分流手术。经历30年的发展,Rex手术已经经历肠-门分流术、胃-门分流术、脾-门分流术和门-门分流术的发展(图2)。因其可重建门静脉入肝血流,恢复肝脏供血的作用,Rex手术已经成为治疗儿童EHPVO的最主流手术方法。参考文献:ZhangJ,LiL.RexShuntforExtra-HepaticPortalVenousObstructioninChildren.Children.2022;9(2):297.张金山.小儿门脉高压答疑宝典.贵州科技出版社.2021,9.
 张金山医生的科普号
张金山医生的科普号 2022年07月07日
2022年07月07日 710
710
 0
0
 4
4
-
肝硬化门静脉血栓管理专家共识(2020年,上海)
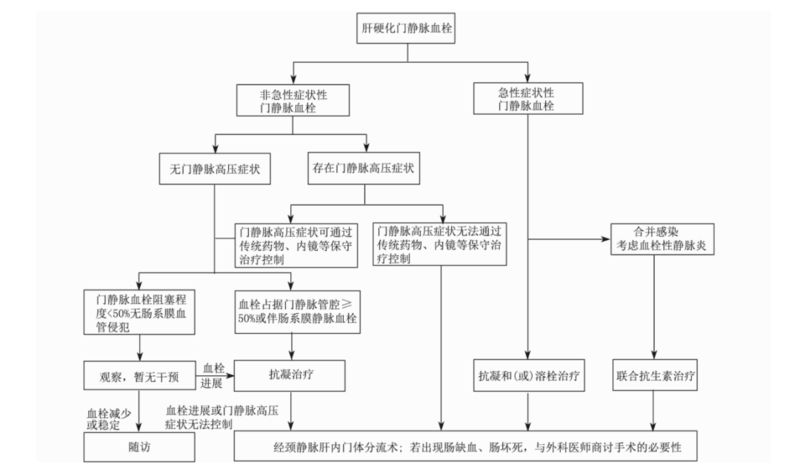
门静脉血栓(portalveinthrombosis,PVT)是指门静脉主干和(或)门静脉左、右分支发生血栓,伴或不伴肠系膜静脉和脾静脉血栓形成。急性PVT易导致肠系膜缺血,甚至肠坏死等严重不良结局;慢性PVT可导致门静脉闭塞或门静脉海绵样变性,继发门静脉高压。肝硬化患者PVT发病隐匿,常在体格检查或筛查肝癌过程中偶然被发现,需要与恶性肿瘤导致的癌栓鉴别。由于肝硬化本身存在凝血功能障碍和出血风险的矛盾,肝硬化PVT患者的抗凝治疗难以实施。尽管越来越多的研究表明抗凝治疗可促进门静脉再通,改善肝功能,但肝硬化PVT患者抗凝治疗的最佳时机和药物仍未确定。有些医院已将经颈静脉肝内门体分流术(transjugularintrahepaticportosystemshunt,TIPS)用于肝硬化PVT的治疗,但其具体适用人群有待商榷。迄今为止,国内外尚无专门针对肝硬化PVT管理的指南或共识。因此,中华医学会消化病学分会肝胆疾病学组牵头,邀请国内致力于该领域的相关专家共同参与讨论和修改,历时1年余,撰写完成本专家共识,以规范肝硬化PVT的临床诊治。本专家共识重点参考并分析样本量大且有代表性的原创性研究和meta分析结果。一、肝硬化PVT的流行病学共识意见1:PVT是肝硬化的常见并发症之一。肝硬化患者PVT患病率为5%~20%[1-2],年发病率为3%~17%[3-6]。由于不同研究纳入肝硬化患者的性别、年龄、病因、临床表现、肝功能严重程度和诊断方法各异,报道的患病率和发病率差异也较大。在2项以Child-PughA级患者为主的队列研究中,PVT的1年、3年累积发病率分别为4.6%、8.2%和3.7%、7.6%[3-4]。在另外2项以Child-PughB或C级患者为主的队列研究中,PVT的1年累积发病率分别为16.4%和17.9%[5-6]。国内多中心、回顾性研究表明,伴有急性失代偿事件的肝硬化患者PVT患病率高于无急性失代偿事件的肝硬化患者(9.36%比5.24%)[7]。这些研究结果均表明PVT是肝硬化患者的常见并发症,且与肝功能损害严重程度相关。二、PVT对肝硬化预后的影响共识意见2:PVT影响肝硬化患者预后。PVT可能增加肝硬化患者远期死亡、出血、腹水、急性肾损伤和肝移植术后死亡的风险[8-9]。临床医师需结合PVT分期、严重程度和范围评价其对肝硬化患者预后的影响。PVT和肝功能不全的严重程度是影响肝硬化患者预后的潜在因素。Senzolo等[10]发现抗凝治疗后未再通的PVT仅增高Child-PughB和C级患者的病死率;而纳入Child-PughA和B级患者的研究显示,PVT并不会增加肝硬化失代偿事件和死亡的风险[3]。因此,PVT可能主要影响肝功能较差的肝硬化患者的预后。若PVT蔓延至肠系膜静脉,将增加肝硬化患者肝移植的手术难度。三、肝硬化PVT的危险因素菲尔绍(Virchow)静脉血栓形成的三要素包括血流缓慢、局部血管损伤和血液高凝状态[11],也适用于解释肝硬化PVT的形成机制。(一)门静脉血流速度降低共识意见3:门静脉血流速度降低与肝硬化PVT风险密切相关。肝硬化患者肝内纤维组织增生、肝窦破坏、血管扭曲闭塞,导致入肝的门静脉血流速度降低。多项研究通过多普勒超声检查门静脉血流速度发现,若门静脉血流速度<15cm/s,肝硬化患者发生PVT的风险将增加10~20倍[5-6,12]。非选择性β受体阻滞剂是肝硬化门静脉高压患者最常用的药物之一,可降低门静脉血流速度,导致肝硬化PVT发生风险增加4倍[13-14]。(二)局部血管损伤共识意见4:脾切除术是我国肝硬化PVT最常见的局部血管损伤因素。腹部手术是肝硬化PVT形成最主要的局部血管损伤因素。脾切除术是国内最常用于治疗肝硬化门静脉高压和脾功能亢进的外科治疗方式[15],开腹或腹腔镜脾切除术后PVT发生率约为22%。脾切除术可导致PVT发生风险增加10倍以上[16]。因此,对食管胃静脉曲张(gastroesophagealvarices,GEV)伴脾功能亢进患者行脾切除术应特别慎重,术后需预防PVT。(三)易栓症共识意见5:遗传性易栓症可能不是我国肝硬化PVT的主要危险因素,获得性易栓症可能是部分肝硬化患者发生PVT的潜在危险因素。对于脾大但血小板计数正常或升高的肝硬化患者,建议筛查骨髓增殖性肿瘤的可能。易栓症继发于止血缺陷的遗传性或获得性血液高凝状态[17]。静脉血栓栓塞相关的遗传性易栓症的主要危险因素包括亚甲基四氢叶酸还原酶(methylenetetrahydrofolatereductase,MTHFR)C677T基因突变、凝血因子ⅤLeiden突变和凝血酶原G20210A突变、遗传性抗凝蛋白(抗凝血酶、蛋白C和蛋白S)缺乏等[18-20]。相关meta分析证实,MTHFR C677T纯合突变、凝血因子ⅤLeiden突变和凝血酶原G20210A突变与肝硬化PVT有关,而抗凝血酶、蛋白C和蛋白S缺乏与肝硬化PVT并无显著相关性[21-23]。我国汉族人群罕有凝血因子ⅤLeiden突变和凝血酶原G20210A突变,其对我国肝硬化患者PVT的影响可能非常微弱[24]。获得性因素包括骨髓增殖性肿瘤(真性红细胞增多症、原发性血小板增多症、骨髓纤维化)、抗磷脂综合征、妊娠、产后、口服避孕药、阵发性睡眠性血红蛋白尿症、高同型半胱氨酸血症等,也可能是肝硬化患者PVT的潜在危险因素[25]。尤其是伴有脾大但血小板计数正常或升高的肝硬化PVT患者,应特别注意骨髓增殖性肿瘤的可能[26]。(四)炎症共识意见6:门静脉、腹腔和肠道炎症可能是肝硬化PVT的重要危险因素。肝硬化患者常存在肠源性内毒素水平升高,其与肝硬化患者门静脉系统的凝血酶生成潜力增强有关,可导致血液高凝状态[27-28]。Huang等[29]发现,肝硬化合并GEV的患者中,PVT组的IL-6和TNF-α水平均显著高于无PVT组。四、肝硬化PVT的影像学检查共识意见7:多普勒超声是诊断肝硬化PVT的初筛影像学检查方法,增强CT和MRI检查有助于明确诊断。影像学检查可诊断和评估PVT的分期、严重程度、海绵样变性侧支血管,这与肝硬化患者的预后和治疗方法的选择密切相关。主要的影像学检查手段包括多普勒超声、增强CT、MRI和血管造影。多普勒超声操作简单、便捷,可作为肝硬化患者PVT临床筛查和评估的首选方法。多普勒超声诊断PVT的灵敏度为89%~93%,特异度为92%~99%[30]。PVT表现为管腔内高回声或等回声填充物,急性期可表现为血管腔扩张。多普勒超声还可用于测定门静脉血流速度;门静脉海绵样变性表现为门静脉周围多发小血管影。然而,多普勒超声常受到操作者诊断水平,以及腹水和气体的影响。CT和MRI检查,尤其是门静脉重建,可用于进一步确诊PVT,其对肠系膜静脉血栓和脾静脉血栓的诊断更具优势。PVT表现为门静脉管腔内充盈缺损;新发PVT在CT平扫和MRI扫描下可表现为门静脉管腔内高密度影;门静脉海绵样变性在CT增强和MRI扫描下表现为阻塞的门静脉周围有诸多细小、迂曲的侧支血管。CT检查还可评判肠缺血和肠坏死。门静脉直接或间接血管造影检查属于有创操作,目前很少用于PVT的诊断,而主要用于血管介入治疗前的评估;此外,血管造影对附壁或部分性PVT的诊断未必优于增强CT检查。五、肝硬化PVT的诊断和病情评估共识意见8:根据慢性肝病病史和典型的影像学表现,可诊断肝硬化PVT。对于影像学检查发现有PVT,但肝硬化诊断证据不足者,肝脏穿刺活组织检查是肝硬化最重要的诊断方法。需结合生物化学指标、血清甲胎蛋白水平、影像学特征和病理结果等,并注意与非肝硬化PVT和门静脉癌栓进行鉴别。(一)诊断和鉴别诊断通常根据慢性肝病病史和典型的影像学表现诊断肝硬化PVT。首选影像学检查方法为多普勒超声,增强CT和MRI检查也可确诊肝硬化PVT,并确定血栓范围。对于影像学检查有PVT表现,但肝硬化诊断证据不足者,肝静脉压力梯度测定和经颈静脉肝脏穿刺活组织检查等是重要的诊断方法。肝硬化PVT需要与非肝硬化PVT和门静脉癌栓鉴别,常可通过临床病史、影像学特征和血清甲胎蛋白水平进行初步鉴别。门静脉癌栓常表现为门静脉扩张、血栓强化、新生血管、临近血栓的肿瘤形成或血清甲胎蛋白水平>1000ng/dL;若满足以上3个或3个以上表现,则考虑为门静脉癌栓,灵敏度为100%,特异度为94%,阳性预测值为80%,阴性预测值为100%[25]。(二)病情评估1.肝硬化PVT的分期共识意见9:肝硬化PVT的分期主要包括急性症状性和非急性症状性。共识意见10:肝硬化患者发生急性腹痛,无论有无发热或肠梗阻,均应考虑急性症状性PVT可能。确定PVT分期对制定后续抗血栓治疗策略至关重要。肝硬化PVT多是在常规影像学检查评估肝硬化严重程度或监测肝癌时偶然被发现,故常难以界定血栓形成时间。本共识并不推荐根据发病时间将肝硬化PVT分为急性和慢性,而推荐根据是否存在PVT相关的临床症状进行分期。肝硬化患者若存在急性腹痛(发病初期,症状与体征不一致)、恶心、呕吐等PVT相关症状,则定义为急性症状性PVT;若无相关症状,则定义为非急性症状性PVT。建议肝硬化患者发生腹痛的时间>24h,无论有无发热或肠梗阻,均应考虑急性症状性PVT,均需进行影像学检查确诊;当伴有发热、畏寒,无论有无腹腔感染,推荐进行常规血液细菌培养。2.肝硬化PVT的严重程度共识意见11:肝硬化PVT的严重程度主要包括附壁、部分性、阻塞性和条索化。Yerdel分级是当前最常用的PVT分级系统[31],包括4个等级:①血栓占据门静脉管腔的50%以内,伴或不伴轻度肠系膜静脉血栓;②血栓占据门静脉管腔的50%以上或完全占据门静脉管腔,伴或不伴轻度肠系膜静脉血栓;③门静脉和近端肠系膜静脉完全血栓;④门静脉、近段和远端肠系膜静脉完全血栓。Yerdel分级主要用于肝移植术前评估手术成功率和术后并发症风险,对于抗血栓治疗选择的价值有待商榷。BavenoⅥ共识[32]提出了PVT评估系统,但并非专注于评估肝硬化患者,而是将恶性肿瘤、非肝硬化、肝移植术后等诸多疾病状态均考虑在内。目前,国内有学者将肝硬化PVT的严重程度分为附壁、部分性、阻塞性和条索化,这更加简易,贴近临床实践,且有助于治疗选择和预后评判。附壁PVT指血栓占据门静脉管腔的50%以下;阻塞性PVT指血栓完全或接近完全占据门静脉管腔[33];部分性PVT指血栓程度介于附壁和阻塞性之间;条索化PVT指血栓长期阻塞门静脉而发生机化,影像学检查无法探明门静脉管腔[34]。阻塞性和条索化PVT常伴有门静脉海绵样变性。3.肝硬化PVT的转归共识意见12:肝硬化PVT的转归评判主要包括新发、部分再通、完全再通、进展、稳定和复发。临床需动态观察肝硬化PVT的发生和发展,以便及时调整治疗方案。规范肝硬化PVT转归的定义有助于未来研究观察终点的标准化。根据肝硬化PVT发生及其程度的变化,转归评判的定义如下。新发指既往影像学检查提示无血栓,本次首次诊断为血栓;部分再通指血栓严重程度较前降低至少1个等级,但仍存在血栓;完全再通指原有血栓完全消失;进展指血栓的严重程度较前加重至少1个等级;稳定指血栓的严重程度较前无明显变化;复发指原有血栓完全消失后再次出现血栓。六、肝硬化PVT的治疗流程共识意见13:对于肝硬化急性症状性PVT,一旦出现肠缺血或肠坏死表现,应及时联系外科医师商讨手术的必要性。共识意见14:对于肝硬化非急性症状性PVT,可根据PVT的严重程度、范围和动态演变,酌情考虑是否采取抗凝药物治疗。肝硬化PVT是否需要治疗、何时启动治疗及采用哪种治疗方式,取决于PVT的分期、严重程度、范围,临床表现,门静脉高压并发症、出血风险,以及随访期间血栓动态变化结局等[35]。肝硬化PVT的初步治疗流程(图1)提示,急性症状性PVT应尽早启用抗凝药物治疗,以再通血管并预防血栓蔓延;急性症状性PVT经抗凝治疗无效且出现肠缺血、肠坏死表现,应积极请外科医师会诊,探讨手术的必要性和可行性;伴有GEV出血或高危GEV的肝硬化PVT患者应在控制静脉曲张后再酌情启用抗凝药物治疗;经内镜和药物治疗后GEV仍反复出血的肝硬化PVT患者应积极考虑TIPS;PVT程度<50%且血栓尚未累及肠系膜静脉的患者可随访观察,其中一部分患者的血栓可能在随访期间减轻或消失而无需抗凝药物治疗,而另一部分患者的血栓发生进展后可酌情启用抗凝药物治疗;若血栓占据门静脉管腔≥50%或伴肠系膜静脉血栓,则需考虑启用抗凝药物治疗。图1肝硬化门静脉血栓的治疗流程七、肝硬化PVT的治疗方法肝硬化PVT的治疗方法主要包括抗凝治疗、溶栓治疗和TIPS。一部分肝硬化PVT患者在未应用任何抗血栓药物或其他血管介入治疗的情况下可自发再通,即肝硬化一过性PVT[25,36],但如何准确预判此类患者尚不清楚,影像学检查随访间隔和观察时限也未明确。由于PVT再通率在很大程度上取决于从诊断到启动治疗的时间间隔,越早开始治疗再通率越高[37-38],目前仍需更多研究明确肝硬化PVT启动治疗的最佳时机。(一)抗凝治疗共识意见15:抗凝治疗的主要适应证为急性症状性PVT、等待肝移植、合并肠系膜静脉血栓形成;伴有近期出血史、重度GEV、严重血小板减少症的肝硬化PVT患者应暂缓抗凝治疗。共识意见16:肝硬化PVT患者抗凝治疗前,应进行内镜和血液学检查,充分评估出血风险。共识意见17:存在GEV高危出血风险的肝硬化PVT患者,在抗凝治疗前,建议启用非选择性β受体阻滞剂和(或)内镜下治疗进行GEV破裂出血的一级预防。共识意见18:既往有GEV破裂出血的肝硬化PVT患者,在抗凝治疗前,建议启用非选择性β受体阻滞剂和内镜下治疗进行GEV破裂出血的二级预防。尽早抗凝可有效安全治疗非肿瘤、非肝硬化急性PVT已达成共识[39-40]。肝硬化患者常存在GEV破裂出血和鼻出血等出血风险,也常伴有PT、国际标准化比值(internationalnormalizedratio,INR)明显延长和血小板计数减少等凝血异常表现。对于肝硬化PVT患者,是否需要抗凝治疗、何时启用抗凝治疗及如何应用抗凝药物均需谨慎评估风险和获益。有2项meta分析研究提示,抗凝治疗后肝硬化PVT的门静脉再通率为66%~71%,门静脉完全再通率为41.5%~53%,血栓进展率为5.7%~9%[41-42],抗凝治疗较无抗凝治疗可显著提高门静脉再通率和完全再通率,降低PVT进展率;抗凝治疗和无抗凝治疗组出血风险差异无统计学意义。队列研究提示,抗凝治疗可延长肝硬化PVT患者的生存时间,尤其是抗凝治疗后达到门静脉完全再通的患者[43-44]。然而,这些研究在选择抗凝治疗的患者时可能存在潜在偏倚,如非阻塞性PVT、凝血功能和血小板计数相对正常、既往未发生过出血、无或低风险GEV和肝功能更好的患者等。抗凝治疗的风险主要来源于高危GEV和严重血小板减少症。因此,抗凝治疗需在预防上消化道出血措施实施后启动。启用抗凝治疗前,可用非选择性β受体阻滞剂和(或)内镜下治疗预防GEV破裂出血。1.抗凝药物的适应证和禁忌证:肝硬化PVT的抗凝治疗应个体化。主要适应证包括急性症状性PVT、等待肝移植、合并肠系膜静脉血栓的肝硬化。主要禁忌证包括近期出血史、严重的GEV、严重的血小板减少症。然而,界定严重血小板减少症的阈值仍存争议;国外学者认为血小板计数<50×109/L的肝硬化患者出血风险增高[17,32],但国内有学者发现血小板计数<50×109/L的肝硬化患者采用抗凝治疗并未增加出血风险。进展期肝硬化患者,特别是Child-PughC级患者,需谨慎考虑抗凝治疗[17]。共识意见19:低分子肝素和直接口服抗凝药物对代偿期肝硬化伴PVT患者相对安全、有效。直接口服抗凝药物对于Child-PughC级肝硬化患者的安全性和疗效需进一步评估。2.抗凝药物类型的选择:抗凝药物包括维生素K拮抗剂、肝素类和新型直接口服抗凝药物。维生素K拮抗剂主要是华法林。华法林剂量达标常需密切监测INR,传统认为将INR升高至正常参考值上限的2.0~3.0倍为达标。终末期肝病患者未服用华法林时INR已较高,在肝硬化患者中如何准确监控华法林的使用尚不确定。INR会受食物、药物等因素的干扰,这也给华法林的药效评估带来了困难。肝素类药物主要包括普通肝素、低分子肝素和磺达肝癸钠。普通肝素剂量达标常需密切监测活化部分凝血活酶时间(activatedpartialthromboplastintime,APTT),传统认为将APTT升高至正常参考值上限的1.5~2.5倍为达标。值得注意的是,普通肝素可引起血小板减少症,常于应用肝素5d后出现,建议在使用后第3至10天复查血小板计数;低分子肝素发生肝素诱导血小板减少症(heparin-inducedthrombocytopenia,HIT)和出血风险低于普通肝素,常无需监测血小板计数,但肾功能不全者慎用。低分子肝素需要皮下注射,如果患者用药依从性差,可采取低分子肝素-口服抗凝药物序贯治疗。一项随机对照试验发现,低分子肝素注射治疗1个月后口服华法林5个月的抗凝治疗方案对肝硬化PVT患者安全、有效[45]。亦有研究报道,磺达肝癸钠成功治疗7例失代偿期肝硬化合并PVT患者,未发生出血或HIT等药物不良反应[46]。新型直接口服抗凝药物包括直接Ⅹa因子抑制剂(如利伐沙班、阿哌沙班)和直接Ⅱa因子抑制剂(如达比加群),此类抗凝药物的安全性和有效性可能优于传统抗凝药物[47-48],轻、中度肾功能不全者可以正常使用直接Ⅹa因子抑制剂。肝脏血管病兴趣组进行的多中心调查显示,38例肝硬化PVT患者中,最常应用的直接口服抗凝药物是利伐沙班,其次是达比加群和阿哌沙班;选择直接口服抗凝药物的原因是无需监测INR[49]。一项来自埃及的随机对照试验比较了利伐沙班与华法林治疗慢性丙型肝炎感染、因脾功能亢进行脾切除或化脓性门静脉炎后发生急性PVT、处于代偿期患者的效果和安全性[50]。利伐沙班组门静脉完全再通率(85%比45%)和部分再通率(15%比0)均显著高于华法林组,而利伐沙班组消化道出血发生率(0比43.3%)和病死率(0比36.4%)均显著低于华法林组,结果表明肝病患者PVT抗凝药物应首选利伐沙班,而非华法林。考虑到这项随机对照试验患者选择的局限性,其结论尚需更多高质量研究证实。利伐沙班主要通过肝脏代谢,适用于Child-PughA级患者,慎用于Child-PughB或C级患者。3.抗凝药物剂量的选择:深静脉血栓形成的诊断和治疗指南推荐皮下注射低分子肝素的剂量为100U/kg,1次/12h[51]。对于肝硬化PVT患者而言,各项研究报道的抗凝药物剂量包括那屈肝素5700U/d[52]、那屈肝素85U·kg-1·12h-1[53]和依诺肝素钠200U·kg-1·d-1[54]。Cui等[55]比较了皮下注射2种不同剂量(1mg/kg,2次/d;1.5mg/kg,1次/d)的依诺肝素钠治疗肝硬化PVT的疗效和安全性,结果表明2种不同剂量组间门静脉再通率和静脉曲张出血率差异均无统计学意义,但1.5mg·kg-1·d-1剂量组出血风险更高。与传统抗凝药物相比,利伐沙班为凝血因子Ⅹa抑制剂,使用时常可按固定剂量给药,无需因食物、体质量、轻度肝肾功能损害调整剂量。共识意见20:对于肠系膜静脉血栓形成或既往有肠缺血、肠坏死、等待肝移植、存在遗传性血栓形成倾向的患者,可考虑长期抗凝治疗。4.抗凝治疗疗程:BavenoⅥ共识和欧洲肝病学会临床实践指南推荐抗凝治疗疗程常为6个月以上;门静脉完全再通后仍需继续抗凝治疗数月或直至肝移植手术;对于肠系膜静脉血栓或既往有肠缺血或肠坏死、等待肝移植、存在遗传性血栓形成倾向的患者,可考虑长期抗凝治疗[32,56]。一部分肝硬化PVT患者经6个月的抗凝治疗后门静脉未再通,但继续抗凝治疗至12个月可实现门静脉再通[37]。因此,若条件允许,对于抗凝治疗6个月后PVT无明显改善的患者,可尝试持续抗凝治疗至12个月。共识意见21:抗凝治疗过程中发生出血事件,建议根据出血严重程度延缓使用或停用抗凝药物;发生消化道出血时应及早行内镜检查和治疗;发生致命性大出血时,及时使用拮抗剂,并进行红细胞、新鲜冰冻血浆、血小板输注等替代治疗。5.抗凝治疗过程中的出血管理:首先明确抗凝药物的类型、剂量和末次使用时间,完善血常规、肝功能、肾功能、凝血功能,有条件者评估血浆药物浓度,同时评估出血严重程度。轻度出血应延迟用药或停药,并进行对症治疗,调整抗凝药物的种类和剂量;发生非致命性大出血,应停用抗凝药物,并根据出血部位采用机械按压、补液、输注红细胞、新鲜冰冻血浆和血小板替代等对症治疗,也可考虑使用拮抗剂;发生消化道出血时,尽早行内镜检查,明确出血部位和原因,可按相应指南进行处置;发生致命性大出血时,应立即停药,并采取生命支持措施,使用拮抗剂对症处理[54]。共识意见22:抗凝治疗成功后定期监测门静脉通畅性,以评估血栓是否复发。6.抗凝治疗后的监测和随访:抗凝治疗达到门静脉再通后,仍可再发血栓。有研究报道,停用抗凝药物后PVT的复发率分别为27%、38%,中位随访时间分别为1.3、4个月[37,54]。抗凝治疗后3个月内仍需再次监测门静脉通畅性,以决定是否继续应用抗凝药物。(二)溶栓治疗共识意见23:溶栓治疗肝硬化PVT的疗效和安全性需要更多高质量研究证实。溶栓治疗肝硬化PVT的相关证据匮乏,故可参考深静脉血栓的治疗经验,并结合肝硬化PVT自身特点制定溶栓治疗方案。溶栓前需判断以下问题:首先要排除禁忌证,如近期大手术、近期创伤史、近期未控制的活动性出血、严重高血压、主动脉夹层等。其次是评估患者的意愿和整体情况,如年龄、营养状况、肝功能、肾功能、凝血功能等。最后再考虑适应证,溶栓治疗的最佳适应证是急性症状性PVT,伴有血浆D-二聚体水平升高,且门静脉高压症状轻,无门静脉海绵样变性。条索化PVT或广泛门静脉海绵样变性不适合溶栓治疗。溶栓治疗方式主要包括全身溶栓和局部溶栓。局部溶栓包括经皮肝穿刺、经颈静脉穿刺或肠系膜上动脉置管溶栓等。鉴于经皮肝穿刺途径的潜在出血风险,应谨慎选择[57]。溶栓治疗期间,需密切动态监测血浆D-二聚体水平和凝血功能,避免出血并发症;溶栓治疗3~5d后评估血管通畅情况;最长溶栓治疗时间≤2周。溶栓治疗后可根据门静脉再通情况和患者整体情况判断是否需要继续口服抗凝药物及其疗程。在一项意大利单中心研究中,9例诊断为近期PVT的肝硬化患者连续静脉泵入0.25mg·kg-1·d-1重组组织型纤溶酶原激活物联合皮下注射低分子肝素,最长疗程为7d;4例患者达到门静脉完全再通,4例患者门静脉部分再通,1例患者PVT稳定;无临床显著的不良事件发生[58]。经肠系膜上动脉间接溶栓或经门静脉直接溶栓可有效、安全地治疗肝硬化急性或亚急性门静脉和肠系膜静脉血栓[59-60]。一项随机对照试验也比较了经肠系膜上动脉持续泵入15000U·kg-1·d-1尿激酶与TIPS治疗肝硬化PVT的疗效差异[60]。虽然溶栓组与TIPS组的门静脉主干血栓的再通率相近,但溶栓组的肠系膜上静脉和脾静脉血栓的再通率显著高于TIPS组,且肝性脑病发生率更低[60]。鉴于溶栓治疗导致出血的潜在风险高,未来仍需更多高质量研究探讨溶栓治疗肝硬化PVT的安全性。(三)TIPS共识意见24:肝硬化PVT患者行TIPS的主要适应证包括抗凝治疗效果欠佳或存在抗凝治疗禁忌证、合并GEV出血但常规内科止血疗效不佳、急性症状性PVT合并GEV出血。TIPS开通PVT的优势为可在肝内建立门腔分流道以加快门静脉血液回流速度,使更多淤积在门静脉系统血管内的血液回流入下腔静脉,对局部血栓产生冲刷效应[61]。TIPS对肝硬化PVT患者的技术可行性已得到认可,但在肝内门静脉闭塞和门静脉海绵变性侧支血管管径细小的患者中,TIPS技术难度仍非常高。TIPS主要的适应证包括抗凝治疗效果欠佳或存在抗凝治疗禁忌证、合并GEV出血但常规内科止血疗效欠佳、急性症状性PVT合并GEV出血。对于高危GEV但未出血的PVT患者,是否可早行TIPS值得进一步探讨。我国西安、成都、北京、昆明等地的研究已报道了TIPS对肝硬化PVT的有效性和安全性数据。与传统内镜联合普萘洛尔和抗凝药物治疗相比,TIPS治疗能明显提高PVT再通率和显著降低再出血率,但对生存率无明显改善[34,62-68]。TIPS术后需警惕发生腹腔内出血和肺栓塞的可能,建议至TIPS经验丰富的医疗单位进行该手术。也应注意TIPS支架将增加未来肝移植手术难度。八、有待解决的问题1.早期识别肝硬化PVT的高风险人群有助于尽早启动预防措施,但目前尚缺少可以准确预测肝硬化PVT风险的模型。旋转式血栓弹力测定、血栓弹力图和凝血酶生成测定等可全面检测凝血功能,其在预测肝硬化PVT风险方面的价值应进一步探讨。2.及早启动治疗可增加肝硬化PVT的再通率,但一部分患者可能无需任何抗凝治疗即可达到门静脉再通。因此,应进一步明确肝硬化PVT启动治疗的最佳时机。3.抗凝治疗是肝硬化PVT最重要的治疗手段之一,但抗凝药物的种类、剂量、疗程都可能影响治疗结局。因此,应进一步优化肝硬化PVT抗凝治疗方案。4.出血是抗凝治疗期间最常见的不良反应之一。肝硬化患者存在消化道出血风险,且伴有血小板减少症。早期预测、有效监测可降低或规避出血风险,但尚缺乏特异的方法。未来研究应明确严重血小板减少症的界值以预判启动抗凝治疗的出血风险,也需探讨如何监测肝硬化PVT患者抗凝治疗过程中的出血风险。5.溶栓治疗所致的出血风险高,肝硬化PVT患者溶栓治疗期间如何规避出血相关事件是值得深入探究的问题。
 赵东锋医生的科普号
赵东锋医生的科普号 2022年05月25日
2022年05月25日 536
536
 0
0
 2
2
-
【专家论坛】杨玲:肝硬化门静脉血栓管理面临的困难与挑战原创中华肝脏病杂志
摘 要 门静脉血栓是肝硬化常见并发症,现结合近期《肝硬化门静脉血栓管理专家共识(2020年,上海)》,分析肝硬化门静脉血栓领域存在的一系列分歧,指出临床抗凝治疗面临的困难与挑战,为临床进一步探索肝硬化门静脉血栓的规范管理提供参考。 门静脉血栓(portal vein thrombosis,PVT)是肝硬化最常见并发症,发病隐匿,常在体检或肝癌筛查过程中偶然被发现 [1-2] 。不少研究结果表明 PVT 可增加肝硬化患者出血率、内镜下急性出血控制失败率、再出血率及出血后的 6 周病死率,并会明显增加肝移植的手术难度、术后并发症发生率及病死率 [1-4] 。因此,不少专家提出肝硬化 PVT 应当积极治疗 [5] 。近年来的研究结果显示抗凝、经颈静脉肝内门体分流术(transjuglar intrahepatic portosystem shunt,TIPS)可促进门静脉再通 [1,5-6] 。但由于肝硬化患者出血与血栓风险并存,且部分肝硬化 PVT 可自行消退 ;同时对抗凝导致出血等并发症风险增加的恐惧,常常导致临床医生选择不治疗肝硬化 PVT [7] 。因此对于肝硬化 PVT 患者究竟哪些人群需要治疗、何时启动治疗、选择何种方式治疗缺乏统一认识。近期中华医学会消化病学分会肝胆疾病学组基于最新的研究证据,组织国内相关专家制定了《肝硬化门静脉血栓管理专家共识(2020 年,上海)》,首次系统阐述了肝硬化 PVT 的流行病学、危险因素、影像学检查、诊断、病情评估和治疗策略,对进一步规范肝硬化 PVT 的临床诊疗实践具有重要指导意义 [1-2] ,但肝硬化 PVT 的抗凝治疗仍面临不少困惑与挑战。 1、PVT 是否影响肝硬化患者的预后 尽管不少的回顾性或前瞻性研究、荟萃分析结果显示 PVT 可能增加肝硬化患者远期死亡、出血、腹水、急性肾损伤和肝移植术后死亡的风险,但需要注意的是这些研究存在一定的缺陷 [8] :(1)研究人群的异质性大 :肝硬化 PVT 的分期、严重程度与范围对预后的影响有显著差别,但不少研究在评价 PVT 对肝硬化预后的影响时,没有根据 PVT 的分期、严重程度与范围等进行评估,在某些研究中部分或分支 PVT 病例被排除,而某些研究又将部分性和阻塞性 PVT 病例纳入 ;(2)回顾性研究为主 :尽管共识意见参考并分析样本量大且有代表性的原创性研究和荟萃分析结果,但我们需要注意这些发表的荟萃分析结果,可能是在没有随机化的情况下,将选择治疗的队列数据与未选择治疗的队列数据相结合,加剧了患者选择的偏倚风险 [9-10] 。近期来自国内的研究结果显示在急性失代偿期肝硬化患者中,PVT 的存在并不增加患者 1 年病死率 [11] 。因此未来仍需要设计良好的前瞻性对照研究进一步明确 PVT 对肝硬化患者预后的影响。《肝硬化门静脉血栓管理专家共识(2020年,上海)》提出了评估肝硬化 PVT 的分期、严重程度及转归的标准 [1-2] ,有利于在今后的研究中统一诊疗标准,克服既往研究中的缺陷,减少偏倚风险。 2. 如何早期识别肝硬化 PVT 人群 肝硬化 PVT 的风险因素除了与门静脉血流速度降低、局部血管损伤、易栓症有关外 [1-2] ,更主要与肝硬化患者的凝血功能处于不稳定、不安全的平衡有关。一方面肝硬化患者由于肝功能减退,凝血谱紊乱,表现为血小板及凝血因子减少,易于出血 ;但另一方面又存在抗凝蛋白(如抗凝血酶 III、蛋白 S 或蛋白 C)的减少,以及促凝因子(如凝血因子 VIII 或 von Willebrand 因子)的增加,尤其是 FVIII/PC 比值增高可反映肝硬化高凝状态 [12-13];同时肝硬化患者对血栓调节蛋白的抗凝作用存在抵抗性,也可增加肝硬化血栓形成风险 [14] ,再加上感染、肾功能不全等因素则进一步增加血栓形成风险。因此凝血酶原时间、国际标准化比值、血小板计数等传统的监测凝血功能的参数,对于预测肝硬化患者出血与血栓形成方面的价值非常有限 [15] 。目前尚缺乏精准预测肝硬化 PVT 风险的模型。有研究结果显示旋转式血栓弹力测定、血栓弹力图和凝血酶生成测定等可全面监测凝血功能 [16-17] ,但其在预测肝硬化 PVT 风险方面的价值还需进一步研究。肝硬化患者来自门静脉、腹腔及肠道的炎症也是增加门静脉血栓形成风险的重要因素 [1-2] 。一方面肝硬化患者常伴有高水平的肠源性内毒素,可增加门静脉系统的凝血酶生成能力与血小板的高活性,促进血栓形成 [18] ;另一方面炎症区域激活的中性粒细胞胞外杀菌网络可直接增加血栓形成风险。“上海共识意见”首次明确提出门静脉、腹腔及肠道炎症可能是肝硬化门静脉血栓形成的重要危险因素 [1] 。近期 Huang 等 [19] 、Nery 等 [20] 先后发现肝硬化 PVT 患者白细胞介素 -6 水平明显升高,并在矫正非选择性 β- 受体阻滞剂的应用、饮酒史、门体侧支循环建立、食管静脉曲张≥ 2 级、腹水、终末期肝病模型评分≥ 13 和脾大等混杂因素后,多因素 Cox 回归分析结果显示白细胞介素 -6 水平高于 5.5 pg/ml 和淋巴细胞计数低于 1.2×10? /L是门静脉血栓形成的独立预测因素 [20] 。上述研究对于早期如何识别肝硬化 PVT 风险人群有重要指导意义,未来仍需要更多的前瞻性研究以探讨肝硬化 PVT 的早期识别标志物。 3. 失代偿期肝硬化 PVT 患者是否应进行抗凝 失代偿期肝硬化患者 PVT 患病率为 8% ~ 25%,显著高于代偿期肝硬化患者(< 1%)。代偿期肝硬化 PVT 患者,促凝因子和抗凝因子之间的平衡相对稳定,而失代偿期肝硬化 PVT 患者,促凝与抗凝之间的平衡非常脆弱,是否应该进行抗凝治疗目前争议较大。赞成抗凝治疗的专家认为 :(1)失代偿期肝硬化患者体内合成的抗凝因子如蛋白 C 和 S 减少,促凝因子如 VIII 因子、凝血酶、组织因子和血管性血友病因子增加,总体导致血栓前状态 ;(2)尤其是在静脉曲张出血患者中,PVT 的存在是 5 d 治疗失败(定义为再出血、无法控制的出血或死亡)的重要独立预测因素 ;(3)尽管移植前肝硬化 PVT 不影响等待移植患者的病死率,但显著增加移植后病死率 ;(4)现有证据显示抗凝治疗不增加肝硬化患者的不良后果 :失代偿期肝硬化 PVT 患者进行抗凝治疗不仅仅促进门静脉再通,还可降低进一步失代偿率和病死率,并可能带来潜在的额外益处,如降低肠道细菌移位及促炎细胞因子水平等 [7] 。而反对抗凝治疗的专家认为 [8] :(1)目前还没有充分的证据表明抗凝治疗可导致更高的 PVT 完全再通率 :一方面肝硬化 PVT 尤其是部分阻塞患者存在较高的自发性再通率,另一方面已发表的支持抗凝治疗提高 PVT 再通率的研究存在纳入证据质量低及发表偏差的影响 ;(2)肝硬化 PVT 增加病死率和降低移植率可能只是历史上供体选择和手术技术的问题,而目前随着手术技术的进步已得到改善 ;(3)失代偿期肝硬化 PVT 患者抗凝治疗的额外风险不清楚 :现有的支持抗凝的证据主要来自代偿期肝硬化 PVT 患者,这类人群应用抗凝治疗未见出血风险增加,但在失代偿期肝硬化 PVT 患者中的风险尚不明确;(4)目前缺乏可靠的方法来评估抗凝治疗对失代偿期肝硬化患者是否有效:研究结果显示国际标准化比值、抗 Xa7 对于监测维生素 K 拮抗剂及低分子肝素的抗凝效果不可靠 , 尤其是在失代偿期肝硬化 PVT 患者中如何监测尚无可靠方法 ;同时一旦启动抗凝治疗何时停止更不清楚,有报道认为部分患者停药可能导致血栓快速再形成。因此在失代偿期肝硬化 PVT 患者中是否进行抗凝治疗,还需要更多的高质量循证医学证据。“上海共识意见”强调抗凝治疗的主要适应证为急性症状性肝硬化 PVT、等待肝移植、合并肠系膜静脉血栓形成的肝硬化 PVT 患者,尤其是对于有肝移植需求的肝硬化 PVT 患者,抗凝治疗的目标在于保持门静脉通畅,阻止血栓进展或延伸至肠系膜静脉 [1-2] 。非急性症状性 PVT 是否抗凝应进行个体化评估,可根据 PVT 的严重程度、范围和动态演变,酌情考虑是否采取抗凝药物治疗 ;而对于伴有近期出血史、重度胃食管静脉曲张、严重血小板减少症的肝硬化 PVT 患者应暂缓抗凝 [1] 。 4. 如何选择肝硬化 PVT 抗凝治疗药物 目前肝硬化 PVT 常用的抗凝药物包括维生素 K 拮抗剂、肝素及新型直接口服抗凝药物 [1] 。选择何种药物抗凝,需要根据患者的疾病阶段、严重程度、药物的经济效益比来确定。代偿期肝硬化 PVT 患者使用华法林、低分子肝素和直接口服抗凝药物通常安全有效,但失代偿期肝硬化 PVT 患者存在凝血酶原时间、国际标准化比值延长,血小板减少,如何监测药物的安全性是临床面临的困境,同时失代偿期 Child-Pugh C 级肝硬化患者应用直接口服抗凝药物的安全性和疗效尚需进一步评估 [1] 。因此未来仍需加强如何早期预测、有效监测肝硬化 PVT 抗凝治疗中的出血风险 , 旋转式血栓弹力测定、血栓弹力图和凝血酶生成测定能否作为有效的监测与评估手段尚需更多的证据。 5. 如何确定肝硬化 PVT 抗凝治疗的疗程 关于肝硬化 PVT 抗凝治疗的疗程仍存在争议,比较一致的共识是肠系膜静脉血栓或既往有肠缺血或肠坏死、等待肝移植、存在遗传性血栓形成倾向的肝硬化 PVT 患者,需要长期抗凝治疗 [1-2] 。但对于上述情况以外的非症状性肝硬化 PVT,启动抗凝治疗获得门静脉再通后需要继续抗凝治疗多长时间、停药的指征是什么,尚未达成共识 ;对于抗凝治疗后门静脉未再通的患者,抗凝治疗多长时间可确定为抗凝无应答,亦缺乏相应的证据 ;对于抗凝治疗成功后的病例停药后是否会复发也需要定期监测。因此进一步探索抗凝治疗的疗程,明确停药指征,亦是临床肝硬化 PVT 抗凝治疗过程中亟待解决的问题。 参考文献 [1] 中华医学会消化病学分会肝胆疾病学组 .《肝硬化门静脉血栓管 理专家共识(2020 年 , 上海)》[J]. 中华消化杂志 , 2020, 40(11): 721-730. DOI: 10.3760/cma.j.cn501113-20201112-00612. [2] Xie WF, Wang JY, Liu YL, et al. Consensus for management of portal vein thrombosis in liver cirrhosis(2020, Shanghai)[J]. J Dig Dis, 2021. DOI: 10.1111/1751-2980.12970. [3] Amitrano L, Guardascione MA, Manguso F, et al. The effectiveness of current acute variceal bleed treatments in unselected cirrhotic patients: refining short-term prognosis and risk factors[J]. Am J Gastroenterol, 2012, 107(12): 1872-1878. DOI: 10.1038/ajg.2012.313. [4] Cerini F, Gonzalez JM, Torres F, et al. Impact of anticoagulation on upper-gastrointestinal bleeding in cirrhosis.a retrospective multicenter study[J]. Hepatology, 2015, 62(2): 575-583. DOI: 10.1002/hep.27783. [5] Han GH, Qi XS, He CY, et al. Transjugular intrahepatic portosystemic shunt for portal vein thrombosis with symptomatic portal hypertension in liver cirrhosis[J]. J Hepatol, 2011, 54(1): 78-88. DOI: 10.1016/ j.jhep.2010.06.029. [6] Lv Y, Qi XS, He CY, et al. Covered TIPS versus endoscopic band ligation plus propranolol for the prevention of variceal rebleeding in cirrhotic patients with portal vein thrombosis: a randomised controlled trial[J]. Gut, 2018, 67(12): 2156-2168. DOI: 10.1136/ gutjnl-2017-314634. [7] To UK, Garcia-Tsao G. PRO: patients with advanced cirrhosis and portal vein thrombosis should receive anticoagulation[J]. Clin Liver Dis, 2018, 12(3): 74-79. DOI: 10.1002/cld.717. [8] Mancuso A. Controversies in the management of portal vein thrombosis in liver cirrhosis[J]. J Clin Med, 2020, 9(12): 3916. DOI: 10.3390/jcm9123916. [9] Rank KM, Lake J. CON: anticoagulation for portal vein thrombosis in advanced cirrhosis[J]. Clin Liver Dis, 2018, 12(3): 80-82. DOI: 10.1002/cld.713. [10] Loffredo L, Pastori D, Farcomeni A, et al. Effect of anticoagulants in patients with cirrhosis and portal vein thrombosis: a systematic review and meta-analysis[J]. Gastroenterology, 2017, 153(2): 480-487. DOI: 10.1053/j.gastro.2017.04.042. [11] Zhang Y, Xu BY, Wang XB, et al. Prevalence and clinical significance of portal vein thrombosis in patients with cirrhosis and acute decompensation[J]. Clin Gastroenterol Hepatol, 2020, 18(11): 2564- 2572.e1. DOI: 10.1016/j.cgh.2020.02.037. [12] Tripodi A, Primignani M, Lemma L, et al. Evidence that low protein C contributes to the procoagulant imbalance in cirrhosis[J]. J Hepatol, 2013, 59(2): 265-270. DOI: 10.1016/j.jhep.2013.03.036. [13] Sinegre T, Duron C, Lecompte T, et al. Increased factor VIII plays a significant role in plasma hypercoagulability phenotype of patients with cirrhosis[J]. J Thromb Haemost, 2018, 16(6): 1132-1140. DOI: 10.1111/jth.14011. [14] La Mura V, Tripodi A, Tosetti G, et al. Resistance to thrombomodulin is associated with de novo portal vein thrombosis and low survival in patients with cirrhosis[J]. Liver Int, 2016, 36(9): 1322-1330. DOI: 10.1111/liv.13087. [15] Northup PG, Garcia-Pagan JC, Garcia-Tsao G, et al. Vascular liver disorders, portal vein thrombosis, and procedural bleeding in patients with liver disease: 2020 practice guidance by the American association for the study of liver diseases[J]. Hepatology, 2021, 73(1): 366-413. DOI: 10.1002/hep.31646. [16] Kumar M, Ahmad J, Maiwall R, et al. Thromboelastography-guided blood component use in patients with cirrhosis with nonvariceal bleeding: a randomized controlled trial[J]. Hepatology, 2020, 71(1): 235-246. DOI: 10.1002/hep.30794. [17] Shamseddeen H, Patidar KR, Ghabril M, et al. Features of blood clotting on thromboelastography in hospitalized patients with cirrhosis[J]. Am J Med, 2020, 133(12): 1479-1487.e2. DOI: 10.1002/ hep.30794. [18] Carnevale R, Raparelli V, Nocella C, et al. Gut-derived endotoxin stimulates factor VIII secretion from endothelial cells.Implications for hypercoagulability in cirrhosis[J]. J Hepatol, 2017, 67(5): 950-956. DOI: 10.1016/j.jhep.2017.07.002. [19] Huang XQ, Fan XW, Zhang R, et al. Systemic inflammation and portal vein thrombosis in cirrhotic patients with gastroesophageal varices[J]. Eur J Gastroenterol Hepatol, 2019, 32(3): 401-405. DOI: 10.1097/MEG.0000000000001526. [20] Nery F, Carneirod P, Correia S, et al. Systemic inflammation as a risk factor for portal vein thrombosis in cirrhosis: a prospective longitudinal study[J]. Eur J Gastroenterol Hepatol, 2020. DOI: 10.1097/MEG.0000000000001982.
杨玲医生的科普号 2021年04月15日
2021年04月15日 1566
1566
 0
0
 1
1
-
如何预防和治疗脾切断流术后门静脉系统血栓?
脾切断流术后由于有血管盲端的形成、血小板的增高、血管断端血管内膜的损伤等等因素,门静脉系统形成血栓的几率非常高,尤其是在脾静脉残端部位,术后短期内血栓形成几率能达到90%以上。脾切断流术后门静脉系统血栓形成几率虽高,但是血栓严重程度一般较低,导致的危害一般不大。门静脉形成的大部分血栓都为血管内膜上的附壁血栓,很少有完全堵塞血管影响门静脉血流的。而且血栓形成早起都是较为疏松的结构,就算是堵塞整个血管的血栓,血流不会被完全截流。术后早期血栓形成后若不及时的抗凝祛聚治疗,血栓会加重,有可能堵塞门脉系统的分支或者主干,导致肝脏门脉供血减少影响肝脏功能,而且还会导致胃肠道血液回流障碍,门静脉系统压力增高,有可能会再次诱发食道胃底曲张静脉破裂出血。在我们中心,对于脾切断流术后的患者我们一般术后不给凝血药或者少给凝血药,术后早期应用低分子肝素抗凝治疗,出院后3-6月之内坚持抗凝治疗(低分子肝素钙、阿司匹林、氯吡格雷等),个人经验是术后出院早期单用低分子肝素钙,后期单用阿司匹林或者氯吡格雷。从临床随诊患者复查的CT结果看,规范抗凝治疗后患者术后3-6月,门脉系统血栓大部分可消失。脾部分切除断流术是在脾全切除断流术基础上发展起来的,由于保留了部分脾脏极其血管的流入道及流出道,减少血管盲端的形成,在血流动力学因素上大大减少了门脉系统血栓形成的因素,所以脾部分切除断流术本身就能起到减少门静脉系统血栓形成的几率。
张鹰医生的科普号 2020年10月26日
2020年10月26日 2663
2663
 0
0
 0
0
-
脾(部分)切除断流术后门静脉系统为什么会形成血栓?
门脉高压症患者行脾(部分)切除断流术后有一个非常核心的问题需要引起患者及医生的重视,那就是术后门静脉系统血栓的形成。术后门静脉系统形成血栓的主要原因来源于两个方面,一方面是脾被全切或者部分切除后,脾静脉残端会成为一个没有血流或者部分没有血流的盲端,这个盲端由于没有血流流动会形成血栓。这个非常好理解,就跟河流一样,如果某段河流水不流动了,那么水中的固体渣质就会沉积下来形成淤泥。血管里头的血流跟河流的机理差不多。这个是血流动力学方面的因素导致血栓形成的原理,也是血栓形成的主要因素。其次就是术后血小板的增高,尤其是脾全切除术后血小板升到比正常值高很多的时候,血管中血小板容易积聚形成血栓。脾全切除与脾部分切除术后门静脉系统血栓形成的几率是不一样的。脾全切除术后脾静脉残端形成血栓几率非常高,但是门静脉主干、左右分支及肠系膜上静脉等部位血栓形成几率会低很多。脾部分切除术后由于留下了部分脾脏及其血管的流入道流出道,所以脾部分切除患者脾静脉内还是有回流入门静脉的血液流动的,该回流血液流量及流速与残留脾脏大小及其供血管道直径大小直接相关。有血液流动的血管不容易形成血栓,脾部分切除患者在血流动力学方面能够大大减少血栓的形成。同时由于剩余有部分脾脏,使得术后患者血小板水平能够基本维持在正常水平,不至于太高,也减少了血小板的积聚,减少血管内血栓的形成。
张鹰医生的科普号 2020年10月06日
2020年10月06日 3764
3764
 0
0
 1
1
-
脾切除术后如何预防血栓

 张瑞医生的科普号
张瑞医生的科普号 2019年11月24日
2019年11月24日 2439
2439
 1
1
 0
0
-
肝癌伴有门静脉癌栓是不是就不能手术,?

 张友磊医生的科普号
张友磊医生的科普号 2019年05月28日
2019年05月28日 16599
16599
 0
0
 30
30
相关科普号

吴宇旋医生的科普号
吴宇旋 主任医师
深圳市人民医院
介入科
226粉丝41.3万阅读

汪名权医生的科普号
汪名权 副主任医师
安徽医科大学第一附属医院
介入科
27粉丝5.7万阅读

姜在波医生的科普号
姜在波 主任医师
中山大学附属第三医院
介入科
592粉丝3.1万阅读
-

 推荐热度5.0幺立萍 副主任医师西京医院 消化内科
推荐热度5.0幺立萍 副主任医师西京医院 消化内科胃癌 37票
食道癌 35票
贲门失弛缓症 34票
擅长:各种消化系统疾病的诊断治疗,擅长肝硬化食管胃底静脉曲张出血内镜下套扎、硬化及组织胶止血治疗,食管良,恶性狭窄扩张、支架植入治疗,贲门失弛缓症内镜POME术,食道,胃,肠道粘膜下肿瘤内镜切除STER术,消化道早期癌ESD,胃肠息肉EMR等多项内镜微创手术。 擅长消化道各肿瘤化疗,消化性溃疡 ,慢性萎缩性胃炎,各种肠病的治疗。 -
 推荐热度4.9李建军 主任医师北京佑安医院 肿瘤微创介入中心
推荐热度4.9李建军 主任医师北京佑安医院 肿瘤微创介入中心肝硬化 11票
门静脉高压症 9票
擅长:擅长对肝癌、肺癌等实体肿瘤的射频消融、微波消融、氩氦刀冷冻消融、化学消融,以及梗阻性黄疸、布加综合征、肺栓塞、下肢静脉血栓等疾病的介入治疗,另擅长门静脉高压(反复消化道出血、顽固性腹水、肝窦阻塞综合症)的TIPS治疗;肝脏等疾病的影像诊断。 -
 推荐热度4.9张金山 副主任医师首都儿科研究所附属儿童医院 普通(新生儿)外科
推荐热度4.9张金山 副主任医师首都儿科研究所附属儿童医院 普通(新生儿)外科门静脉高压症 6票
小儿门静脉海绵样变性 4票
皮肤肿瘤 1票
擅长:小儿门脉高压、腹腔肿瘤(肝母细胞瘤、神经母细胞瘤;胰腺肿瘤)、先天性巨结肠、小儿胆道闭锁、胆总管囊肿、胰腺炎、肛门闭锁,单孔腹腔镜手术,Rex手术治疗门脉海绵样变。小儿外科所有常见病,多发病及罕见病的诊治。




