就诊指南
发表者:胡志伟 人已读
F1000Research 2018,7(F1000 Faculty Rev):498 Last updated:26 APR 2018
室间隔治疗的最新进展
本文就室间隔缺损(VSD)的治疗进行综述。VSD有几种类型:膜周型,流出道型,流入道型和肌部型。VSD需要治疗的适应症是中到大的VSD伴左心房和左心室增大或者肺动脉高压升高(或两者兼有),以及肺循环与体循环血流量之比大于2。传统外科手术修补适用于大的膜周型VSD,流出道型VSD,VSD合并主动脉瓣脱垂。而大的肌部VSD采取微创经皮介入封堵手术。过去多种类型的封堵器被应用于VSD封堵手术,多数在开展临床试验研究中,但目前Amplatzer肌部VSD封堵器是唯一经过美国食品药品监督管理局(FDA)批准用于临床的封堵器。一种微创杂交经心室封堵技术可用于小婴儿的大肌部VSD的封堵治疗,及时干预以阻止肺血管阻塞性疾病(PVOD)的肺动脉高压的发生对这些婴儿是有益的。
引言
室间隔缺损(VSD)是最常见的先天性心脏病,占到先天性心脏病中20到25%。VSD最常见的分类是基于它们在室间隔上的定位,而分成为膜周型(定位于主动脉下区域的膜部间隔),流出道型(位于肺动脉下区域的圆锥间隔),流入道型(缺损定位于后间隔),以及肌部型(定位于室间隔的肌部和心尖部)。膜周VSD室最常见的,约为80%,流出道VSD为5-7%,流入道VSD为8%,肌部VSD为5-20%。VSD缺损按直径的大小分为大、中、小。大部分缺损是单一的,多个缺损可以出现在肌部,描述成”瑞士奶酪“样VSD。
VSD的大小很难精确描述,主要是根据婴儿期心脏超声检查报告大致确定,小VSD其直径小于3毫米,中VSD3-5毫米,大VSD是6-9毫米,很大VSD大于10毫米。有时采用VSD直径与主动脉直径之比来表示,小VSD是直径小于主动脉直径33%,中VSD是33-75%主动脉直径,大VSD是大于75%主动脉直径。
经过VSD的左向右分流会导致左心室和左心房的扩大,在新生儿期由于有较高的肺阻力,所以这种分流并不表现出临床症状。随着肺小动脉的成熟,肺循环阻力就会下降而出现左向右分流量的增加而才出现呼吸急促,生长发育迟缓等症状。在中到大的VSD的患儿中会出现右心室和主肺动脉和分支的扩大。在大的VSD,如果不修补可能会在18到24个月时发展成为阻塞性肺血管病导致严重肺动脉高压形成。
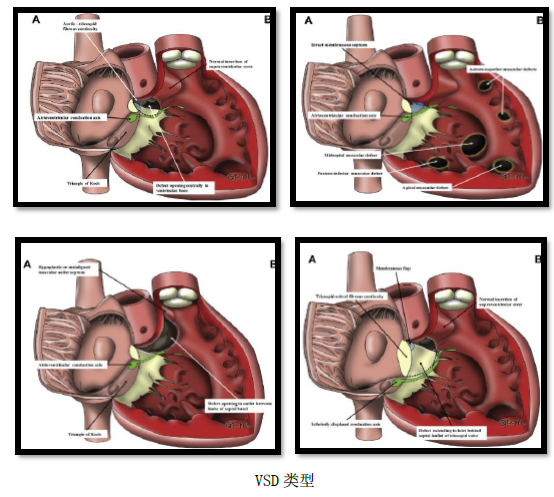
VSD干预是的指证
VSD干预的指证很大程度上取决于VSD的大小和类型。
小VSD的修补是没有必要的,对于父母的建议是保证随访和预防亚急性细菌性心内膜炎,就是注意局部炎症的积极的治疗,特别是口腔牙齿和咽部炎症的预防,防止菌血症的发生。如果VSD变小,是由于主动脉瓣叶脱垂到VSD中导致的VSD变小,会出现主动脉瓣关闭不全,需要积极地外科修补和悬吊主动脉瓣叶,这种情况常见于膜周部和流出道VSD。
中VSD如果充血性心力衰竭(父母可以观察到呼吸急促,心跳过速,呼吸困难和(或)反复肺部感染)存在,应该治疗。在生长发育迟缓,明显左心房和左心室扩大或者肺动脉压升高(或两者兼而有之),一般建议修补VSD。另外一个标准是右心导管检查肺循环血流量与体循环血流量的比值大于2(在中国很少做这有创的检查)。
大VSD中右心室收缩压和肺动脉压接近左心室压和主动脉压时,应当关闭该室间隔缺损。大多发生时间在6至12个月(当然不迟于18个月),无须考虑心脏衰竭的控制和合适的体重而行干预治疗。这个建议的原因是为了预防不可逆性肺动脉高压。在唐氏综合症的婴儿中,修补应尽可能在六个月内进行,因为这些患儿比非唐氏婴儿更容易发生肺动脉高压。在目前的实践中,首选的是外科修补不同于早期先行肺动脉环缩术然后再手术修补VSD,是一种过去常见方法。可是,这种分期方法可以考虑用来治疗肌部瑞士奶酪样多发性VSD,因为在低体重的小婴儿外科修补可能会增加心脏传导阻滞的发生。
VSD合并肺动脉高压大多数权威人士建议,在肺血管阻力升高的情况下,肺血管阻力指数小于6Wood,或者肺动脉对全身血管阻力比小于0.35,或者当肺循环与体循环量比大于1.5(或两者兼而有之),则积极干预VSD。在肺血管阻力较高时,需要做肺血管反应试验,吸氧或一氧化氮(NO),如果肺血管阻力指数降至6-8Wood以下,这些病人应积极VSD修补。VSD大、肺血管阻力严重升高的患者(即:不可逆肺动脉高压)不适合VSD修补,这些患者最终可能成为肺移植的候选者。
干预的方法
VSD的治疗,在很大程度上取决于它的大小和病人的临床症状。
药物治疗
中至大VSD患儿,若出现充血性心衰症状应积极治疗,措施包括地高辛、利尿剂(速尿)以及减轻后负荷药物(血管紧张素转换酶抑制剂:卡托普利/依那普利等)。地高辛在婴儿和儿童的充血性心衰治疗中是有作用的。当长期给药速尿时,要加螺内酯以保钾的效果。对这些婴儿优化营养,保持充足血红蛋白水平,并积极改善呼吸系统症状应成为全面管理的一部分。
适当的药物治疗可以改善临床症状,这种改善可能与VSD自发性闭合或缩小、右心室流出道梗阻发展、或肺血管阻力增加等有关。仔细的临床和超声心动图随访评估,必要时进行心导管检查,以确保这种改善不是与肺血管阻力升高有关。VSD修补应在18个月内进行,防止不可逆性肺血管阻塞性病发展。
大VSD合并严重肺动脉高压(不可逆肺动脉高压)时VSD是不能关闭了。最近出现的肺血管扩张剂(前列环素类药物,西地拉非,波生坦)的使用能够明显地改善临床症状。心房穿刺建立心房间通道,减轻严重肺动脉高压症状,可能最终需要行肺移植术。
尽管为防止严重肺动脉高压的努力是极其重要的,但应认识到40%VSD自动闭合以及另外25-30%的VSD会变得较小,而不需要干预。肌部VSD往往比膜周部缺损更容易闭合。小VSD很可能比大VSD更容易闭合(60%比20%)。临床实践证明,即使在婴儿期出现充血性心衰或者大VSD需在婴儿期行肺动脉环缩术的VSD也可能会自行闭合,且大多数VSD闭合发生在两年内,有时这个自行闭合的过程持续到儿童期,青春期,甚至成年。当决定推荐手术或经导管关闭VSD时应该考虑到这种情况。
外科修补
1950年代随着体外循环技术的发展,Lillehei和Kirklin成功修补VSD,外科修补技术得到很大发展。大多数膜周VSD通过右房切口采用Dacron补片修补,流出道VSD通过肺动脉切口修补。VSD合并主动脉瓣关闭不全,尽管缺损很小,为了防止主动脉瓣关闭不全的发展也应该尽早修补。VSD合并中到重度主动脉瓣关闭不全时,需要同时悬吊主动瓣叶或者主动脉瓣成形术。
小肌部VSD可能自发闭合而不需要手术。尤其是婴儿,大肌部VSD,特别是“瑞士奶酪”肌部VSD,很难从右心室侧来修补。对小婴儿(不超过3个月的婴儿)早期为了控制充血性心衰和降低肺动脉压力而采取肺动脉环缩术,等待儿童期通过左心室切口来修补室间隔缺损。此时,肺动脉缩带被除取,恢复肺动脉恢复正常血流。早期手术者发现,许多行肺动脉环缩术患儿肌部VSD自行闭合了,需再次开胸取掉环缩带。目前发明了可吸收的肺动脉环缩带,该环缩带减少肺动脉血流和压力,减轻了充血性心衰的症状。当VSD自行闭合后,该环缩带被吸收掉,并不需要另外的外科手术取出。
结果
外科修补VSD是安全的,总体死亡率低于3%。长期随访其结果是很好。常见是右束支传导阻滞,较少见残余分流,心脏传导阻滞或者窦房节功能障碍。偶尔肺动脉高压,以及进行性主动脉瓣关闭不全。VSD修补术后,正常左心室功能,左心室大小和重量随着也恢复正常。
微创经皮VSD封堵术
微创经皮封堵VSD是Rashkind在20世纪70年代初首次报道在动物模型成功使用钩状、单盘和双盘的雷氏封堵器。后来,其他心脏病学专家也效仿Rashkind双盘动脉导管未闭封堵器,Rashkind的VSD双盘封堵器。大部分封堵器是双盘装置和要求室间隔边缘牢固。因此,只能用于封堵肌部VSD和远离主动脉瓣的膜周部VSD。较常见的膜周VSD由于缺损靠近主动脉瓣边缘,不可能采取微创封堵术。在为了应对这一挑战,该装置被重新设计为左心室盘近主动脉瓣端是边缘较短(0.5毫米),而另一端的设计较长(5.5毫米)的非对称样封堵器,称为Amplatzer膜周VSD封堵器,应用于小到中的VSD,获得在美国FDA许可,正处于临床试验阶段。该手术的常见并发症是在安置时合随访期间出现完全性房室传导阻滞,引起对该封堵器使用的合理性的关注。



膜周VSD非对称封堵器
Amplatzer膜周VSD封堵器是依靠腰部的张力支撑在VSD边缘。挑选时封堵器的大小要大于VSD,传导束就在室间隔缺损边缘,封堵器会对传导系统产生压力,这也是产生心脏传导阻滞的机制。完全性传导阻滞的发生率波动很大从1-22%,许多需要安置永久起搏器。然而外科修补发生完全性阻滞发生率率是1%。因此,微创导管介入封堵膜部VSD缺乏其合理性。建议说该封堵器经过重新设计,使其边缘柔软或柔软施加在传导系统上的压力少或没有。然而,据作者目前所知,还没有这样的理想的改进。
目前大多数VSD封堵器都有动物实验结果,随后在当地审查委员会如CR Mark(在欧洲),FDA(在美国)批准下正在进行人体临床试验。许多VSD封堵器展示其可行性、安全性、和有效性。然而,目前,只有Amplatzer肌性VSD封堵器已获FDA批准临床使用。
应用Amplatzer肌性VSD封堵器VSD封堵术在1-119例患者单一中心的报告,在术后第二天看到有一定程度的残余分流存在。可是,在多中心临床研究中,24小时后完全封堵率在是47%,6个月增加到70%,12个月增加到92%。并发症包括一过性完全性左束支传导阻滞和节性心律,完全性房室传导阻滞(需要安置临时性和永久性起搏器),心包填塞导致死亡,心脏穿孔,封堵器引起血栓栓塞,封堵器移位需要外科移除,封堵器引起严重溶血(有些导致肾功能衰竭)和死亡等。可是,这些并发症是罕见的。
微创(经心室)杂交VSD封堵术
在小婴儿肌部VSD经皮微创封堵和外科修补术有其限制和风险,一种杂交的方法,也被称为微创经心室介入封堵技术引入,该技术的可行性在动物实验的模型和小婴儿VSD成功地实施。
报道了一系列微创杂交手术在闭合膜周部和肌部VSD的早期治疗结果,从6到408名患者,封堵器成功封堵率82%到100%,不成功封堵者是转为传统的开胸手术修补。残余分流不显著,并发症很少,偶尔有心包积液发生。
目前一项涉及408名膜周型VSD患者研究中,平均年龄3.1±1.7年(年龄范围5个月至15岁,体重4.5至26公斤),393例(96.3%)成功封堵。使用的封堵器设备类似于Amplatzer肌部VSD封堵器,由中国上海合金材料有限公司在制造。213例(54.2%)为对称性封堵器,180例(45.8%)为非对称性封堵器。随访3个月至2年没有残留分流,封堵器位置稳定,没有新的主动脉瓣关闭不全发生。
在一项来自欧洲的多中心回顾性研究中,报道21例肌部VSD杂交封堵术,89%成功封堵,余下患者因为心律失常、封堵效果不佳或其他缺损而需取出封堵器。平均随访1.4年,仅1例有轻微分流,没有其它并发症发生。这种杂交技术特别对对患肌部VSD小婴儿有帮助,与年长的孩子相比较,该类小婴儿经皮封堵会有较高的不良事件发生率。
微创经皮封堵与外科手术比较
在一项对比研究中,微创经皮封堵852例与1326例常规手术修补术相比较。手术成功率和主要并发症发生率是相似的。然而,轻微并发症的发生率(6.4%vs 0.6%)及输血需求(10.3%vs 0%)和住院时间(12.9天vs 3.2天)手术组明显高于微创经皮封堵组,作者认为,微创经皮封堵手术是一种有效的、合理替代外科手术治疗VSD的方法。
在另一项研究中,微创经皮封堵和外科手术治疗膜周室间隔缺损,结果相对比,1312例经皮封堵与1822例外科修补,经皮封堵组年龄比外科修补组高(平均年龄12.2 vs 55岁),但是缺损大小相似。手术成功率,严重并发症发生率(如需要再次手术,死亡,永久性起搏器安置),在随访期间残余分流,重度主动脉瓣和三尖瓣反流,严重房室传导阻滞等都是相似的,但外科修补组具有较多输血和长住院时间。作者的结论是,经皮封堵和外科修补膜周室间隔缺损具有相似的手术成功率,经皮封堵并没有表现出更高的瓣膜关闭不全发生率和房室传导阻滞率。
微创杂交经心室封堵手术与外科修补相比较
49例微创杂交经心室封堵与41例手术修补手术相比较,年龄上是相似的,但外科修补组VSD稍大(6.03 vs 5.03mm)。主要的并发症,即死亡,严重瓣膜功能不全,严重残余分流,致命性心律失常在两组均未发生。两组手术后早期和随访期间完全闭合率相似。但在手术组输血量和在重症监护室治疗时间均较杂交组高。作者认为微创杂交经心室封堵手术可能是一种替代外科修补的方法。
尽管作者对以上研究都做了大量不同手术方式组间的比较工作,但是所有的研究都是回顾性和非随机对照的,其结论可能不像作者认为那样,具有权威性而让我们相信。此外,还应注意到上述比较研究并不完全相同患者年龄群体,所以存在选择偏差。同时使用封堵器也是存在选择偏差,因为只有理想的候选对象使用合适的封堵器,以及还有更多复杂的室间隔缺损。此外,作者没有考虑到在体外循环下修补手术需要一段时间呼吸功能恢复和长的重症监护时间。
当考虑对VSD干预时,许多VSD都小于5mm和肺循环与体循环学血流量之比小于2。微创经皮介入封堵手术的适应证应该如同外科手术治疗一样严格掌握。此外,疾病自然历史研究表明VSD发生自发闭合持续发生在儿童时期,青少年时期,和成年。不论干预方式如何(传统的外科手术、经皮封堵手术还是杂交手术),儿科内科医生和儿科心脏病专家应该成为“过于积极干预者的看门人”,有时候心脏外科医生和介入心脏病专家认为“小”的室间隔缺损,可以不严格按照VSD干预的指证标准。
外科手术修补仍然是大的和非限制性膜周部VSD主要治疗选择。及时干预来预防肺血管阻塞性病变是非常重要的,也是儿科医生和儿科心脏病专家的职责范围。微创经皮封堵闭合大的肌部VSD是一个有价值的选择。在小婴儿大的肌部VSD微创杂交经心室封堵也是一个不错的选择。特别是在小婴儿具有瑞士奶酪样肌部VSD,最初姑息性肺动脉环缩术,后期再关闭VSD很可能对这些婴儿是有益的。
本文是胡志伟版权所有,未经授权请勿转载。 本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅
发表于:2019-02-07