 三甲
三甲
RET融合阳性在非小细胞肺癌中的治疗价值
肺癌作为常见的恶性肿瘤,其治疗方式的改进一直是大家关注的热点,伴随靶向时代的到来,彻底改变了部分肺癌的治疗格局,对伴有驱动基因阳性的患者采取个体化的靶向治疗成为共识,使得部分肺癌患者的预后得以改善。
目前非小细胞肺癌患者除检测表皮生长因子受体(epidermal growth factor receptor, EGFR)、间变性淋巴瘤激酶(anaplastic lymphoma k inase, ALK)、肉瘤致癌因子– 受体酪氨酸激酶(C-ros oncogene 1 receptor tyrosine kinase,ROS1) 等驱动基因突变外, 规范地检测转染重排原癌基因(rearranged during transfection proto-oncogene, RET)也日渐被大家所重视。
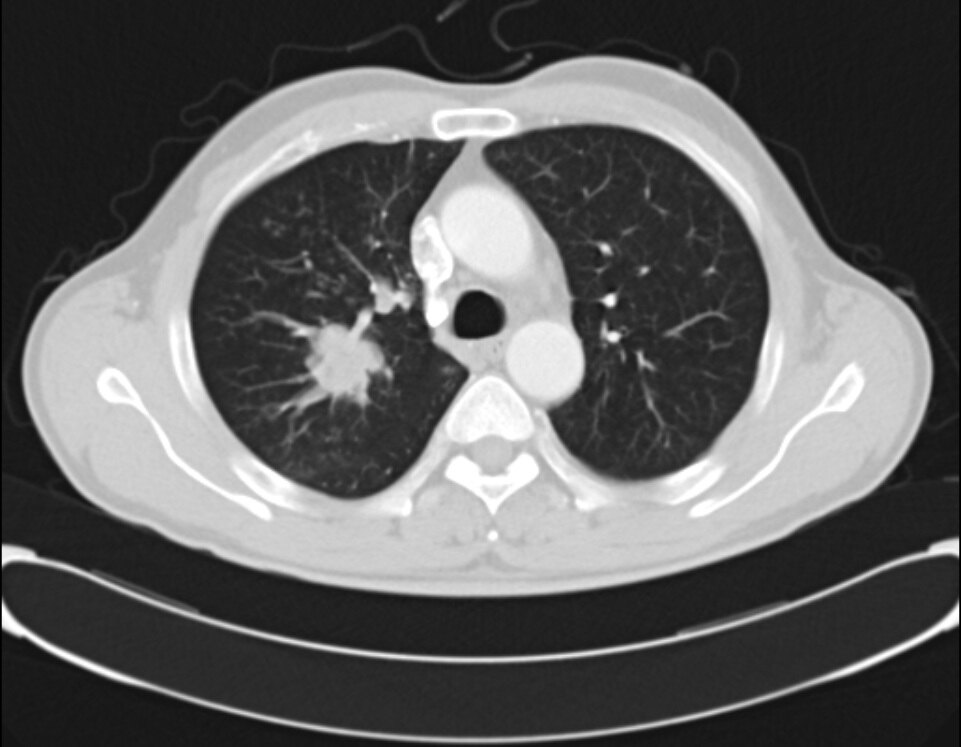
RET融合是在2012年被鉴定为NSCLC的一种新的致癌基因改变,目前共确定了RET中的48个独特的融合伙伴,其中KIF5B-RET 是最常见的融合形式,其次为CCDC6-RET、NCOA4- RET。2个新的融合伙伴CCNYL2和TRIM24对EGFR 酪氨酸激酶抑制剂(tyrosinase inhibitor,TKI)具有耐药性。在经过大量临床资料整理总结发现,RET 融合在不吸烟或轻度吸烟、年轻肺腺癌患者中较常见,且RET融合与其他致癌驱动基因相互排斥。
在NSCLC中RET融合发病率为1%–2%。在无其他致癌驱动突变的NSCLC患者中,RET融合的发病率约为5%。高选择性RET抑制剂问世之前,RET 融合阳性NSCLC在含铂类的双药化疗方案、非选择性的多激酶抑制剂。特异性RET抑制剂 的应用,并且在国内外的临床研究中均显示出了出色的疗效,RET融合阳性NSCLC患者在不同治疗方向上都有了最新进展。
近年来靶向治疗、免疫治疗等成为新辅助治疗的“ 新星”, 为局部晚期NSCLC新辅助治疗提供了新思路。对于非小细胞肺癌已有部分研究证实了新辅助靶向治疗对ALK 、ROS 1 等驱动基因阳性NSCLC的有效性。对于罕见突变的肺癌患者, 1例RET融合阳性的NSCLC患者在应用普拉替尼( pralsetinib) 完成新辅助治疗后, 成功地将不可切除的肿瘤转化为可切除的肿瘤, 术后病理结果显示,原发肿瘤中有26%的肿瘤细胞存活,淋巴结内未见残留的肿瘤细胞, 普拉替尼杀伤肿瘤细胞的有效率达74%。除此之外,该新辅助治疗后肿瘤微环境也发生了变化, 新辅助后M 1 型巨噬细胞(macrophage,M)比例上调,而CD8+肿瘤浸润淋巴细胞(tumorinfiltrating lymphocytes,TILs)数量和程序性死亡分子配体-1(PD-L1),表达水平显着降低。从目前的新辅 助治疗前后对比来看,普拉替尼也许会改变RET融合阳性患者的肿瘤微环境,若我们在此病例中继续探究TILs与PD-L1表达降低的机制并寻找相关靶点抑制剂联合普拉替尼形成利于抗肿瘤治疗的免疫微环境的证据,可能会得到增强抗肿瘤效果的结论。通过该病例报道表明了普拉替尼作为新辅助治疗策略的可行性,为未来探索RET阳性NSCLC新辅助治疗领域开启了新思路。
对于晚期RET融合阳性非小细胞肺癌,普拉替尼(pralsetinib)是一种高选择性、强靶向性的酪氨酸激酶抑制剂,能够靶向包括V804守门 员突变在内的RET融合和突变,与其他酪氨酸激酶抑制剂相比该分子对野生型RET激酶结构域的效力高出 8至28倍。根据ARROW研究[32]公布的结果,普拉替尼治疗RET融合阳性NSCLC的疗效是令人惊喜的。87例既往接受过治疗患者在后线治疗中口服普拉替尼治疗,客观缓解率(objective response rate, ORR) 为61 %, 缓解持续时间( duration of response,DoR)长达22.3个月,中位无进展生存期(progression-free survival,PFS)达17.1个月。在初治的患者中ORR更高达70%,完全缓解率达11%,中位PFS为9.1个月。塞帕替尼( selpercatinib) 是一种ATP竞争性小分子RET激酶抑制剂,可以靶向RET融合、点突变和某些获得性耐药突变(包括RETV804L/M和M918T耐药突变)。在全球性的LIBRETTO-001试验[35]中,纳入144例RET阳性NSCLC患者接受塞尔帕替尼治疗, 其中105例为既往接受过铂类药物化疗的RET融合NSCLC成人患者组,ORR可达到64%, 中位DOR长达17.5个月,中位PFS达16.5个月;39例 为初治患者,ORR达到85%,中位随访时间为7.4个 月,中位DOR及中位PFS尚未达到。最常见的3级及 以上不良反应发生率依次为高血压(14%)、转氨酶升高(13%)、低钠血症(6%)、淋巴细胞减少(6%)。
RET基因检测方式的多样选择及精准靶向RET抑制剂的出现都为RET融合阳性NSCLC患者的预后和生存带来了希望。与既往治疗相比,RET抑制剂具有持续的抗肿瘤活性、更少发生耐药突变等优势,开辟了RET驱动肿瘤的精准治疗新时代。
作者:刘政呈
南京鼓楼医院心胸外科
副主任医师,医学博士,硕士研究生导师,江苏省科教强卫工程医学青年人才
毕业于上海交通大学,美国胸心外科学会(AATS)Graham奖获得者,约翰. 霍普金斯医院访问学者
单孔胸腔镜技术及剑突下胸腔镜手术入选美国胸心外科学会年会,在大会发布研究成果及手术视频
从事胸外科临床、科研、教学工作十余年,主刀手术数千例,长期致力于肺部结节及纵隔病灶的诊治、胸外科精准微创手术技术及快速康复研究,对于肺癌、纵隔肿瘤的手术治疗有深刻见解,重症肌无力的综合诊治技术领先。
擅长单孔胸腔镜肺部手术,经剑突下单孔胸腔镜胸腺切除术,复杂肺癌、胸腺肿瘤的外科手术及综合治疗。
门诊时间:周五全天(南京鼓楼医院本部),周三上午(南京鼓楼医院江北院区)
可在微信小程序“鼓楼医院互联网医院”上预约挂号
美国胸外科医师协会(STS)国际会员International Member
美国外科医师学院(ACS)Fellow
国际肺癌研究协会(IASLC)Member
国际胸腺协作组(ITMIG)Member
江苏省医学会胸外科学分会纵隔学组委员
江苏省医师协会微无创医学专委会青年委员
中国抗癌协会纵隔肿瘤专业委员会会员
中国卓越外科科研协作组成员
中华医学会胸心血管外科分会会员
江苏省青年医学人才
美国胸心外科学会(AATS)Graham奖获得者
约翰. 霍普金斯医院访问学者(Johns Hopkins Hospital Fellow)
《中国胸心血管外科临床杂志》中青年编委
《BMC Surgery》Peer Reviewer
《Mediastinum》Section Editor
本文是刘政呈版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论