
宫腔菌群影响胚胎着床的研究进展
文章摘要:宫腔微生态失调与女性生殖健康密切相关。宫腔内乳杆菌丰度降低及特殊致病菌丰度增加可诱导宫腔内免疫失调,进而导致疾病以及妊娠失败,严重危害育龄期妇女的生殖及心理健康。
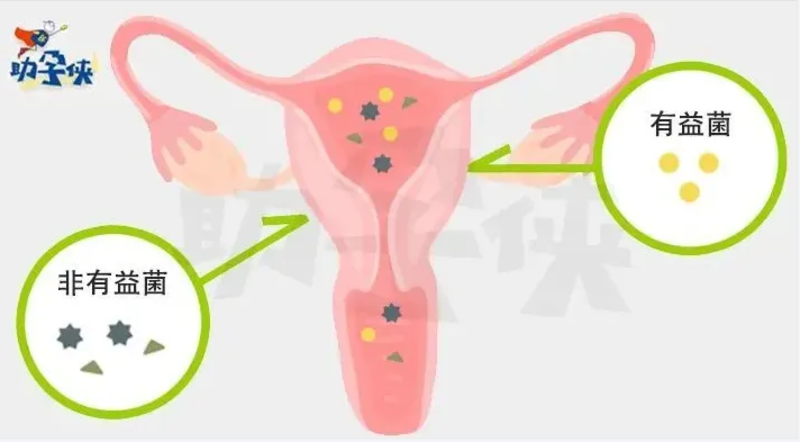
人类微生物群影响生理、疾病和代谢生殖。由于阴道的自净作用、宫颈口的关闭以及宫颈黏液栓的作用,传统观点认为宫腔内是一个“无菌环境”。但近年随着16S核糖体核糖核酸(16SrRNA,是细菌核糖体30S小亚基的组成部分之一)测序技术和微生物组学的发展,宫腔内存在微生物菌群定植已得到广泛认可。多数研究认为,宫腔微生物来源于阴道菌群的上行传播,宫腔微生物与阴道菌群存在相关性,是以乳杆菌为主导 (Lactobacillus -dominatedmicrobiota)的菌群且宫腔微生物的状态和组成易受月经周期、激素、饮食和运动等因素影响。
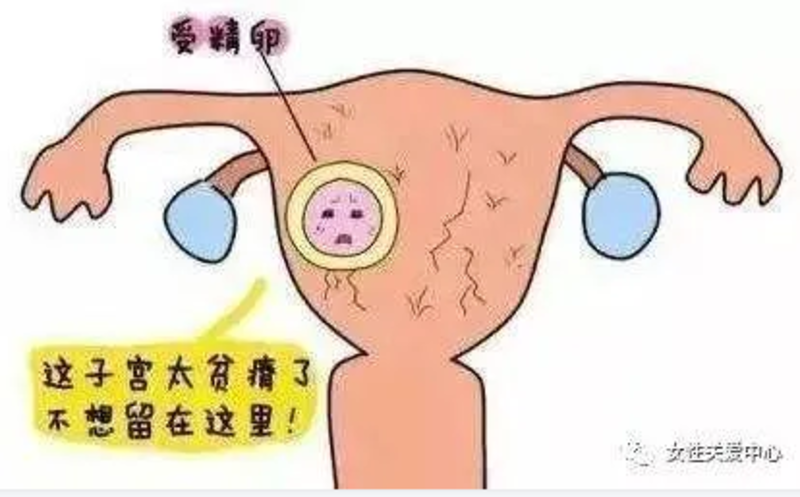
当宫腔微生物组成改变、致病菌丰度增加时,细菌毒素分泌增多、细胞因子分泌、宫腔微环境改变,趋化免疫细胞导致免疫紊乱,目前已知宫腔内免疫细胞参与母体螺旋动脉重塑进而影响绒毛外滋养层的迁移,如果生殖道微生物群在妊娠前改变而引起炎症及免疫反应,这将显著影响子宫内膜容受性以及正常胎盘初始化形成的能力。子宫内膜微生物在胚胎着床、妊娠维持中的作用机制尚不清楚 。目前认为可能机制有:①免疫调节。有研究认为子宫内膜微生物使得子宫免疫细胞发生了适应性的改变 。子宫内膜组织定植的拟杆菌可引起循环系统中 CD4+ Th1 细 胞 的 增 加,Th1细胞比例增加,介导妊娠早期滋养细胞凋亡导致胚胎毒性。有研究显示内膜中共生微生物能诱导和引起调节性 T 细(regulatory T cells,Tregs 细胞) 的聚集。Tregs 细胞分泌抑制性细胞因子如 IL-10、IL-35发 挥 免 疫 抑 制 作 用 ,对 妊 娠 维 持 具 有 重 要 的 作 用。子宫内膜微生物可能通过影响内膜各种免疫细胞的比例及免疫反应,介导母-胎之间的对话。②内膜微生物可能直接与子宫内膜相互作用调节炎症因子表达,进而影响子宫内膜蜕膜化过程及胚胎种植。③子宫内膜共生微生物竞争抑制,阻止致病微生物黏附于内膜组织。最常见的定植微生物是乳杆菌,乳杆菌形成弱酸性环境,分泌过氧化氢、细菌素、类细菌素等抑制致病微生物生长。此外,微生物菌群的代谢物和相关酶产生的复合物可以通过影响滋养层细胞的迁移与血管重构,进而干扰子宫内膜与胚胎间相互作用的协同性。
宫腔微生态失调与女性生殖健康密切相关。宫腔内乳杆菌丰度降低及特殊致病菌丰度增加可诱导宫腔内免疫失调,进而导致疾病以及妊娠失败,严重危害育龄期妇女的生殖及心理健康。但目前的研究多集中在疾病发生后宫腔微生态失调及失调后微生物组成中,这就导致了各研究在研究对象、取样方式、细菌检测方法等的选择上存在一定程度的差异,因而无法对现有的宫腔微生物结果进行汇总分析而得到宫腔核心微生物群。因此,进一步探讨健康人群宫腔核心微生物群落以评估宫腔微生物紊乱,探究不同疾病与其独特菌群组成间的关系,微生物组可以作为一种新的生物标志物,并可能在基于益生菌/益生元和子宫微生物组移植的个性化医疗中发挥作用,以提高接受性,从而最终有助于女性生殖系统的健康。
本文是李冉版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论