 三甲
三甲
成人低风险甲状腺微小乳头状癌主动监测的适应症和策略:日本内分泌外科协会关于甲状腺微小乳头状癌管理工作
介绍
甲状腺癌的发病率在世界范围内迅速增加。这种增加通常归因于在广泛采用超声检查 (US) 和 US 引导的细针穿刺细胞学 (FNAC) 等成像方式后,小甲状腺乳头状癌 (PTC) 的检出率增加。以前仅在尸检时才检测到小的 PTC。甲状腺癌死亡率保持稳定。因此,人们越来越担心小 PTC 的过度诊断和过度治疗 。
自 1990 年代以来,Kuma 医院和癌症研究所医院 (CIH) 两家日本机构就低风险 (T1aN0M0) 甲状腺微小乳头状癌 (PTMC) 进行了主动监测 (AS) 的前瞻性临床研究 。这些研究显示出有利的结果:(1) 癌症生长率和淋巴结转移 (LNM) 的新出现率较低;(2) 没有因肿瘤生长或新的 LNM 接受手术的患者出现危及生命的复发或死于甲状腺癌;(3) 在 AS 期间没有患者发生远处转移或死于甲状腺癌 。
基于这些发现,2010 年日本内分泌外科医师协会和日本甲状腺外科学会(这两个协会合并到于 2018 年成立了现在的日本内分泌外科协会 [JAES]) 。2015 年,该管理策略被美国甲状腺协会管理指南视为成年甲状腺结节和分化型甲状腺癌患者的替代管理策略 。
AS 作为全球低风险 PTMC 的可接受管理选项已获得一定程度的共识。事实上,根据 2018 年对 JAES 成员机构的调查,当时 53.8% 的低危 PTMC 成年患者在这些日本机构中接受了 AS。然而,许多医疗保健提供者仍然对在现实世界中提供 AS 存在各种担忧。因此,由 JAES 创建的 PTMC 管理工作组就 AS 的适应症和策略产生了目前的共识声明,以促进对诊断为低风险 PTMC 的成年患者实施这种管理替代方案。
方法
JAES 管理 PTMC 工作组的成员由 JAES 董事会任命,成员包括 11 名内分泌/甲状腺外科医生、1 名头颈外科医生、1 名内分泌学家和 1 名甲状腺疾病病理学家。作为共识方法,我们根据工作组采用了修改后的名义小组流程。
相关临床问题是在工作组成员的意见下创建的。使用搜索引擎(PubMed、Cochrane 图书馆和 Ichushi web)搜索了截至 2019 年 6 月的英语和日语相关文献,并进行了额外的手动搜索。我们确定了六项关于成年低危 PTC 患者中 AS 的临床研究。表格1) 但没有发现随机研究比较立即手术和 AS 之间的结果。这些陈述是根据尽可能多的科学证据做出的;在缺乏证据的情况下,根据成员的共识决定,至少目前认为适当的原则是适用的。证据分级被认为不适合目前的共识声明。
表格1。
低危甲状腺乳头状微小癌患者主动监测的临床研究
作者,国家,年份 患者人数 随访时间(月) 肿瘤增大(≥3 mm) 肿瘤体积增加 (>50%) 淋巴结转移的发展
伊东,日本,2014 ( 8 ) 1235 平均,60共 4.6% ND共 1.5% 4.9%/5 年 1.7%/5 年 8.0%/10 年 3.8%/10 年
日本福冈,2016 ( 15 ) 409平均值,81.6共 6.0%ND 共 1.0%6.3%/5 年7.3%/10 年
塔特尔,美国,2017 ( 16 ) 291个中位数,25共 3.8%12.4% 0% 2.5%/2 年11.5%/2 年12.1%/10 年24.8%/5 年
韩国,2018 ( 17 )370中位数,32.5 3.5% 23.2% 1.4%
哥伦比亚萨纳布里亚,2018 ( 18 )57个中位数,13.33.5% ND ND
莫利纳罗,意大利,2020 ( 19 )93 中位数,19 2.1%16% 1.1%
说明:a包括直径 10-15 毫米的甲状腺乳头状癌患者。
ND,没有数据。
诊断和决策
AS 的适应症和 PTMC 的立即手术
PTMC 定义为最大直径≤10 mm 的PTC。AS 的候选者是患有低风险 PTMC 的成年患者。表 2显示了那些适合手术的 PTMC。具有临床 LNM、远处转移(尽管非常罕见)和侵犯邻近器官(特别是气管和喉返神经 [RLN])等高危特征的 PTMC 应立即手术,如有指征应给予术后放射性碘治疗.
表 2。
无需主动监测的甲状腺微小乳头状癌立即手术的指征
1. 存在临床淋巴结转移或远处转移(罕见)
2. 临床上明显侵犯 RLN 或气管
3. 细胞学诊断侵袭性甲状腺乳头状癌亚型(罕见)
4. 肿瘤附着于气管,可能侵犯
5. 位于 RLN 过程中的肿瘤
6. 伴有其他需要手术的甲状腺或甲状旁腺疾病
7. 年龄 <20 岁(无当前证据)
RLN,喉返神经。
当预防性清扫颈部各区时,甚至在临床淋巴结阴性的 PTMC 中,不仅在中央区而且在侧颈中也以相当高的比率检测到显微 LNM。然而,根据接受 AS 的患者的结果,这种微观转移在临床上变得明显的比率似乎很低。在出现临床 LNM 后进行的转换手术是成功的,而且不会影响患者的预后。
此外,FNAC 特征提示 PTC 的侵袭性亚型,例如高细胞变异,建议立即手术,尽管缺乏直接证据,而且仅根据 FNAC 怀疑此类亚型在实践中不容易诊断。郭等人。研究了 18,260 个常规 PTMC 的手术病例,发现了 97 个 PTMC 的高细胞变体和 90 个 PTMC 的弥漫性硬化变体 。研究人员还发现,与传统 PTMC 相比,PTMC 的弥漫性硬化变体具有甲状腺外延伸 (ETE) 和 LNM 的频率明显更高,并且 PTMC 的高细胞变体具有显着更大的肿瘤,以及更高的肿瘤多样性和 ETE 率。对于附着在气管上或位于 RLN 过程中的肿瘤,也建议立即手术,尽管这些特征不一定具有生物学侵袭性。
2018 年发布的修订后的 JAES 治疗甲状腺结节临床实践指南建议 AS 应由“适当的医疗团队”进行。包括在颈部成像方面经验丰富的美国专家在内的多学科团队对于进行 AS 是必不可少的,以便在 AS 开始和期间准确评估原发肿瘤和淋巴结,并与个别患者适当地做出共同决定。重要的是,目前缺乏 AS 对 20 岁以下患者安全性的证据。
关键点: AS 的候选对象是临床 T1aN0M0 低危 PTMC 的成年患者。
ETE 和 LNM 的评估
位于甲状腺腹侧且具有提示侵犯带状肌的超声特征的肿瘤不一定适合立即手术。此类病例进展后的转换手术不会影响患者的生活质量 (QoL),因为只需要部分切除肌肉。此外,这种最小的 ETE 对患者预后的影响很小。位于甲状腺叶外侧囊的 PTMC 很少侵犯颈动脉,导致 AS。然而,对于背侧的肿瘤并怀疑侵入气管或 RLN,应非常谨慎地决定管理策略。为了评估侵入气管和 RLN,不仅 US 成像而且计算机断层扫描 (CT) 可能有用,尤其是在肿瘤钙化模糊了肿瘤与这些结构之间关系的情况下。必要时采用喉镜检查是否存在声带麻痹。
隈研吾报告 [肿瘤与气管呈钝角,浸润风险高。图。1)。如果肿瘤和 RLN 病程之间没有正常的甲状腺组织边缘,则 RLN 可能有侵袭的风险。图2)。在手术过程中,没有 PTMCs <7 mm 显示侵入气管或 RLN。然而,在肿瘤和气管之间具有钝角的 51 个 PTMC 中,有 12 个 (24%) ≥ 7 mm 需要剃除软骨或切除气管的全层。类似地,98 个≥7 mm 的 PTMC 中有 9 个(9%)在肿瘤和 RLN 病程之间没有正常边缘,需要在手术过程中进行剃须切除术、部分层切除术或切除术并重建 RLN。仅触及气管或远离 RLN 过程的肿瘤可能是 AS 的候选者。
图1.
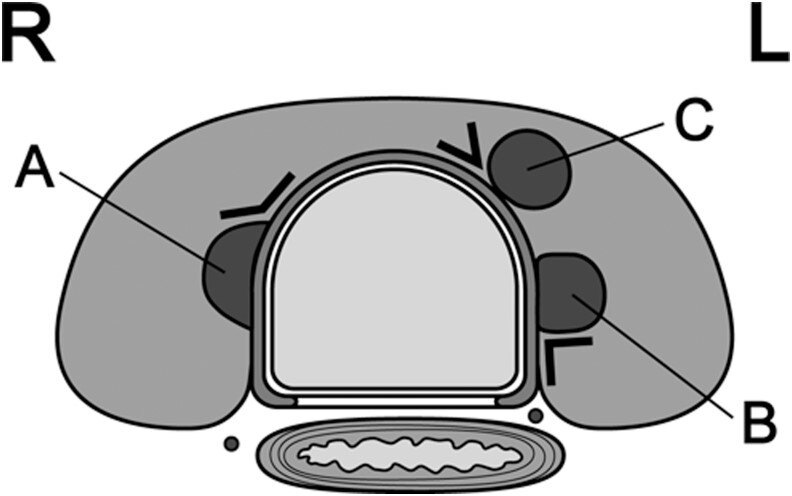
肿瘤与气管之间的夹角。(A)钝角;(B)几乎是直角;(C)锐角。L,左侧;R,右侧。
图2.
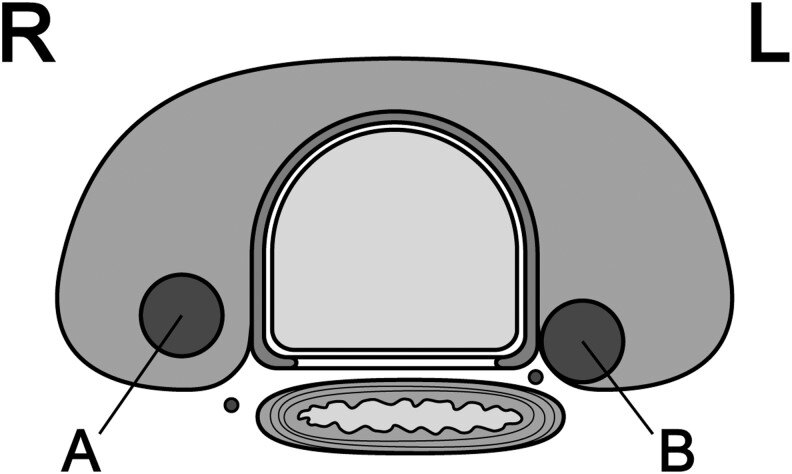
肿瘤和 RLN 病程之间存在(A)和不存在(B)正常边缘。RLN 的路径在右侧比左侧更倾斜。因此,远离气管食管沟但位于背侧区域的肿瘤可能仍然有侵入 RLN 的风险。L,左侧;R,右侧;RLN,喉返神经。
US 通常用于评估 LNM。当怀疑侧颈存在 LNM 时,建议使用 FNAC 并测量针头冲洗液中的甲状腺球蛋白。在慢性甲状腺炎病例中经常观察到淋巴结肿胀,需要仔细考虑个别病例 。伊藤等报道,位于甲状腺上极的 PTMC 更可能表现出临床或病理性横向 LNM ,Jeon等人确定年龄 <50 岁、男性和肿瘤中的微钙化是横向 LNM 的危险因素。然而,由于没有证据表明除年轻之外的这些风险因素是疾病进展的预测因素,因此显示这些风险因素的病例不应被视为不是 AS 的候选者。
要点: ETE和LNM应由超声大夫评估。如果需要可以添加 CT 成像。评估侵入气管和 RLN 时,应特别注意肿瘤表面和气管之间形成的角度,以及肿瘤和 RLN 病程之间是否存在正常的甲状腺组织边缘。
胸部CT评估远处转移
关于低风险 PTMC 远处转移的发生率,Sugitani等人。据报道,148 名 T1aN0 PTMC 患者在手术治疗后均未出现远处转移或远处复发。据报道,626 名接受手术的 T1aN0 患者在随访期间均未检测到远处转移 。崔等人。报道称,满足纪念斯隆凯特琳癌症中心 (MSKCC) 适应症的 4927 个低风险 PTMC 中没有一个显示远处转移。赖因克等人。在 803 个 PTMC 中有 6 个(0.7%)检测到远处转移,但 527 个 T1aN0 PTMC 中没有一个有远处转外。此外,川野等人回顾了 1000 名连续接受胸部 CT 作为常规术前研究的低风险 PTMC患者。他们报告说,这些患者中没有一个在胸部 CT 上有转移性病变 。综合来看,低危PTMC远处转移的发生率极低,常规胸部CT可能弊大于利。
至于 AS 期间远处转移的出现,Sugitani等人。据报道,他们的 230 名患者均未出现远处转移(平均随访 60 个月)。伊藤等人。在他们的 1235 例 PTMC 中同样没有检测到任何远处转移(平均随访 60 个月)。塔特尔等人。MSKCC 的 291 个低风险 PTC(定义为≤1.5 cm)在 AS(中位随访时间,25 个月)期间均未检测到远处转移,表明 AS 期间出现远处转移的发生率为低风险 PTMC 也极低。
关键点:在AS 开始时不建议胸部 CT检查,但如果有疾病进展,则可能需要进行胸部 CT 检查。
影响成年 PTMC 患者决策的因素
年龄
Kuma 医院一项纳入 1235 例观察中的低危 PTMC 的研究表明,≥60 岁患者的 10 年进展率(肿瘤直径增大至 ≥ 12 mm 或出现 LNM)为 2.5%,4.9 % 在 40-59 岁的人群中,22.5% 在 40 岁以下的人群中。多变量分析显示年轻(≤40 岁)是 PTMC 进展的独立危险因素(优势比,4.348;95% 置信区间 [CI 2.293–8.196];p < 0.0001)。宫内等人估计就诊时 20 多岁的患者终生疾病进展概率为 48.6%,30 多岁为 25.3%,40 多岁为 20.9%,50 多岁为10.3%,60 多岁为 8.2%,70 多岁为 3.5%。其他研究也表明老年患者的 PTMC 进展率较低。
要点:具有低风险 PTMC 的老年患者是 AS 的理想人选。尽管年轻患者的肿瘤更容易进展,但这些患者仍然是 AS 的候选者,因为 AS 后手术的结果非常好,即使在就诊时 20 多岁的患者中,终生进展概率也小于 50%。
多发癌灶
自 2003 年 Kuma 医院最初的 AS 报告以来,多发病变不被视为排除标准。162 例 AS 中有 30 例 (18.5%) 有多个病变 。伊藤等人的报告2010 年发现多发病例和单发病例的 PTMC 扩大率没有显着差异。此外,在 1055 名接受立即手术的患者中,未观察到多发灶与无病生存率 (DFS) 之间的显着关联。2014 年,他们对 1235 例 AS 期间 PTMC 进展的危险因素进行了多变量分析,表明多发展不是肿瘤扩大≥3 mm 或出现 LNM 的危险因素。
杉谷 等人在 CIH 和日本医科学校医院招募了 571 名低风险 PTMC 并进行了 ≥1 年的 AS,发现 115 例多发病例和 456 例孤立病例的 10 年进展率分别为 14.8% 和 12.2%(p = 0.51) . 此外,通过多变量分析,多重性不是进展的危险因素。在该研究中,10 名多发病变患者中有 9 名接受甲状腺全切除术,作者得出结论,AS 有利于多个 PTMC,以避免甲状腺全切除术和由此产生的手术并发症。美国、加拿大或韩国的低风险 PTMC 方案和报告中并未将多发灶列为排除标准。
关键点:没有数据表明肿瘤多发灶与肿瘤增大和 LNM 的出现有关。因此,患有 PTMC 和多处病变的患者可能是 AS 的候选者。
家族史
内野等人回顾性分析了 6458 例分化型甲状腺癌 (DTC) 手术病例,并报告其中 258 例 (4.0%) 为家族性 DTC。这些病例更有可能是多发性,并在残余甲状腺中表现出复发,并且 DFS 率低于散发性 DTC。然而,家族性和散发性 DTC 的远处复发率和总生存率没有差异。伊藤等人报道称,在 6015 例 PTC 手术病例中,273 例(4.5%)为家族性 PTC 和临床病理特征(多样性除外),家族性和散发性 PTC 之间的 DFS 率和病因特异性死亡率没有差异。他们得出的结论是,家族性患者的治疗策略应与散发性患者的治疗策略相同,但家族性患者建议行甲状腺全切除术。
卢波利等人1999 年分析了 7 例家族性 PTMC 并报告了高多重性和 LNM 。Capezzone等人 回顾性分析了 291 例 PTMC 手术病例(中位随访时间,8.3 年),并比较了 248 例散发病例和 43 例家族性病例之间的变量。发现家族性病例更可能在双叶都有病理性病变,临床 LNM 阳性并有复发。因此,他们得出结论,在 PTMC 的管理中应充分考虑家族史 。然而,伊藤等人发现家族性和散发性病例的 LNM 增大和外观无显着差异。因此,家族史的存在不应成为 AS 的禁忌症。然而,家族性 PTC 可能更具侵袭性。当计划对 AS 后的家族性病例进行手术时,应考虑甲状腺全切除术。
关键点:有 PTC 家族史的患者的 PTMC 可能是 AS 的候选者。
生育和怀孕
在适当的管理下,怀孕期间的 DTC 显示出良好的结果,患者可以安全地分娩。Shindo等人 Kuma 医院的研究人员分析了怀孕期间的低风险 PTMC 患者,并报告与年龄调整的对照组(27 名患者中的 3 名,11.1 %; p = 0.0497) ( 45 )。然而,研究队列较小,调查周期较短。
伊藤等人Kuma医院的Kuma医院随后通过增加研究时间较长的病例数,调查了能够怀孕的低风险PTMC女性患者是否可以成为AS的候选者。在这份报告中,50 名低危 PTMC 患者在 AS 期间怀孕了 51 次。尽管 4 名患者 (8%) 的 PTMC 直径增加 ≥ 3 mm,但在其余 46 名患者 (92%) 中未观察到尺寸变化。4例扩大病例中,2例分娩后接受手术且未复发。剩下的2个因为分娩后没有扩大而接受了连续的 AS 。
关键点:由于仔细和持续的监测可以安全管理妊娠期低风险的 PTMC,因此希望生育的患者和妊娠患者可能是 AS 的候选者。
钙化
福冈等人报道钙化程度与 PTMC 的增大有关。他们通过将患者分为四类钙化:无钙化、微钙化、宏观钙化和边缘钙化,对 384 名接受 AS 平均 6.8 年的患者(484 个病灶)进行了研究。各组平均年龄分别为52.1、54.2、56.3、60.1岁,增大≥3 mm的比例分别为9.6%、5.5%、3.2%和0%。钙化程度与患者年龄显着相关,钙化较粗的肿瘤肿大的可能性较小。此外,在 AS 期间,分别有 25.1% 和 51.8% 的病变在 5 年和 10 年的随访中显示钙化程度增加。在多变量分析中,最近一次检查中粗钙化(宏观或边缘)的病例显示出明显较低的扩大率(优势比,0.34 [CI 0.11-0.87];p = 0.022)。
在 Kuma 医院的一项研究 中,180 名在 AS 一年后接受手术的患者中,160 例 AS 期间未扩大的病例中有 13.8% 显示大钙化 ≥2 mm 并伴有声影,而 18 例扩大病例中没有一个显示此。相比之下,Oh等人。来自韩国的 273 例低风险 PTMC 观察了 ≥1 年(中位数,42 个月),并证明在 AS 开始时有大钙化的病例比有微钙化的病例更可能显示肿瘤体积扩大 ≥50%,与日本的报道不一致。总之,与钙化强的结节相比,弱钙化的低风险 PTMC 可能会进展,但据报道,钙化会随着时间的推移而变得强烈。因此,具有精细钙化或无钙化的PTMC 仍然是 AS 的候选者。
关键点:没有令人信服的证据可以根据钙化的程度或类型将 PTMC 患者排除在考虑 AS 作为管理策略之外。
血管性
2010 年,杉谷等人CIH 证明,在平均 5 年的 230 例患者(300 个病灶)中,血管丰富的肿瘤(33 个病灶,12%)比血管分布差的肿瘤增大≥3 mm 的比率更高(245 个病灶,88%)(30.3% 对 3.7%;p < 0.0001)。此外,在 2016 年,福冈等人。在同一机构研究了每个肿瘤中血管分布随时间的变化与预后之间的关系。根据他们的数据,AS 开始时血管丰富的 70 个病灶中14.6% 扩大 ≥ 3 mm,明显高于 410 个血管较差的病灶(4.6%)的扩大率。此外,在初始评估时,61.4% 具有丰富血管的 PTMC 在 AS 期间血管分布减少。在多变量分析中,最近一次检查中血管化不良的病例显示出显着较低的肿瘤增大率(比值比,0.17 [CI 0.07–0.43];p = 0.0004)。因此,尽管血管丰富的肿瘤比血管少的肿瘤扩大的风险更高,但低风险 PTMC 的血管分布会随着时间的推移而减少。
关键点:缺乏证据表明根据血管分布程度将 PTMC 排除在考虑 AS 作为管理策略之外。
Graves病和良性结节的共存
似乎没有报告调查过格雷夫斯病对 AS 下 PTMC 的影响。关于格雷夫斯病 PTC 手术后预后的结论存在差异。Graves 病的共存是否影响 PTMC 的生物学行为尚不清楚。但是,至少没有证据表明此类案例应被排除在 AS 候选之外。由于格雷夫斯病的治疗,促甲状腺激素 (TSH) 水平的变化可能会影响 AS 期间的肿瘤扩大。
对于共存的良性结节,虽然未来可能因良性结节扩大而进行手术,但尚无证据表明良性结节患者的PTMCs除外AS。
要点:没有证据表明 PTMC 的 AS 应排除 Graves 病或良性结节患者。应根据合并症的手术指征决定治疗策略。
跟进和监测
如图所示 表一,一AS 下少量 PTMCs 显示进展,即肿瘤增大或新的 LNM 出现。因此,必须进行后续检查,以避免因疾病进展而忽视手术的必要性。表3 总结了 AS 期间的手术指征。
表3。
甲状腺微小乳头状癌主动监测后的手术指征
1. 肿瘤直径达到13mm
2. 出现新的淋巴结转移
3. 患者偏好的变化
4. 出现其他需要手术的甲状腺疾病或甲状旁腺疾病
适当的检查间隔
在由两家日本机构进行的 AS 前瞻性研究方案中,在 AS 开始时每年进行两次美国检查,之后至少每年进行一次。经验丰富的检查员评估了肿瘤大小的变化以及新甲状腺病变和 LNM 的外观。AS 的其他协议建议每年一次或两次美国检查,或在 AS 开始后两年内每六个月检查一次,如果没有任何变化,则每两年一次 。虽然没有发表关于美国检查的最佳间隔的比较研究,但大多数前瞻性研究采用每六个月或一年检查一次进行随访。没有证据表明何时可以进一步延长检查间隔,例如每 2-3 年一次。
关键点:建议在 AS 开始后 1-2 年内每 6 个月由经验丰富的检查员对 PTMC 进行美国评估,如果未检测到疾病进展,则此后每年一次。
肿瘤肿大的定义和合适的手术时机
肿瘤大小是由超声在矢状面和冠状面图像上测量的,最大值通常被认为是最大直径。Ito等人将扩大定义为“最大直径增加 ≥ 3 mm” 。2007 年 。2010 年,伊藤等人和杉谷等人。报告了该定义下的放大率,用于长期观察。这个定义很简单,因此被许多中心采用。使用这个定义,没有患者在 AS 期间表现出 RLN 麻痹或远处转移。
最近,一些研究人员已经通过测量三个维度(定义如放大肿瘤体积增加50%)。另一份报告发现,肿瘤体积的倍增时间提供了一个非常有用的肿瘤生长速度标志物。他们报告说,对肿瘤体积的评估可以准确反映肿瘤大小的变化,并且可以用作其他恶性肿瘤中用于未来生长的潜在预后标志物。然而,这种方法似乎过于敏感,因为从 6 × 6 × 6 到 7 × 7 × 7 毫米的结节的增长率为 59%。将最大直径增加 ≥ 3 mm 视为增大的两个日本机构均未报告手术干预为时已晚的病例。肿瘤体积的测量受观察者高度可变性的影响,因为 US 是一种二维技术,并且体积是用这种测量的所有潜在缺陷推断出来的。因此,推荐基于最大直径的评估作为一种实用且简单的方法。
至于手术时间,Miyauchi 和 Ito 指出,如果患者愿意,可以允许 AS 持续到肿瘤直径达到 13 毫米(24),因为最大 PTMC 增加 3 毫米(即最大直径 10 毫米) ) 形成一个 13 毫米的肿瘤。坂井等人报道,T1bN0M0 PTC(最大直径,11-16 毫米;平均,11.7 毫米)的 5 年和 10 年疾病进展率分别为 5% 和 12%,与 T1aN0M0 没有差异,PTC T1bN0M0 < 15 mm 表明手术后复发。
宫内等人对 AS 下 169 个 PTMC 的肿瘤体积进行动力学分析,报告仅 3% 显示出相当快的增长(倍增率 >0.5/年),17% 甚至缩小(<0.1/年),并且肿大结节的发生率随着年龄(55 岁)。关于扩大后 PTMC 的临床过程,Ito等人。分析了一系列 824 个低风险 PTMC 并报告说,在曾经显示最大直径≥3 mm 和肿瘤体积≥50% 的肿瘤中,分别只有 7.7% 和 3.8% 显示进一步增大。肿大后生长较肿大前明显下降,多见肿瘤缩小。这些发现表明,并不总是需要在直径超过 10 毫米后立即对 PTMC 进行手术。对于这种情况,考虑到肿瘤位置(侵犯 RLN 和气管的可能性)、生长速度和患者偏好,可以进行连续 AS。
要点:为了评估肿瘤生长,应使用最大肿瘤直径,并且在超声上增加≥3 mm 被认为代表肿大。当最大 PTMC 直径超过 10 毫米时,并不总是需要立即手术。
AS期间是否应该进行TSH抑制治疗?
没有发表关于 AS 期间 TSH 抑制治疗低风险 PTMC 的随机前瞻性试验,但已经发表了一些关于 TSH 水平与肿瘤增大之间关系的报告。杉谷等人报道,323 名患者(415 个病灶)的诊断时 TSH 水平和 AS 期间(平均随访 6.5 年)的平均 TSH 水平在肿大组(≥3 毫米)和非肿大组之间没有差异。在多变量分析中,诊断时的 TSH 不被认为是肿瘤扩大的重要预测因素,并且 AS 期间的平均 TSH 水平与肿瘤体积的变化没有显着相关性。
相比之下,伊藤等人。报道在一系列 1235 例病例(平均随访 60 个月)中,1184 例未接受 TSH 抑制治疗的患者中有 57 例(4.8%)出现肿瘤增大,而 PTMC 仅 1 例(2.0%) 51 名接受 TSH 抑制的患者扩大。虽然差异不显着,但接受 TSH 抑制治疗的患者均未出现临床疾病进展(肿瘤大小达到 12 mm 或更大或新出现 LNM),他们建议 TSH 抑制治疗可能预防低危 PTMC进展。金等人韩国报道,在 126 名患者的 AS 中(中位随访,26 个月),高 TSH 组的肿瘤体积增加率高于其他组≥50%。他们报告高 TSH 水平是 PTMC 扩大的独立危险因素,TSH >2.50 mIU/L 的低风险 PTMC 的无进展生存率明显低于其他组。综上所述,不能排除高TSH水平影响低危PTMC进展的可能性,但至少目前还不能得出TSH抑制治疗对患者有益的结论。主动抑制 TSH 可能对心脏或骨骼产生不利影响,尤其是对老年患者。将 TSH 水平保持在较低的正常水平以避免过度刺激对于年轻患者来说是可以接受的,因为他们的 PTMC 更有可能扩大。
关键点:关于 AS 期间 TSH 抑制治疗对低风险 PTMC 的影响的证据不足。执行时,将 TSH 水平保持在正常低水平可能是最好的。
AS应该持续多久和多少年?
如前所述,低风险 PTMC 的进展率被认为随着年龄的增长而降低。然而,高龄是预测不良预后的最重要因素之一。如果老年患者的 PTMC 进展并且未及早发现,则可能性很小,可能会出现危及生命的情况。目前,没有证据表明何时和什么年龄可以停止 AS。
终生持续 AS 并不代表 AS 的缺点,因为即使在手术后,除了定期的术后随访外,可能还需要使用甲状腺激素。尾田等人比较了即刻手术和 AS 之间 10 年的管理医疗费用。据报道,在日本医疗系统中,即刻手术组的成本是 AS 组的 4.1 倍。在香港的一份报告中,AS 组在开始治疗后 16 年的医疗费用较低,其后的成本效益甚至优于即刻手术组。
关键点:低风险 PTMC 进展的发生率可能会随着年龄的增长而降低。然而,如果老年患者的 PTMC 进展,他们的预后可能很差。没有证据表明 AS 可以在多少年后停止使用。因此,建议在整个生命周期中使用 AS。
未来研究的主题
分子标记
PTC 中常见的基因改变包括BRAF、RAS和RET/PTC突变。BRAF基因突变是最常见的一种,一些研究人员报告说 PTMC 中的这种突变与 ETE、LNM 和复发有关。BRAF和TERT启动子突变的组合与临床 PTC 的不良预后有关。Yabuta等检查了 AS 后取出的 PTMC 的手术标本,并报告说BRAF疾病稳定组 (61%)、肿瘤增大组 (70%) 和 LNM 外观组 (80%) 的基因突变没有显着差异。这些病例中没有一个对TERT启动子基因突变呈阳性。虽然 de Biase等人报道,431 个 PTMC 中有 4.7% 具有TERT基因突变。然而,这些突变与其队列中的侵袭性特征或临床结果无关。
关键点:目前,缺乏可靠的 PTMCs 行为分子标记。
患者报告的结果
患者的观点代表了重要信息。选择AS可以避免手术并发症和不良事件,但患者可能会出现对疾病进展的焦虑。相比之下,手术可能会减少对“癌症”的焦虑,因为患者已经“治愈”,但手术的副作用可能会持续存在。
关于甲状腺癌患者的焦虑,Hedman等人发现 48% 的诊断为 DTC 的患者报告了对复发的焦虑,即使已经过去了 14-17 年。索卡等人报道称即使对于 PTMC 患者,对疾病的焦虑也会在一定程度上影响他们的日常生活。Smulever等人。表明 135 名 PTC ≤15 mm 的患者中只有 26 名 (19%) 在细胞学诊断时选择了 AS,许多患者将焦虑作为选择手术的原因。相比之下,戴维斯等人。对在 Kuma 医院接受 AS 的 234 名患者进行了半结构式访谈和现场观察的混合方法调查研究。尽管 37% 的患者对癌症进展感到不安,但 60% 的患者回答说,与 AS 早期相比,他们的焦虑有所减轻。此外,83% 的患者报告 AS 是他们个人的最佳管理策略。
已发表的数量有限的研究比较了接受 AS 和接受立即手术的患者之间的焦虑。吉田等人在一项横断面研究中使用状态-特质焦虑量表比较了 20 名接受 AS 的患者和 30 名接受手术的患者之间的焦虑,发现选择 AS 的患者往往比接受手术的患者有更深的焦虑。然而,焦虑程度与每个患者的特质焦虑相关,与治疗选择(AS 或立即手术)无关,与时间段呈负相关。
全等人在一项横断面研究中使用 12 项简表 (SF-12) 问卷比较了 43 名接受 AS 的患者和 148 名接受腺叶切除术的患者的 QoL,并报告说 AS 组的心理负担小于肺叶切除组(系数,-7.71 [CI -15.26 至 -0.16];p = 0.045)。孔等人。使用针对甲状腺的 QoL 问卷纵向比较了 203 名接受 AS 的患者与 192 名接受手术治疗的患者。他们报告说,在调查开始时的心理健康和八个月调查结束时的心理和身体健康方面,AS 组优于手术组。
AS 在身体 QoL 方面似乎优于手术,但焦虑可能比立即手术观察到的更强烈。通过适当的解释和医疗保健提供者的态度,患者的焦虑被认为会逐渐减少,但未来需要对 AS 和手术的患者报告结果(PROs)进行长期比较研究。考虑患者的价值观和偏好并以适当的态度提供适当的信息在共同决策和后续过程中至关重要。
关键点: PROs关于低风险PTMC管理的证据仍然不足,需要未来长期的比较研究
本文为转载文章,如有侵权请联系作者删除。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论