 三甲
三甲
肺癌KRAS G12C 突变最新靶向药(更新至2024年6月)
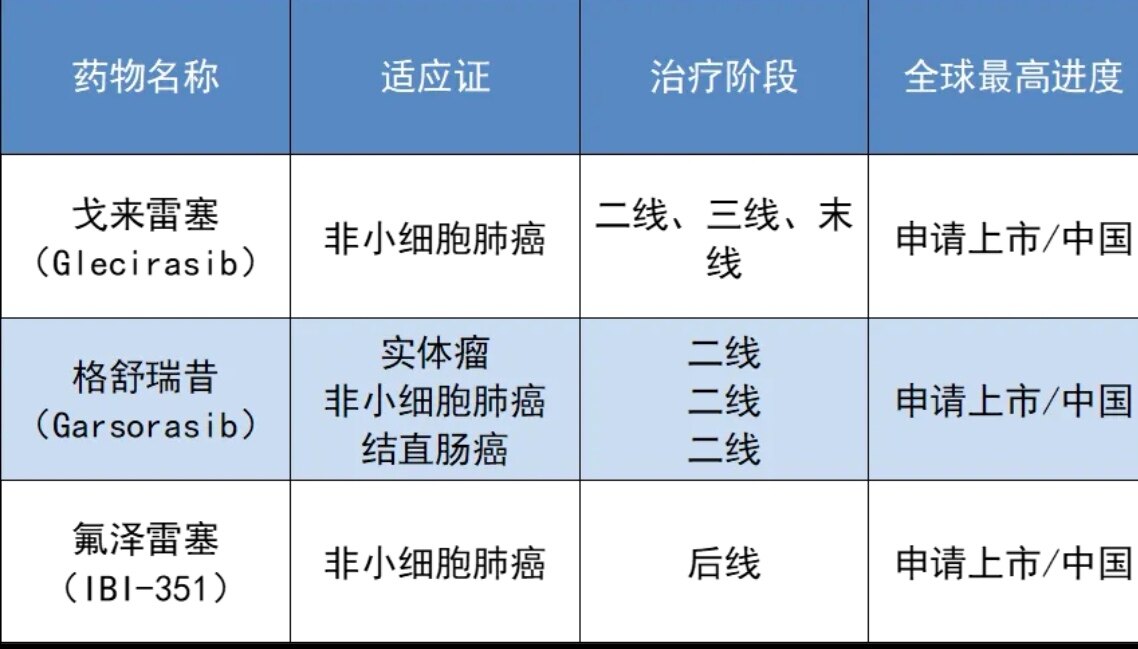
1、格舒瑞昔(Garsorasib )II期临床试验结果于2024年6月11日发表在《柳叶刀-呼吸病学》,这是国产KRAS G12C抑制剂首次登上柳叶刀旗下刊物。
上海交通大学医学院附属胸科医院陆舜研究团队研究结果显示:在既往接受过治疗且携带KRAS G12C突变的NSCLC患者中,客观缓解率(ORR)为50%,疾病控制率(DCR)为89%,中位缓解持续时间(mDOR)为12.8个月,中位无进展生存期(mPFS)为7.6个月。从II期数据来看,Garsorasib与已上市进口药物不分伯仲。目前该产品上市申请已获国家药品监督管理局(NMPA)受理,并纳入优先评审。
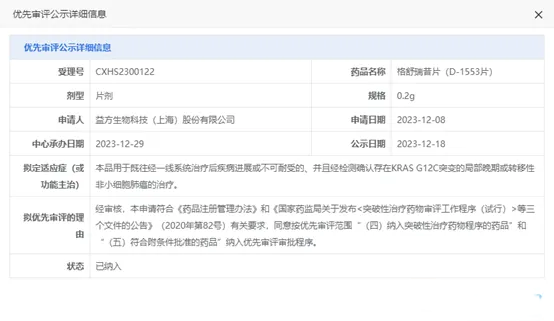
益方生物研发的Garsorasib上市进展
中文名称:格舒瑞昔
英文名称:Garsorasib
研发代码:D-1553
剂型规格:片剂,200mg
申报适应症:KRAS G12C突变的局部晚期或转移性非小细胞肺癌(NSCLC)的治疗。
2、2024年美国临床肿瘤学会(ASCO)年会上,中国医学科学院肿瘤医院石远凯教授团队一项题为“戈来雷塞治疗KRAS G12C 突变非小细胞肺癌(NSCLC)患者的关键性II期单臂研究”:戈来雷塞在本研究中展现出强力的肿瘤控制效果。可评价疗效患者(n=117)的ORR为47.9%,DCR达86.3%,36例患者肿瘤体积缩小超过50%。在随访10.4个月时,仍有34%的患者继续接受治疗,这也提示足够的肿瘤缓解深度和缓解持续时间(DoR)。戈来雷塞的另一个显著特点是起效快,患者在用药后中位1.4个月时即出现首次缓解。戈来雷塞治疗患者的中位PFS为8.2个月。
2024年5月6日,加科思药 业宣布其自主研发的KRAS G12C抑制剂戈来雷塞(通用名:Glecirasib,代号:JAB-21822)的新药上市申请已正式向中国国家药品监督管理局(NMPA)药品审评中心(CDE)提交:用于治疗二线及以上治疗带有KRAS G12C突变的晚期或转移性非小细胞肺癌患者。
本文是王昆版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论