
皮肤黏膜病总好不了?真正的病因可能被忽视了(多图预警)
皮肤黏膜病变是炎症性肠病(inflammatory bowel disease,IBD)最常见的肠外表现之一,约见于 22%~75% 的克罗恩病(CD)患者和 5%~11% 的溃疡性结肠炎(UC)患者[1]。这些皮肤黏膜病变主要有三种类型:反应性皮肤表现、相关性皮肤表现和特异性皮肤表现(图 1)。
许多此类症状的患者,在经过长期的对症治疗后仍未能痊愈,对患者的身心健康造成损伤,同时也对医患关系造成了不利影响。因此,本文特地整理了这些相关表现,旨在为各位皮肤科医生提供学习与参考的素材,以期在诊疗过程中能够更准确地识别和处理此类复杂病例。
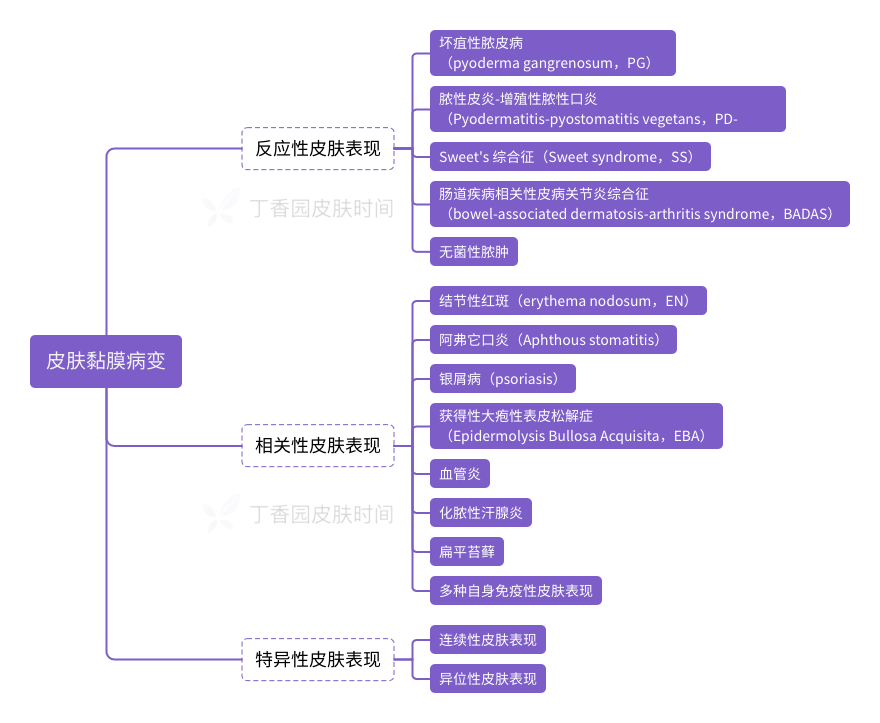
图 1. 思维导图
01、反应性皮肤表现
反应性皮肤表现的组织病理表现,因其皮肤组织有中性粒细胞浸润,亦被叫做「嗜中性皮肤病」。
坏疽性脓皮病
PG 是 IBD 最严重的皮肤损害,对患者生活质量的影响超过消化道受累本身。PG 在 UC(5%~20%)比 CD(1%~2%)更常见。PG 通常在 IBD 确诊后出现,多在疾病活动度增加时发作,罕见于疾病静止期。
PG 可以发生在身体的任何部位,常见于轻微创伤部位,最常见于小腿和肠造瘘口周围。PG 最初表现为多个疼痛的丘疹或脓疱,皮肤坏死后形成溃疡,伴有特征性的紫色边界破坏和无菌脓性渗出物(图 2)。PG 的组织学特征是中性粒细胞过度募集而无感染征象。组织病理学显示中性粒细胞浸润,滤泡周围炎症和真皮内脓肿形成。
患者常报告发热、关节痛和全身不适等伴随症状。诊断前应排除皮肤感染,包括臁疮、坏死性血管炎、脂质渐进性坏死和由动静脉缺血引起的溃疡。
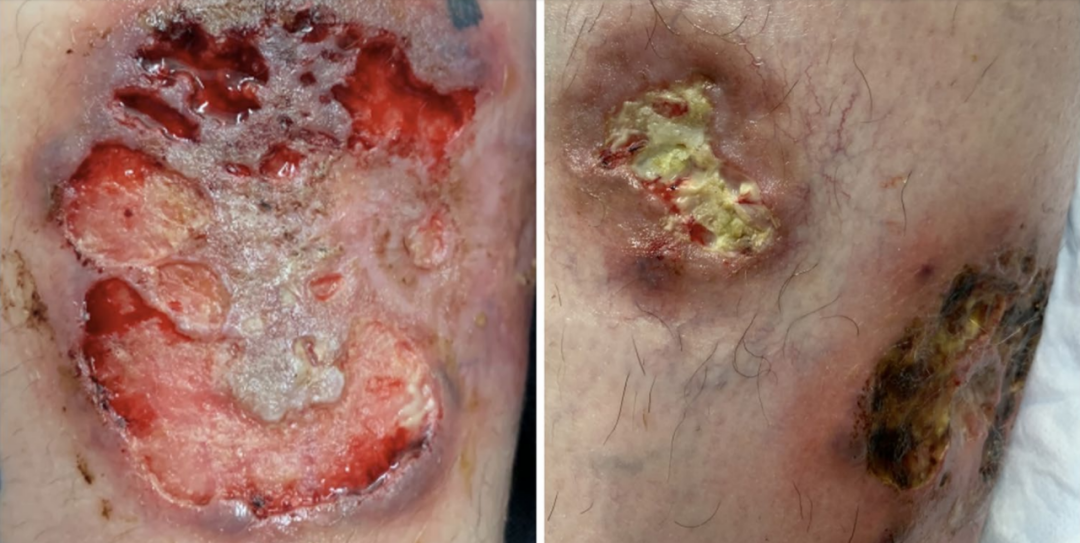
图 2. 53 岁女性克罗恩病患者,四肢呈网状溃疡,边界呈紫色破坏,符合 PG[1]
Sweet’s 综合征
Sweet’s 综合征(SS),又叫急性发热性中性粒细胞性皮肤病。SS 常累及 30~50 岁女性,在 CD(70%)比 UC(30%)更常见,多见于疾病活动期。SS 以红斑丘疹和斑块为特征,主要累及面部(图 3)、颈部和上肢,常有明显压痛。在病程中可出现囊泡和脓疱,有时演变为靶形损害。内镜下可见食管、十二指肠和直肠粘膜溃疡。
多数患者伴有发热、关节肌痛、头痛、结膜炎和口腔溃疡等全身症状和体征。皮损往往会在数周到数月内自行愈合,不留疤痕。
IBD 相关 SS 主要诊断标准包括:
(1)痛性红斑斑片或结节急性发作;
(2)组织病理学证据显示真皮中有致密的中性粒细胞浸润,但无血管炎。
次要标准包括:
(1)发热;(2)与恶性肿瘤、炎症性疾病、妊娠或感染相关;(3)异常的实验室检查:ESR、CRP 和白细胞增多(中性粒细胞 >70%);(4)对全身糖皮质激素治疗反应良好。
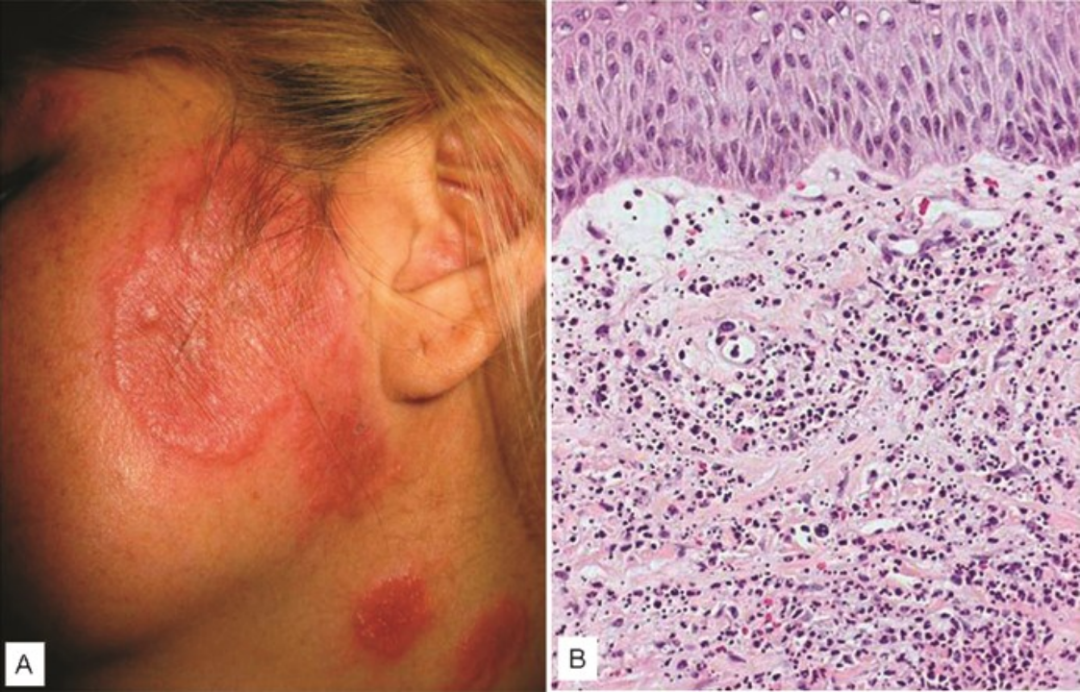
图 3.(A)Sweet’s 综合征的女性面部和颈部出现典型的红斑伴水疱样边界;(B)组织学显示致密的皮肤浸润,以中性粒细胞为主(H&E 染色,原始放大 ×200)[1]
肠病相关皮病-关节炎综合征
BADAS 是一种罕见的中性粒细胞性皮肤病,主要发生在肥胖症旁路手术后的患者中,也有与 IBD 相关的报道。
BADAS 的特点是发热、关节痛(主要累及周围小关节)、肌痛、腹痛、腹泻和皮肤受累,常表现为慢性病程,迁延不愈。皮肤病变一般分布于上躯干和上肢,以疼痛、红斑性丘疹和斑片为特征,偶有脓疱和无菌性囊泡为特征(图 4)。皮肤病变通常为多形性,类似于 PG、化脓性汗腺炎和脂膜炎。组织学上表现为血管周围中性粒细胞浸润,组织细胞的细胞质中含有称为核尘的多形核碎片和真皮水肿。虽然其确切的发病机制尚不清楚,BADAS 可能与小肠细菌过度生长导致含有细菌抗原的循环免疫复合物沉积于皮肤和滑膜有关。
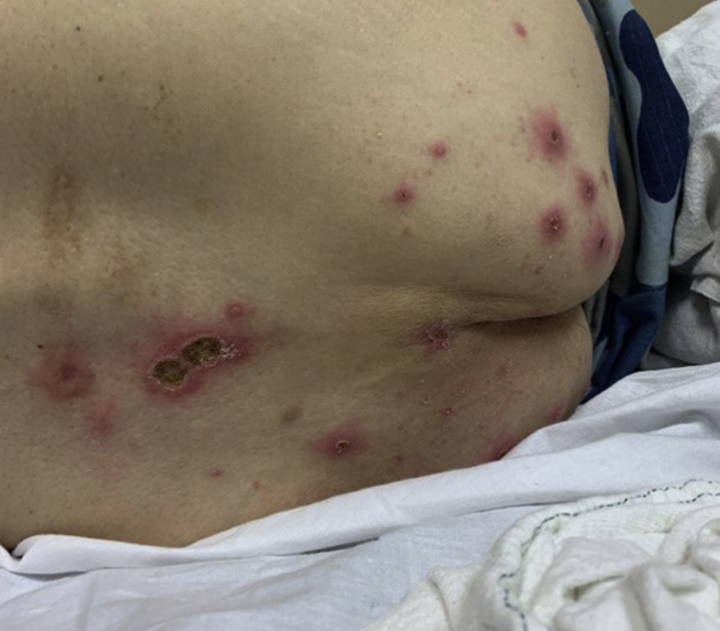
图 4. 克罗恩病直肠炎患者双侧腋窝、大腿、躯干及口腔黏膜多处红斑性水疱及糜烂,下背部和臀部有囊疱和糜烂[2]
无菌性脓肿综合征
2/3 的无菌性脓肿综合征患者合并 IBD。典型的表现包括发热、体重减轻、腹痛和白细胞增多,并伴有无菌性病变,组织学特征为以中性粒细胞为主的炎症浸润。深脓肿主要见于脾脏,但几乎所有脏器都可受累,包括腹腔内(淋巴结、肝、胰)和腹腔外(肺、脑)。有时可出现浅表脓肿(周围淋巴结、肌肉、咽和睾丸)。20% 的患者可检测到皮肤脓肿(图 5)或类似 PG、SS 等典型中性粒细胞皮肤病的特征性皮肤表现。
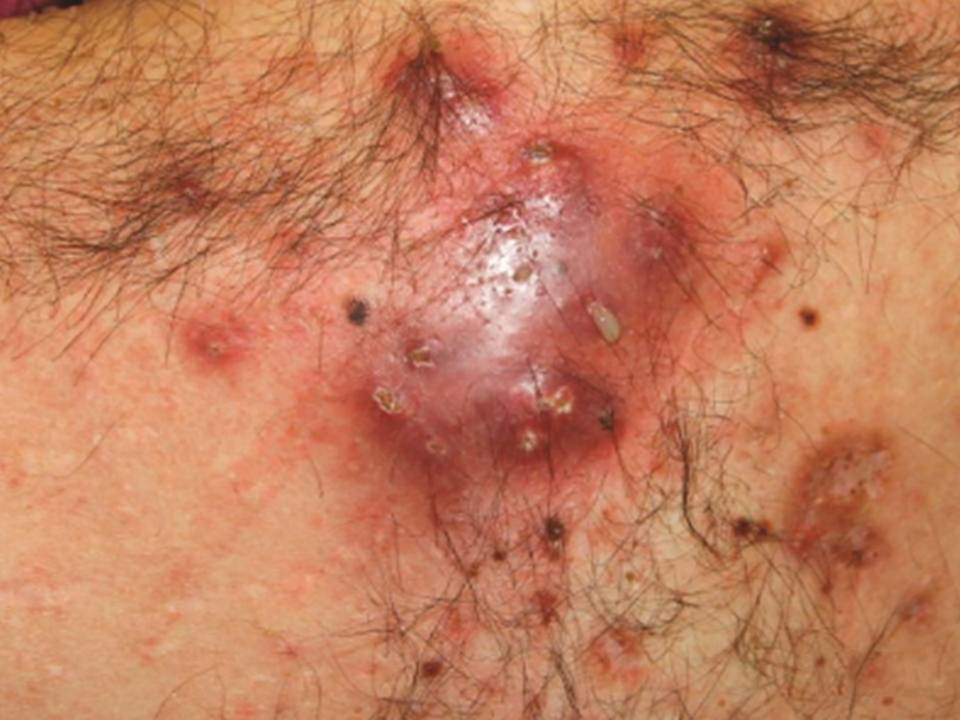
图 5. 无菌性脓肿综合征患者的皮肤脓肿特写[1]
增殖性脓(性)皮炎/口炎
PD-PSV 是一种罕见的皮肤黏膜疾病,大约 70% 的病例合并 IBD,有学者认为 PD-PSV 是 PG 的特殊表现形式。临床上最常见口腔和皮肤病变(尽管任何粘膜表面都可受累)。口腔检查发现红斑和水肿的基础上有多个无痛黄色小脓疱,易破裂形成细长的浅表溃疡,称为「蜗牛纹」侵蚀。皮肤病变表现为丘疹、脓疱、囊泡和结痂,融合成边缘凸起的植被斑块(vegetative plaques)(图 6),主要累及面部、头皮、腋窝、腹股沟,较少累及腹部、胸部和肢体远端。PD-PSV 的皮肤损害通常与口腔病变同时出现或在口腔损害发生后不久出现。
PSV 的组织病理学特征是上皮棘层增生和浅表溃疡伴上皮内和/或上皮下微脓肿。PSV 通常与 IBD 疾病的活动度一致。口腔活检对明确诊断至关重要。此外,90% 的病例存在外周血嗜酸性粒细胞增多。
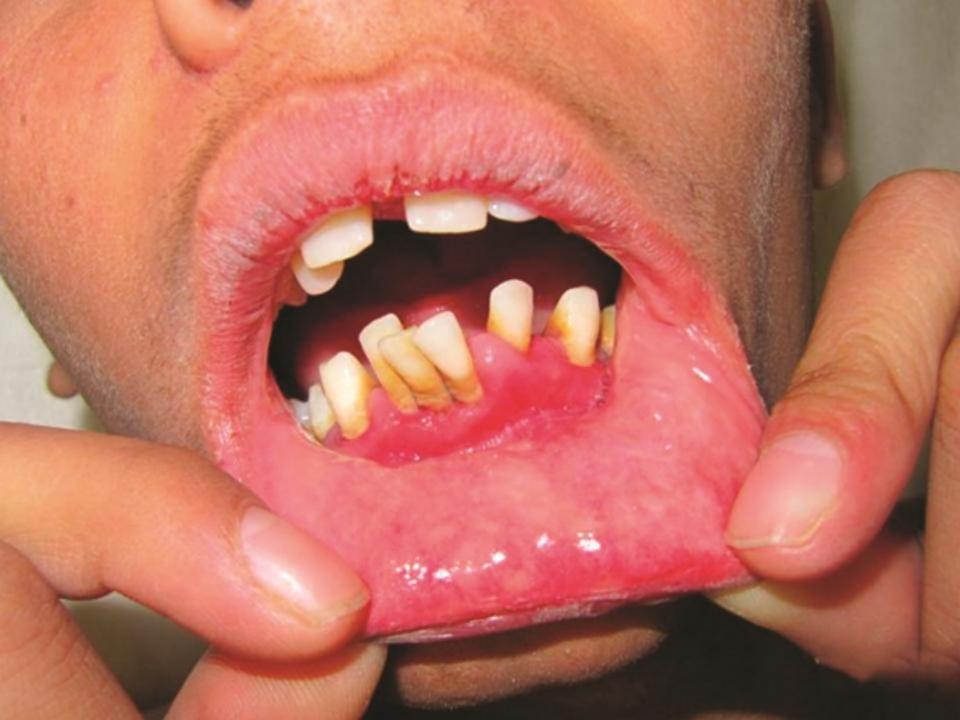
图 6. PSV 年轻男性出现与牙龈增生有关的口腔溃疡性病变[1]
02、相关性皮肤表现
结节性红斑
结节性红斑(EN)是 IBD 中最常见的皮肤表现,见于 15% 的 CD 和 10% 的 UC 患者,女性多见。在大多数情况下,EN 表现为突然出现的对称、凸起、柔软的非溃疡性皮下结节,皮温增高,直径为 1~5 cm,易于辨认(图 7)。EN 通常出现在下肢伸肌表面,最常见于胫骨前区,面部、躯干和上肢很少受累。皮损消退后遗留炎症后色素沉着,无疤痕。EN 常在 IBD 加重时发作,但严重程度并不一定与肠道疾病严重程度平行。
EN 在急性期表现典型,很少需要皮肤活检。如果皮下结节持续超过 8 周,出现溃疡或渗出,应考虑行皮肤活检。组织病理学检查表现为特征性的间隔性隔膜炎,伴中性粒细胞和淋巴细胞浸润。皮肤活检有助于排除硬红斑(Bazin 病)、皮下感染、皮肤结节性多动脉炎、脂膜炎和皮肤 B 细胞淋巴瘤。
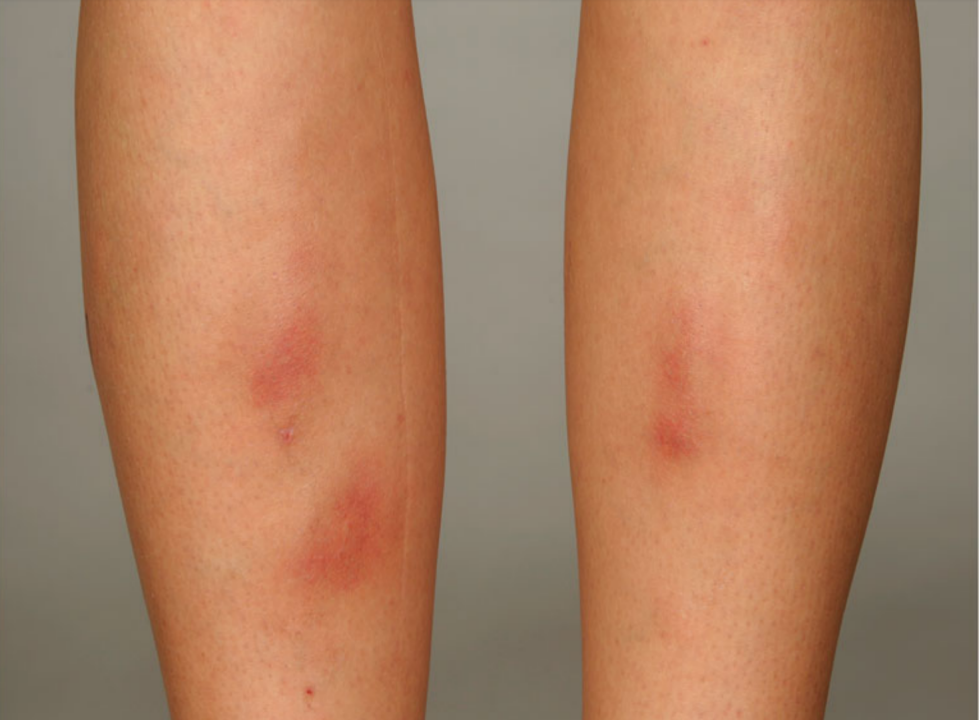
图 7. 结节性红斑:胫骨前皮肤双侧对称、隆起、红斑、痛性的皮下结节[3]
阿弗他口炎
阿弗他口炎在 IBD 患者中的发生率约为 10%,通常与肠道活动性疾病和 HLA-B27 有关。临床表现为多个圆形或椭圆形疼痛性溃疡,伴有黄色假膜基底和红斑边界。溃疡通常位于口腔或唇黏膜(图 8),其特征典型,在确诊的 IBD 患者通常无需行组织病理学检查。对于持续性、复发性和难治性病变以及未明确 IBD 诊断的患者,可行病损边界区域组织活检和培养。
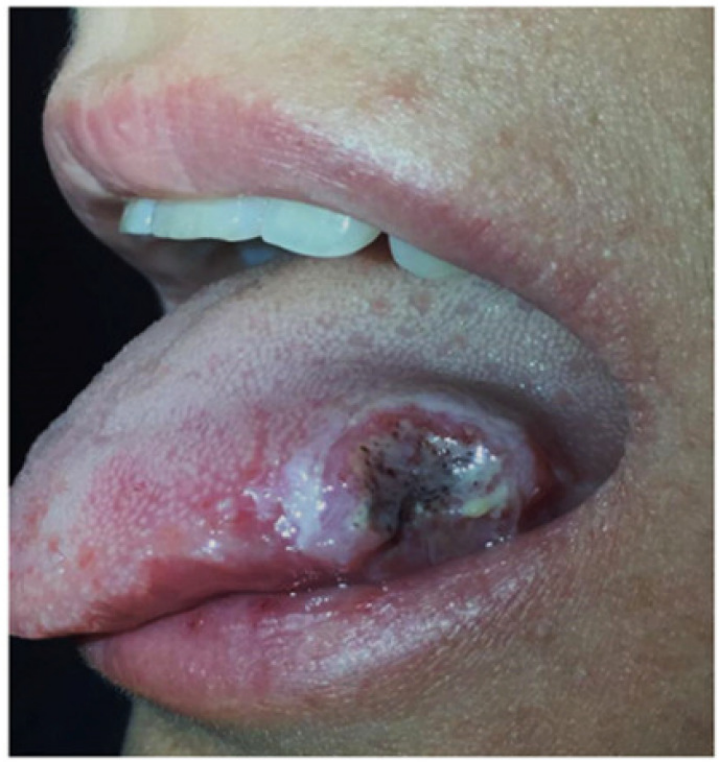
图 8. 克罗恩病患者合并阿弗他口炎[4]
银屑病
银屑病是一种丘疹状鳞状皮肤病(图 9),典型皮损以边界清楚的鳞屑性丘疹斑块为特征,刮屑试验阳性。全身皮肤均可以受累,以头皮、肘部及膝部最常见,冬季好发。
银屑病是最常见的 IBD 相关皮肤病之一,见于 7%~11% 的 IBD 患者,而一般人群发生率为 1%~3%。银屑病在 CD(11.2%)患者中的发病率高于 UC(5.7%)。
某些特定免疫反应模式和常见炎症途径的遗传易感性或 HLA 易感性可解释 IBD 和银屑病之间的关联。CD、UC 和银屑病都与骶髂关节炎和 HLA-B27 相关,IBD 和银屑病共同享有 MHC 相关 6p21 位点易感基因。IBD 和银屑病都是由 Th1 淋巴细胞的异常激活介导慢性炎症性疾病,产生 TNF-α、IFN-γ 和 IL-12 等细胞因子。IL-23R 和 IL-12B 是银屑病和 IBD 发病中共同通路,IL-12B 在银屑病及 IBD 发病中也产生影响。几种靶向 T 淋巴细胞和 Th1 细胞因子的药物,特别是抗 TNF-α 药物对这两种疾病均有效[5]。

图 9. 克罗恩病患者多发性斑块状银屑病[1]
获得性大疱性表皮松解症
大疱性表皮松解症(EBA)是一种自身免疫性疾病,与多种疾病有关,但与 IBD 的关联最强。EBA 表现为表皮下起疱和瘢痕形成,主要局限于易受外伤的部位,如手、膝盖(图 10A,B)、足;粘膜也可受累。
EBA 的特征是产生针对 VII 型胶原蛋白(真皮-表皮交界处固定原纤维的主要成分)的 IgG 同型自身抗体。自身抗体与 VII 型胶原蛋白结合引发炎症反应,包括补体的固定和白细胞的 Fc 依赖性激活。活化的粒细胞释放活性氧中间体和蛋白酶,导致上皮损伤和水疱形成。
EBA 可表现为张力性水泡和大疱,演变为糜烂。水泡可能呈血性,愈合后通常形成疤痕和粟粒疹。可能出现炎症特征,包括红斑、荨麻疹斑块和瘙痒。
EBA 可表现为张力性水泡和大疱,演变为糜烂。水泡可能呈血性,愈合后通常形成疤痕和粟粒疹。可能出现炎症特征,包括红斑、荨麻疹斑块和瘙痒。
EBA 的诊断依赖于免疫病理:病灶周围皮肤直接免疫荧光显示 IgG(少量 IgA)和/或 C3 沉积在真皮-表皮交界处(图 10C),而分离皮肤间接免疫荧光显示 IgG(少量 IgA)和/或 C3 沉积在分离皮肤底部(图 10D)。
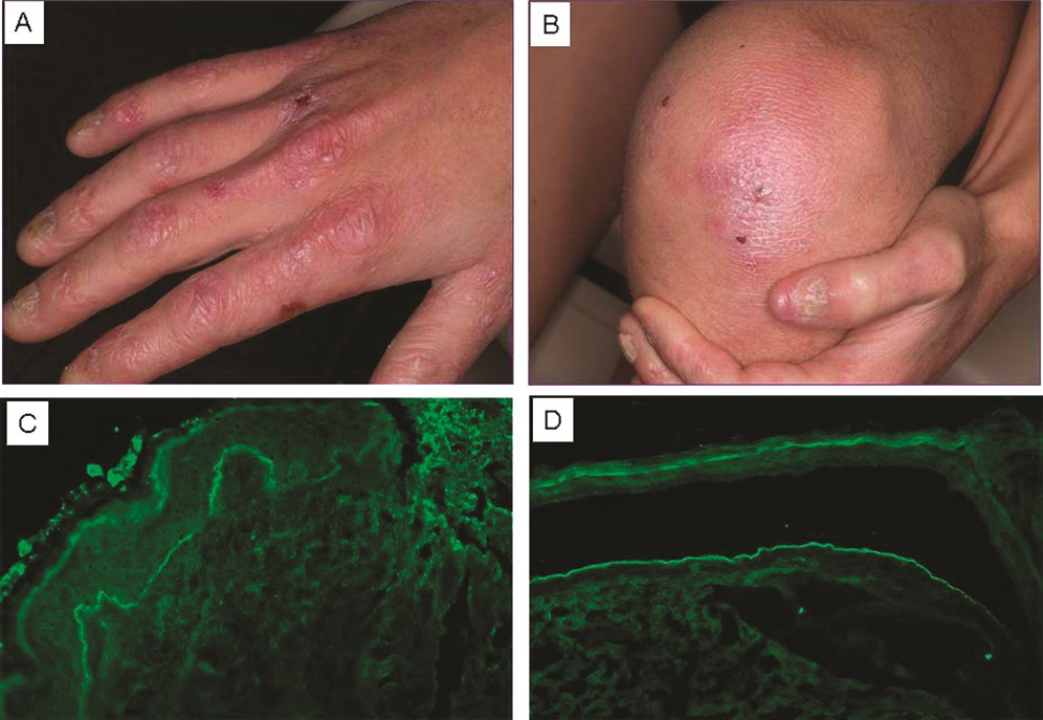
图 10. 手背(A)和膝盖(B)处水疱和糜烂伴红斑,(C)直接免疫荧光显示真皮-表皮交界处有 IgG 沉积,(D)间接免疫荧光(1M 氯化钠分离皮肤法)显示 IgG 沉积在分离皮肤底部[1]
03、特异性皮肤表现
特异性皮肤表现被认为与 IBD 有相同的组织病理学改变,主要表现为非干酪样肉芽肿伴多核巨细胞、淋巴细胞、浆细胞或嗜酸性粒细胞等浸润真皮层,和肠道病理表现一致。这类皮肤表现仅见于 CD 患者。根据皮肤受累的位置不同,可分为连续性皮肤表现及异位皮肤表现(转移性 CD)。
连续性皮肤表现
连续性皮肤表现是肠道症状的延续,即皮损均出现在消化道的连续部位,如唇缘、面部、肛周,表现为脓肿、溃疡、肛瘘,与肠病的活动相关(图 11)。8%~9% 的 CD 患者存在口腔受累,肛周炎症见于 25%~80% 的 CD 患者,肛瘘发生率为 6%~34%。目前除了手术治疗,尚无有效的内科疗法;虽有研究表明生物制剂对 CD 肛瘘有效,但目前该病仍以外科治疗为主[4]。
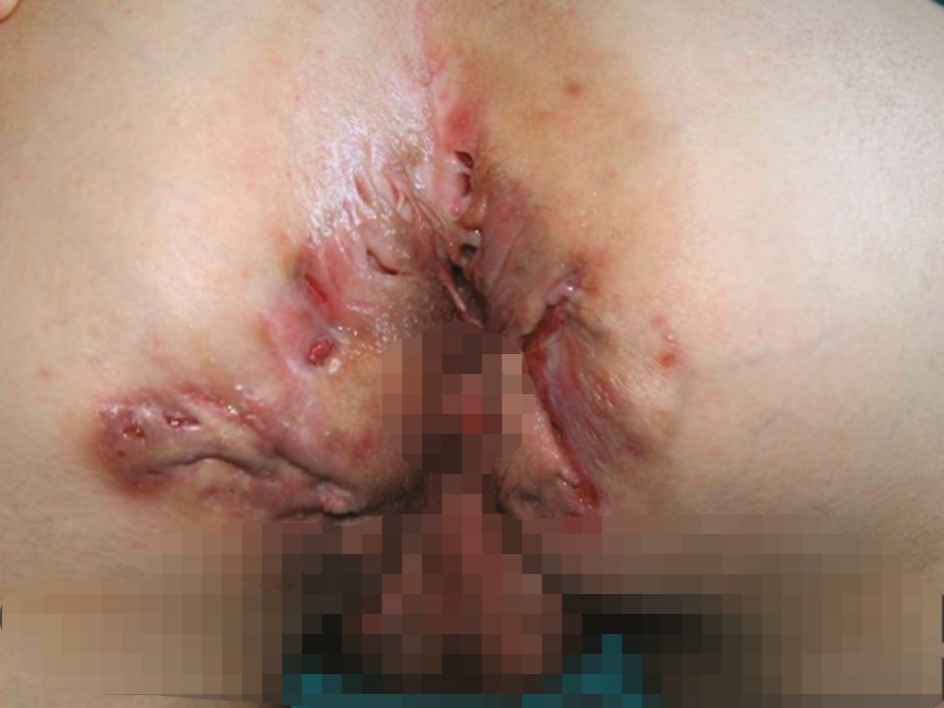
图 11. 肛周克罗恩病,表现为多发脓肿和瘘管形成[1]
异位皮肤表现
转移性 CD 主要表现为脓肿、瘘管、溃疡或结节,皮损可出现在任何地方而非消化道的连续部位,多累及下肢末端和易受摩擦之处,而面部和生殖器少见(图 12)。转移性 CD 不与肠病活动平行。其治疗手段也较为局限,包括局部或系统应用激素、免疫调节剂、生物制剂等,但疗效常不确切[4]。
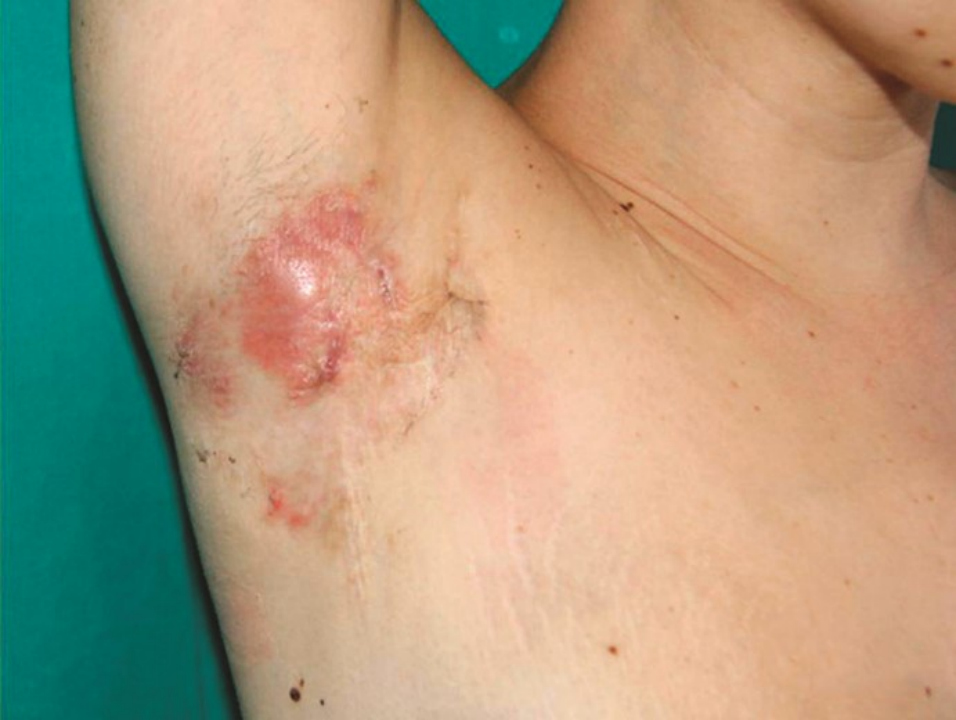
图 12. 表现为红斑性结节和的转移性 CD[1]
04、特点和治疗建议汇总

本文为转载文章,如有侵权请联系作者删除。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论