 三甲
三甲
血管内栓塞治疗脊髓脊柱血管疾病
一般根据Lasjaunias的分类方法,将脊柱及脊髓血管畸形分为椎管内血管畸型、硬膜血管畸形、椎体血管瘤和硬膜周围/椎体旁血管畸形(如Cobb’s综合征)。椎管内血管畸型又分为髓内动静脉畸形、髓周硬膜下动静脉瘘、硬脊膜动静脉瘘。
脊柱及脊髓血管畸形血管内栓塞治疗原理是利用畸形血管的血流优势的特点,将栓塞材料带入畸形血管而不影响正常血管。栓塞原则是经过较安全的途径,循序渐进地减慢脊髓的动静脉间的异常血流,减轻对脊髓机械压迫,减少出血机会,逐渐使畸形血管血栓形成,血管闭塞,最终达到完全消失,从而改善脊髓神经功能。对于只有1~3支供血动脉的小AVM,可采用血管栓塞疗法使之完全闭塞,对于巨大的AVM通过栓塞可减少动静脉分流和缩小病灶,使原来不能手术切除的病变成为可以切除的病灶。
一、脊柱及脊髓血管畸形血管内栓塞治疗方法
(一)术前准备
1.病人准备 见第五章第六节。
2.特殊器械药品准备 16G或18G穿刺针1根;直径0.88mm(0.035)长40cm短导丝1根;6F导管鞘1个;6F导引管1根;4F、5F脊髓血管造影导管各1根;Magic-3F/2F、Tracker-18或Cordis 3F/2.5F微导管1根;0.35mm(0.014inch)微导丝1根;Magic-BD导管1根;带三通软连接管1根;Y型带阀接头1个、二通开关1个;动脉加压输液袋2套;球囊镊1把;BALT带X线标记球囊1、2、3号各若干;微粒栓塞材料:冻干硬脑膜微粒、Ivalon微粒,直径均为100~150m,真丝线段3-0、5-0若干;NBCA0.5ml/支×4支,碘苯酯1ml/支×1支。
(二)体位准备和麻醉 见第五章第六节。
(三)手术步骤
1.穿刺插管采用Seldinger法, 操作见第五章第六节血管造影穿刺技术(一)、(二)、(三),右侧股动脉插入6F导管鞘。
2.将4F或5F脊髓血管造影导管经6F导管鞘分别选择插入根动脉进行选择性脊髓动脉造影,了解病变部位、范围、类型,脊髓AVM的供血动脉及其来源,畸形血管团(表现为脊髓深部一个或几个独立的匐状迂曲的血管染色)的部位、大小、在髓内或髓周,有无动、静脉瘤,引流静脉的粗细、引流方向及循环时间等,从而明确诊断,为决定治疗方法提供重要资料。
3.诊断明确后根据病变情况进行血管内栓塞治疗,整个栓塞过程中病人均需行全身肝素化治疗。
(1)栓塞方法:一般包括经过造影导管直接栓塞和微导管超选择栓塞两种。提倡采用微导管栓塞治疗,尽量送至畸形血管团避开主要功能动脉。但一般的导管技术很难送到每支纤细又迂曲的供血动脉内直至畸形团的边缘,大部分栓塞仍是通过血流趋向性,将栓子送到畸形血管内。 对肋间动脉、腰动脉供血的胸腰段脊髓畸形,有单支或多支供血动脉在造影诊断后直接注入栓子栓塞。一般来说,通过脊髓后动脉栓塞是较安全的途径。对有椎动脉参与供血的颈段脊髓血管畸形,脊髓前动脉供血的胸腰段血管畸形,为避免误栓可采用微导管栓塞。
(2)微导管导入方法:将4F或5F导管撤出,更换6F导引管选择插入病变供血动脉,其尾端接Y型带阀接头,Y型阀接头侧臂与动脉加压输液袋输液管道相连,排净管道内空气后,调节加压输液速度,慢慢滴入生理盐水。经Y型阀有阀臂插入Magic-3F/2F、Tracker-18或Cordis 3F/2.5F微导管,用微导丝将其导入根动脉,尽量使其接近脊髓AVM畸形血管团,避开根动脉的穿支。采用Magic-BD带球囊导管,球囊型号依病变选择。
(3)栓塞材料:以固体栓子较为安全,直径100~150m的冻干硬脑膜微粒、Ivalon微粒、及3-0或5-0,长1-2cm的真丝线段为首选。缺点是有时可并发动脉主干的栓塞和易松动造成畸形再循环。根据供血动脉的直径、血流速度来选择栓塞材料,注入栓子的量应根据畸形病变的大小及术中栓塞情况而定。注入栓子时浓度不宜过高,可用生理盐水、碘水及栓子混悬液,注射速度应慢,不能有返流现象。脊髓动脉在形成中发出许多细小的沟联合动脉供应脊髓,其直径为100μ左右,如栓塞材料直径小于100μ可能在达到畸形血管团之前,先将沟联合动脉栓塞,在影象学上虽然看到脊髓动脉主干通畅良好,但脊髓已处于缺血状态,脊髓神经功能难以恢复,甚至在原障碍的基础上加重,因此脊髓血管畸形伴有瘘时对于栓塞材料的选择是至关重要的。
液态栓塞剂主要为氰丙烯酸正丁酯(NBCA),可永久性栓塞,应注意:①导管尖端必须接近畸形血管团或靠近瘘口处;②确认导管前端无正常脊髓穿支供血动脉;③根据血流速度及病变的大小,严格配制其浓度,控制注入的量,防止栓塞剂进入引流静脉,注入的量过多引起返流而误栓正常脊髓动脉。
(4)术中判定:术中定时注入造影剂了解栓塞情况,当供血动脉流速减慢或畸形血管大部分消失即可停止栓塞,不可一味追求畸形血管团完全消失,这样会造成脊髓主干的闭塞,引起脊髓缺血。引流静脉的显示较栓塞前明显延迟或消失,病灶明显减少,供血动脉保留为停止栓塞的指征。当栓塞完一支供血动脉还应继续行剩余脊髓供血动脉的造影,以免遗留其他供血动脉。
4.治疗结束,酌情用鱼精蛋白中和肝素,拔出导管与导管鞘,穿刺部位压迫15~20分钟,待无出血后盖无菌纱布,并加压包扎。
(四)术后处理
1.严密观察病情变化,尤其是脊髓功能恢复情况,注意穿刺点有无出血,穿刺侧足背动脉搏动与肢体血循环情况。
2.应用钙离子拮抗剂,如尼莫地平、尼莫通防治血管痉挛;
3.应用抗菌素防治感染;
4.应用神经营养剂协助脊髓功能恢复;
5.加强截瘫和泌尿系护理防止褥疮和泌尿系感染。
目前栓塞已成为治疗椎管内血管畸形的首选方法,可能的话,栓塞后应隔3个月、6个月、1年、2年、5年分别造影复查,发现畸形可再次栓塞,直至痊愈。
二、椎管内血管畸形的诊断和治疗
(一)脊髓内动静脉畸形(spinal cord arteriovenous malformation, SCAVMs)
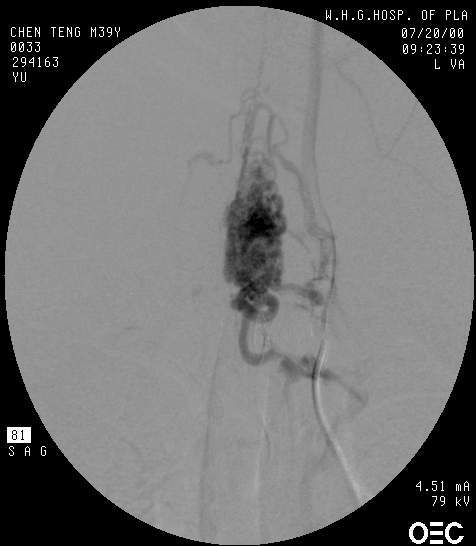
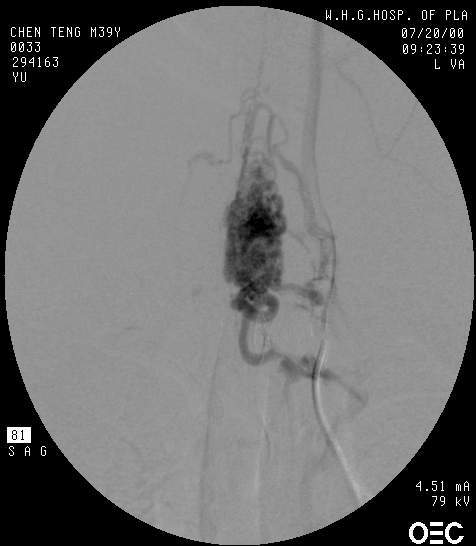
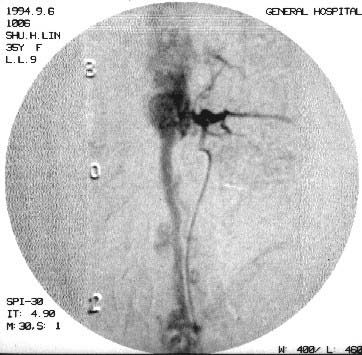
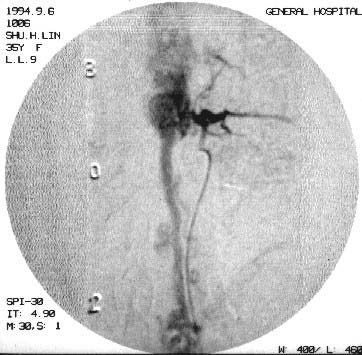
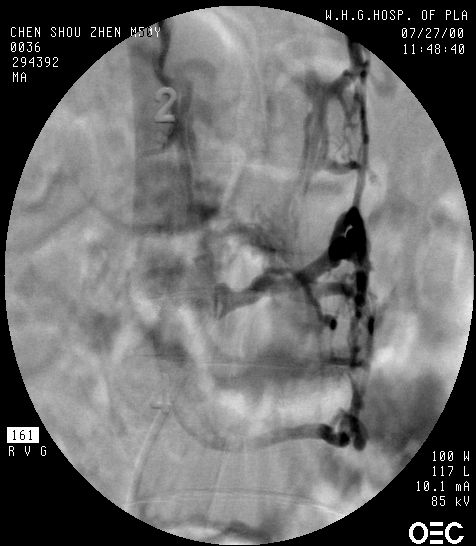
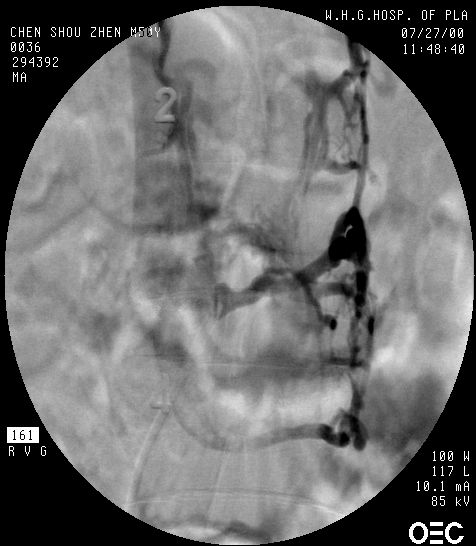
1.血管造影特征 动静脉畸形不同程度地显示紊乱,粗细不一和扭曲的畸形血管、供血动脉,引流静脉多显著扩张,并常向上或向下延伸很远,甚至抵达颅内。SCAVMs伴发囊状动脉瘤者并不罕见,尤其是那些发生蛛网膜下腔出血的病例,两者往往同时存在。这些囊状动脉瘤几乎总是位于SCAVMs的主要供血动脉上。但是在显示脊髓受损及病变与邻近组织的关系方面还存在一定的欠缺(图24-3-1)。
一般说来,由于脊髓与脊柱的生长率之间有差异,所以SCAVMs常位于供血动脉的头侧。SCAVMs的供血动脉的大小与数量常因部位的不同而异。颈段畸形多为中等大小,占据1~3个节段,供血动脉较多,常来自双侧锁骨下分支(椎动脉、肋颈干和甲状颈干),几乎全部都位于腹侧或同时累及腹背侧;胸段畸形范围最广,多在3~4个节段以上,然而其供血动脉较少(2~3支),一般为单侧,源自肋间动脉;胸腰段畸形最小,往往仅一条动脉即Adamkiewicz动脉供血,畸形多位于脊髓背侧髓外,由后动脉系统供血,位于腹侧者由前动脉供血,同时累及背侧者则由相对独立的两部分组成。
2.栓塞治疗目的 减少出血的危险和缓解进行性的脊髓功能障碍。
(1)适应证:血管内治疗首选沟联合动脉短,引流静脉在后方,位于中线两侧,弥漫状,范围广泛超过两个椎体,不适合外科手术或手术困难的动静脉畸形;即使适合外科手术的沟联合动脉长,引流静脉在前或侧方,位于中线,团块状,长度不超过两椎体的局限性动静脉畸形也可考虑栓塞治疗;在动脉瘤和静脉扩张存在时应首先栓塞治疗;长期脊髓完全横断性损害,栓塞术可减少疼痛、肢体痉挛或病变再出血。发育未全型SCAVMs,畸形血管间隙内含有脊髓组织,不可能手术切除的,首选栓塞治疗;术前栓塞可明显减少术中出血,提高手术成功率。
(2)禁忌证:髓内动静脉畸形为脊髓前动脉供血,尤其为Adamkiewicz动脉供血者,超选择插管不能避开由此供血动脉分支供应正常脊髓组织时,栓塞有可能将正常供血动脉分支栓塞而加重脊髓功能障碍,应禁忌栓塞治疗。
3.术中注意要点
(1)对椎管内动静脉畸形,无论那种类型的病变血管内栓塞治疗成败的关键,在于对病变供血动脉的超选择性插管是否成功,而且要避开供应脊髓的正常穿支,并酌情选择适宜栓塞材料。
(2)对SCAVMs的栓塞,如能超选择插入微导管达畸形血管团的边缘,避开主要功能动脉,可注入NBCA,部分或全部栓塞畸形血管团;大部分病例难以将微导管超选择插入到畸形血管团边缘,栓塞时注入真丝线段或微粒是利用优势血流趋向性将栓子带到病灶内,或栓塞与病变恰前方供应的脊髓后动脉,注入量过多,可能造成脊髓动脉主干闭塞,引起脊髓缺血。然而下列情况例外:①位于颈段者,因尚有其它血管供应脊髓,故无论结扎还是栓塞畸形供应动脉均无脊髓缺血发生。②由粗大的Adamkiewicz动脉供应的胸腰段畸形,注入小栓子,仅栓塞其直接供应畸形的分支,既足于减少畸形血流,显著改善症状,又不会引起脊髓缺血。
当畸形血管团主要供血来自脊髓前动脉,尤其是Adamkiewicz动脉,通常认为闭塞该动脉,可引起广泛严重的脊髓缺血。必须经其栓塞时,应选择下述情况:①供血动脉扩张弯曲度大,沟联合动脉短并与畸形血管团直接交通者;②血流速度快,直接进入畸形者;③在畸形血管团的上、下有正常的脊髓前动脉或侧枝循环;④导管头端应尽可能靠近畸形血管团。同时进行保护试验,利多卡因20mg经微导管注入及间歇的脊髓前动脉血管内压监测。当利多卡因刺激试验阳性或血管内压增加到收缩压的90%时,应视为停止栓塞的指征。
(3)由于SCAVMs的供血动脉多源自并非必须的肋间动脉和腰动脉,将之闭塞不必顾忌。另外,SCAVMs的供血动脉进入椎管后(可能在进入硬膜处)有一狭窄点,该处直径常减少50%,是栓塞的理想部位。
(4)对于根动脉起自椎动脉区域的AVM的栓塞,多采用两种技术,用微导管超选择性地插入AVM的供血动脉蒂栓塞或用球囊暂时阻断供应AVM的根动脉起始部远端的椎动脉,然后注射栓塞物质于椎动脉干内。这样可以防止栓子返流造成椎动脉及其分支栓塞。
4.主要并发症 SCAVMs尤其是通过脊髓前动脉,甚至Adamkiewicz动脉供血的,在栓塞时,应尽力避免脊髓动脉主干闭塞,否则会引起脊髓缺血,加重神经功能障碍。
(二)硬膜下髓周动静脉瘘(perispinal arteriovenous fistulas, PSAVFs)
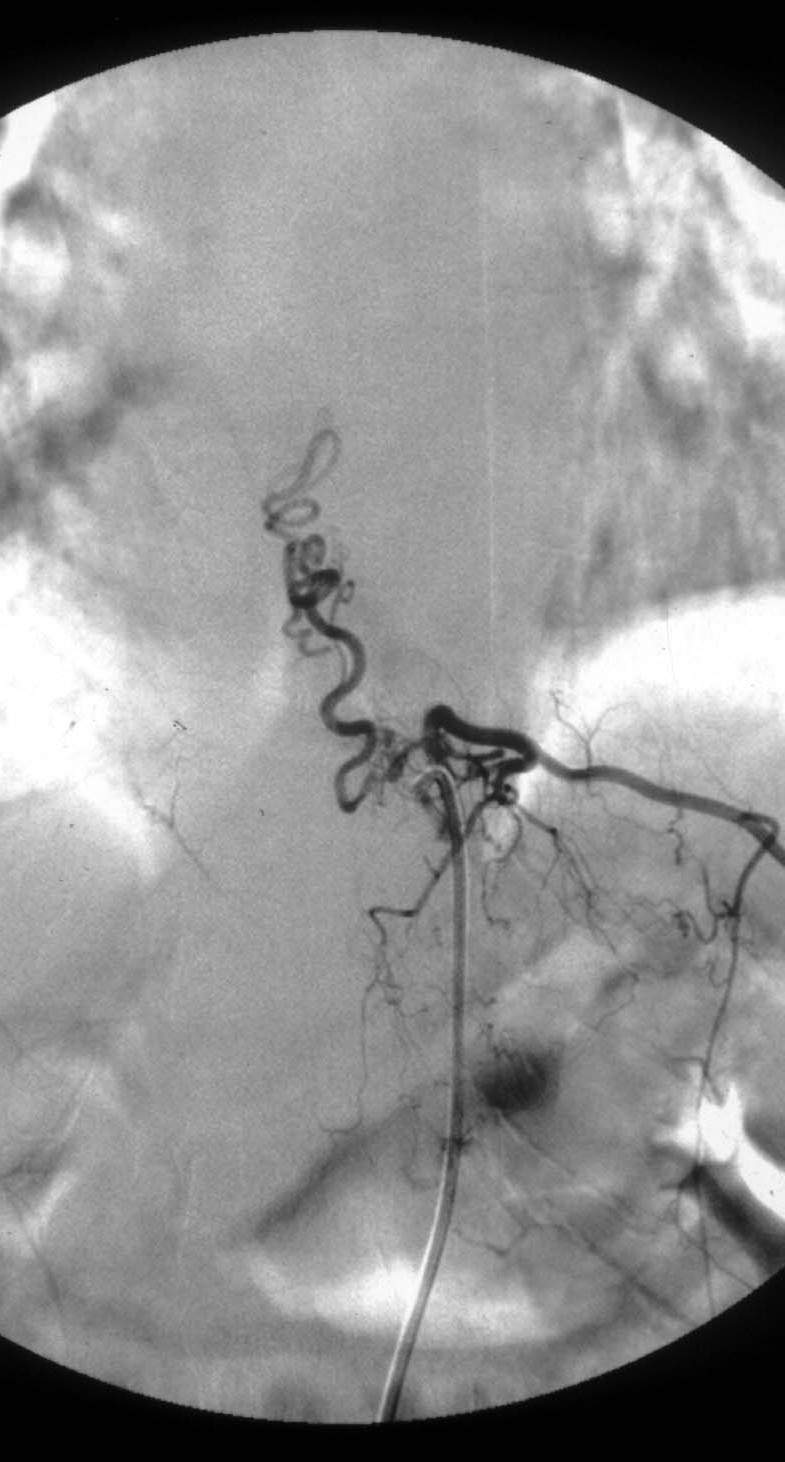
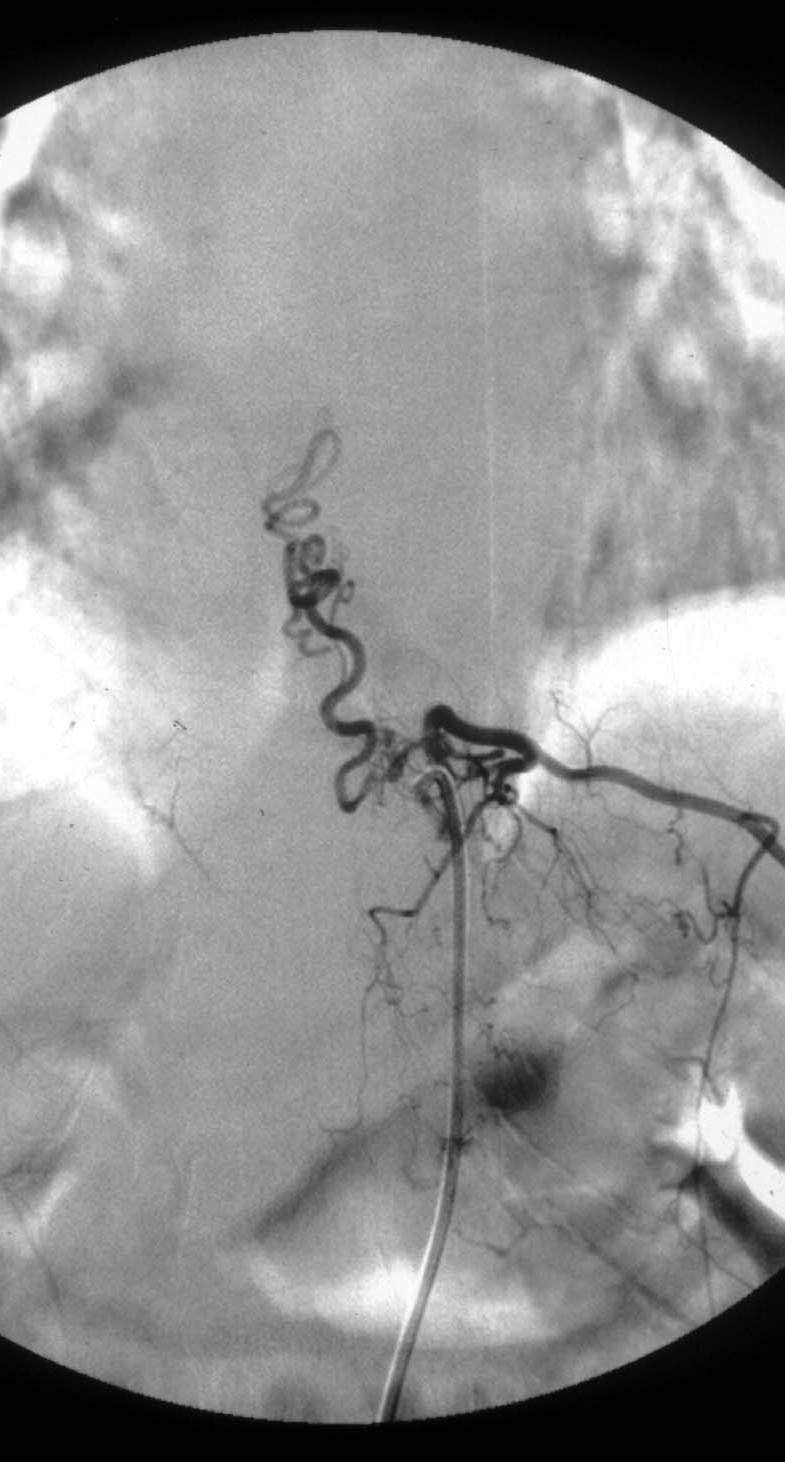
1.血管造影特征 可以了解脊髓前、后动脉与静脉交通瘘口的部位、大小,循环速度因瘘口大小而异等(图24-3-2)。可见于从颈髓到马尾的任何节段,以马尾圆锥部多见。
2.栓塞治疗目的 闭塞瘘口本身。动、静脉都应保留,否则会加重髓内循环障碍的现象。
3.术中注意
(1)PSAVFs的血管内栓塞必须严格注意超选择插管,做到既栓塞瘘口,又保留供血动脉和引流静脉。因此选择栓塞材料应稍大于瘘口,与瘘口相匹配,否则静脉淤滞而导致脊髓水肿、坏死,从而引起症状加重。同时也应注意避免将供血动脉栓塞,只栓塞供血动脉不仅不能治愈,反而给进一步治疗带来困难。
(2)瘘口太小限制微导管在血管内的通过;对瘘口小的可采用微粒栓子(Ivalon、冻干硬膜、微球或弹簧圈等);对于供血动脉和瘘口均粗大的病例,采用可脱性球囊栓塞粗大的供血动脉后,加用微粒栓塞较小的供血动脉,疗效较好。
4.主要并发症 PSAVFs血管内治疗后并发症主要有:①供血动脉被栓塞致供应脊髓的正常分支缺血导致脊髓功能障碍;②引流静脉被栓塞而导致髓内循环障碍,脊髓水肿所致的一系列并发症。
(三)硬脊膜动静脉瘘(spinal dural arteriovenous fistulas, SDAVFs)
1.血管造影特征 瘘口常见一个,有时为多个,位于胸腰段的水平,常见胸5~7和胸12~腰3水平。供血动脉来自肋间动脉、腰动脉或骶动脉,可见血流缓慢地从根动脉发出的一至数根纤细的硬脊膜动脉通过硬膜内微小的瘘口(据报道约为140mm,多位于椎间孔神经根袖套前下方,侧位像可以显示清楚)直接交通到根静脉,没有发夹样的脊髓动脉。常伴有硬膜外正常的引流静脉消失及脊髓引流静脉紊乱,引流静脉向上进入椎管内硬脊膜下参与前或后髓周静脉系统(冠状静脉系统),并使之明显扩张几乎贯穿脊髓全长,静脉系统往往先向下到达圆锥水平,从此沿其它根静脉引流出椎管外。正常的硬膜外静脉丛一般不充盈,其循环时间相当慢,脊髓静脉完全充盈需时40~60秒,正常从Adamkiewicz动脉造影只需13~21秒(图24-3-3)。瘘口部位越低,其椎管内静脉高压的程度也因静水压的增加更趋明显。Willinsky等认为,如果脊髓血液循环中的静脉影像正常,可以排除脊髓功能障碍是由DAVF引起的。
当其主要引流作用的脊髓根静脉因血栓形成而狭窄或闭塞时,使脊髓表面的弯曲引流静脉距离很长,同时没有向椎管外的根静脉引流出现,造影剂在脊髓表面迂曲的血管内滞留达数分钟之久,称之为Foix-Alajouanine综合征。个别报道由于引流根静脉的闭塞,注射造影剂后SDAVF不显影,此时只能靠椎管碘液造影和脊髓MRI来诊断本综合征。
2.治疗目的 阻断到髓周静脉的引流,消灭瘘口及畸形团,缓解脊髓静脉高压,恢复脊髓的正常血运。栓塞治疗应为首选方法,只有当ASA与AVF供血动脉在同一水平时或栓塞失败后,才行手术夹闭。
3.术中注意
(1)治疗的关键是准确闭塞或切除瘘口及畸形团。栓塞要恰好闭塞瘘口和静脉起始端,否则易致瘘口复发。阻塞动静脉分流既可通过栓塞AVF,也可通过栓塞引流静脉起始段的几厘米以诱导瘘道内逆行血栓形成来完成。NBCA是实现这一目的的最好的栓塞剂。
(2)注射NBCA时,应避开或确认没有与脊髓前动脉同干发出。若在同一根动脉既有硬脊膜动脉,同时又发出脊髓动脉,被认为是栓塞禁忌,栓塞极易损伤脊髓动脉。
术后给予抗凝治疗,以减缓引流静脉内血栓形成与发展,促进静脉侧枝循环的开放,降低脊髓静脉压力,以促进神经功能恢复。
一般在治疗第一天或几周内即有明显改善,首先运动功能逐渐恢复,然后感觉障碍好转,括约肌功能恢复需一段时间,如果3个月仍无改善,需造影复查,以寻找新的瘘口。
(四)椎体血管畸形(又称椎体血管瘤)
1.血管造影特征 椎体血运丰富伴有扩张的小动脉,血流速度快,密度增高,椎体内有多个血窦样结构,没有早期静脉引流,应注意辨认在病变水平有无ASA。
2.治疗 手术切除是唯一最有效的手段,术前经肋间动脉行固体栓子栓塞可明显减少术中出血。
(五)椎旁血管畸形
1.Cobb’s综合征 又称为脊柱节段性血管瘤病,其诊断应具备以下四条中的三点:在同一椎体节段出现①髓内血管畸形;②椎管内硬膜外血管瘤;③椎体及椎旁血管瘤;④皮肤或皮下组织血管瘤、褐色痣或片状咖啡色斑。本病多见于青年人,多发生于胸段。
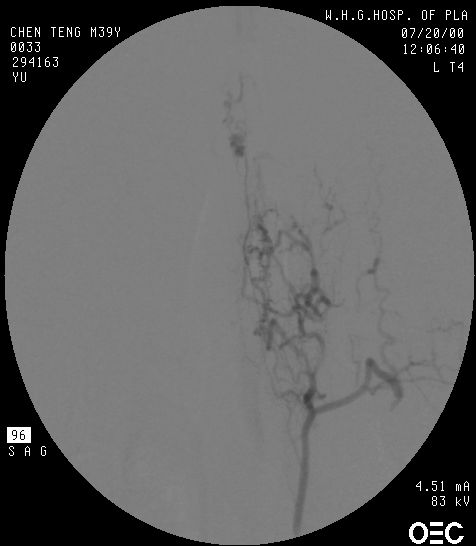
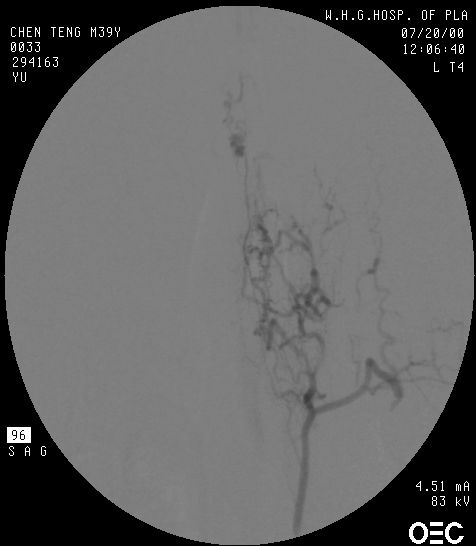
(1)血管造影特征:可确认三个主要方面。①髓内血管畸形:由脊髓前、后动脉发出多支沟联合动脉弥散状供血;②髓周血管畸形:多表现为髓周动静脉瘘,血管造影表现为在瘘口处有血管管径的突然增粗,引流静脉迂曲扩张;③椎体血管瘤及椎旁AVM:椎体血管瘤在造影时可见造影剂呈四方形样浓集,类似椎体形状。椎旁可见大范围扩张迂曲的畸形血管,此即椎旁AVM。在造影时应尽可能多地选择脊髓动脉造影以免遗漏病变(图24-3-4)。
(2)治疗:Cobb’s综合征病变范围广泛,不同的病变以不同机理影响脊髓功能,因此在治疗时也应有针对性的重点。如椎体血管瘤形成脊髓压迫则应重点治疗椎体病变,如果椎旁AVM广泛,引起脊髓动脉盗血和继发性椎管内静脉高压则应重点治疗椎旁AVM。血管内治疗闭塞畸形血管可获得减轻正常脊髓盗血,降低椎管内静脉高压,缩小病变体积,减轻占位效应等多方面的治疗效果,从而减少病变血供,显著改善脊髓功能。
(3)术中要点:针对不同病变采用不同的治疗策略。
1)髓内AVM:栓塞材料首选固体栓子,次选NBCA。因为一般导管很难达到畸形边缘,所以NBCA很少能采用,而固体栓子则随优势血流到达病变。注意不要强求一次栓塞达到“解剖学治愈”的目的,这样有可能使脊髓主干供血动脉闭塞。②髓周AVF:尽可能在瘘口处闭塞,这样,术后复发的可能性会大大降低[5]。③椎旁或椎体的血管畸形通常范围广泛,血流量大。采用先注射真丝线段,降低血流,再注射较高浓度的NBCA,闭塞畸形血管团或以微弹簧圈闭塞供血动脉的方法可获得较好的疗效。在整个治疗过程中应注意超选择插管到畸形血管的供血动脉内,否则会误栓脊髓供血动脉,引起功能障碍。
因病变累及范围广,通过栓塞或手术完全根治均不大可能,且病变有复发的机会,常需多次治疗。据认为有的病变在最初造影时并不显示,待主要畸形血管闭塞后,使潜在病变血流灌注增多或侧枝循环开放,因而显现并出现新的临床表现。
2)Rendu-Osler病(先天性出血性毛细血管扩张症) 血管造影可以发现全身的皮肤-粘膜血管瘤;脊髓血管瘤可发生在颈、胸、腰、骶的任何阶段。所有病变均可用栓塞治疗。
(六)椎管内静脉高压综合征
椎管内静脉高压的概念于1973年由Aboulker最先提出,是由于脊髓 引流静脉回流受阻或椎管外静脉血逆流入椎管静脉系统所致的椎管内静脉系统压力增高、循环减慢而产生的脊髓功能受损的一组综合症状,又称之为椎管内静脉高压综合征。此种情况见于①脊柱及脊髓血管畸形;②后颅窝硬膜动静脉瘘;③椎动静脉瘘。④左肾静脉、下腔静脉、奇静脉狭窄等。
1.选择性脊髓血管造影是确诊本综合征最有价值的方法,可显示病变的部位、类型、瘘口大小、供血动脉的来源、数目、引流静脉的方向与粗细、循环时间延长等;
对因左肾静脉、下腔静脉与奇静脉狭窄引起者及其增粗扩张情况,有时还需经股静脉插管到下腔静脉,再插入左肾静脉、奇静脉了解狭窄的具体部位及狭窄程度(图24-3-5)。
2.治疗 对不同病因所致者,其治疗重点应有不同。
(1)对所有的AVF均应闭塞瘘口,如超选择插管到达瘘口附近,可注入NBCA胶、恰在瘘口处将供血动脉与瘘口闭塞,切不可将引流静脉闭塞。或手术夹闭瘘口也可取得满意效果,术中切不可将引流静脉当畸形血管团切除。因为这些扩张的引流静脉都具有正常的引流脊髓本身静脉血的功能。
(2)对Cobb’s综合征引起者,应在充分栓塞的前题下手术切除硬脊膜外血管瘤,在栓塞椎旁血管瘤时,切勿栓塞可能从血管瘤供血动脉发出的根动脉,以防脊髓供血受损。
(3)对左肾静脉狭窄或奇静脉狭窄引起者,应行狭窄静脉段切除、重新吻合或自体肾移植,恢复正常的静脉回流。
(王启弘 马廉亭)
参考文献
1. 马廉亭 主编.微侵袭神经外科学.北京:人民军医出版社,1999.444-451
2. 徐国政,马廉亭,余泽,等.自发性脊髓蛛网膜下腔出血的病因和治疗方法探讨. 中华神经外科杂志 1994; 10(2): 68-69
3. 薛庆澄 主编. 神经外科学. 天津:天津科学技术出版社,1990. 648-649
4. 高绪文 郑明新 主编. 临床脊髓病学. 北京:人民卫生出版社,1997. 339-340
5. Touho-H, Karasawa-J, Ohnishi-H, et al. Intravascular treatment of spinal arteriovenous malformations using a microcatheter--with special reference to serial xylocaine tests and intravascular pressure monitoring. Surg-Neurol. 1994 ; 42(2): 148-56
6. 白如林, 张光霁, 朱诚,等.脊髓动静脉畸形血管内栓塞治疗. 中华神经外科杂志 1998; 14(5): 306-308
7. Barrow-DL, Colohan-AR, Dawson-R, et al. Intradural perimedullary arteriovenous fistulas (type IV spinal cord arteriovenous malformations). J-Neurosurg. 1994 ; 81(2): 221-9
8. Lee-TT, Gromelski-EB, Bowen-BC, et al. Diagnostic and surgical management of spinal dural arteriovenous fistulas. Neurosurgery. 1998; 43(2): 242-6; discussion 246-7
9. Marey-J, Pego-R, Alonso-G, et al. Endovascular treatment of dural arteriovenous fistulas with medullary venous drainage. Experience with 18 patients. Rev-Neurol. 1998 ; 26(153): 793-9; discussion 799-800
10. Hurst-RW, Bagley-LJ, Marcotte-P, et al .Spinal cord arteriovenous fistulas involving the conus medullaris: presentation, management, and embryologic considerations. Surg-Neurol. 1999; 52(1): 95-9
11. Westphal-M, Koch-C. Management of spinal dural arteriovenous fistulae using an interdisciplinary neuroradiological/neurosurgical approach: experience with 47 cases. Neurosurgery. 1999; 45(3): 451-7; discussion 457-8
12. 凌 锋 李铁林 主编.介入神经放射影像学.北京:人民卫生出版社,1998.348-356
13. Ide C, Gangi A ,Rimmelin A , et al. Vertebral haemangiomas with spinal cord compression: the place of preoperative percutaneous ventebroplasty with methyl methacrylate .Neuroradiology, 1996;38:585
14. Shin-ichi M, Haruhiko K , Tomoaki K , et al . Cobb’s syndrome and its treatment with embolization. J Neurosurg, 1990; 72:497.
马廉亭 教授 广州军区武汉总医院神经外科(430070)
本文是王启弘版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅










评论