 三甲
三甲
【国人临床+基础研究红毯秀】角膜上皮的“逆袭”!齐虹教授团队证实角膜上皮细胞在干眼中的主动抗炎机制
编者按
眼表炎症与损伤被干眼工作小组II (Dry Eye Workshop II,DEWS II)列为干眼四大发病机制之一。干眼状态下,角膜上皮是眼表炎症攻击的对象,然而,角膜上皮能够自我抵抗干眼炎症吗?
国人SCI新鲜出炉:北京大学第三医院眼科齐虹教授带领团队于The Ocular Surface上发表文章,证实干眼状态下,角膜上皮可主动上调保护性蛋白PEDF的表达,从而在干眼中发挥抗炎与免疫保护作用!
不是单纯“挨打”,角膜上皮也能“逆袭”
近20年的临床与基础研究表明,干眼炎症是眼表免疫异常导致的慢性非感染性炎症。其中Th17细胞的活化与眼表浸润发挥重要的致病作用。
角膜上皮直接与泪膜相接触,是干眼发病过程中的核心组织之一。近年来,多项研究与综述指出,角膜上皮在干眼中不仅是受损组织,而且可通过表达多种免疫调节分子主动发挥负向免疫调控作用以抑制干眼的发生发展,而色素上皮衍生因子(Pigment epithelium-derived factor, PEDF)就是其中之一。
PEDF是Tombran-Tink J教授等人在1989年首次在人体视网膜色素上皮细胞的培养基中发现的,而后眼科学者发现角膜上皮细胞、睫状体色素上皮细胞、神经节细胞、内核层细胞中均有PEDF的高表达。研究发现PEDF除了具有神经保护、抗血管生成作用外,还发挥着抗炎的作用。
齐虹教授团队阐明PEDF在角膜上皮主动抗炎中的作用机制
齐虹团队通过横断面临床研究中发现:干眼患者泪液中的PEDF表达水平较正常人增高,并与干眼临床指标OSDI、TBUT呈现相关性,提示PEDF可能在干眼中发挥重要作用。

以此为出发点,团队进行了体内实验与体外实验来阐明干眼条件下PEDF在眼表的表达情况及其抗炎作用机制。
重要结果:
(1)研究发现,在正常小鼠中,PEDF主要在角膜上皮、结膜上皮包括杯细胞中表达。但在干眼条件下,升高的PEDF来自于角膜上皮细胞。
(2)泪液渗透压升高、眼表炎性反应都是干眼的主要病理生理机制之一,究竟角膜上皮细胞PEDF的表达增加因谁而起呢?本研究发现,给予高渗刺激下,人角膜上皮细胞的PEDF表达增加;而给予炎症因子刺激,PEDF表达反而下降。
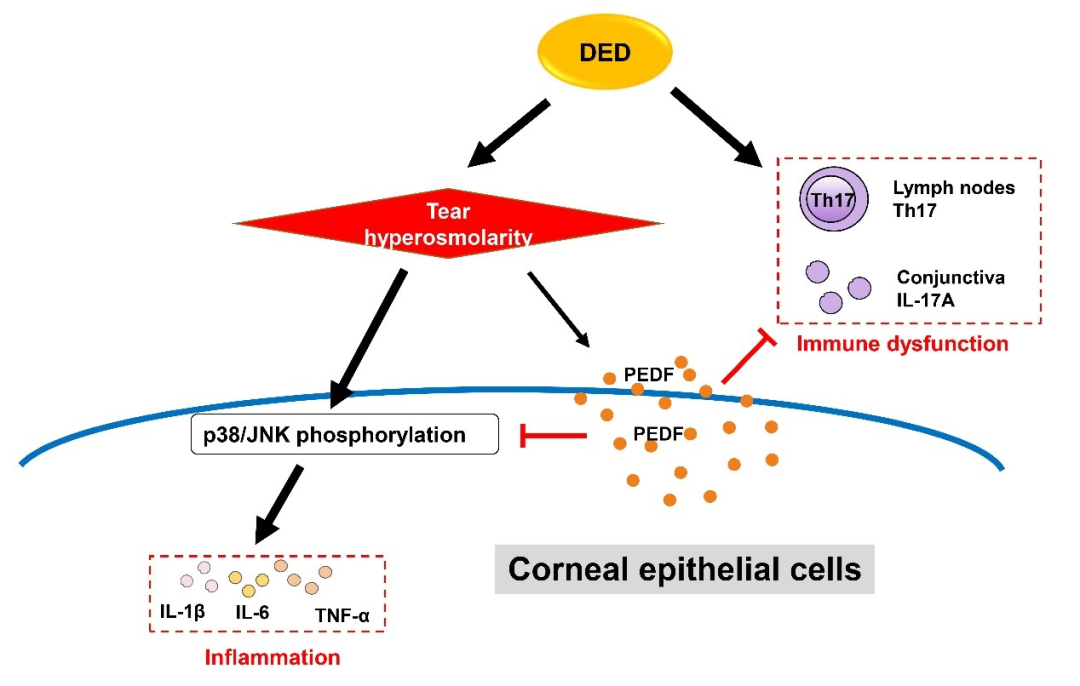
(3)团队在体内实验中,通过采用PEDF重组蛋白以及PEDF中和抗体的方式,证实PEDF缓解干眼小鼠角膜上皮损伤,抑制干眼小鼠眼表炎症因子(IL-1β、IL-6、TNF-α及IL-17A)的表达,并且减少引流淋巴结Th17细胞的比例。
(4)体外实验证实PEDF通过抑制p38及JNK磷酸化从而在降低高渗状态下hCECs的炎性因子表达。
总结来说:
本研究表明,干眼状态下角膜上皮细胞PEDF受泪液高渗刺激发生代偿性的表达增高,从而抑制致病性免疫细胞和免疫分子,主动抵抗干眼炎症。
该研究的临床意义
眼表微环境实质上是一个“微社会”。在干眼状态下,眼表组织受损而影响自身功能,但组织中也存在众多保护性因子。这些保护性因子作为安全卫士,可以发挥主动防御作用。本研究利于我们拓宽对干眼状态下眼表组织作用的认识,这些保护性因子也是很有潜力的干眼治疗方向。
课题组研究方向
齐虹教授在干眼免疫与神经调控领域已深耕10余年。本文是齐虹教授课题组继2019年于American Journal of Ophthalmology发文阐明糖尿病干眼患者泪液免疫学特征后的又一力作。在此过程中,团队参考国内外现状,对干眼小鼠模型进行了多方面改进,使得模型更高效稳定,目前已获批实用新型专利一项(ZL 202020578318.9)。

齐虹教授团队在眼表领域潜心耕耘20余年,临床积累丰厚,科研基础坚实。在眼表疾病的诊疗中,紧跟国际前沿进展,不断开拓进取,为干眼的诊疗提供精准化定位。
本文为转载文章,如有侵权请联系作者删除。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论