儿童神经母细胞瘤(NB)诊疗专家共识 CCCG-NB-2021 方案
儿童神经母细胞瘤诊疗专家共识 CCCG-NB-2021 方案
Expert consensus on diagnosis and treatment of neuroblastoma inchildren CCCG-NB-2021 regimen
中国抗癌协会小儿肿瘤专委会中华医学会小儿外科分会肿瘤学组

儿童肿瘤的放射治疗(radiotherapy)/放疗(RT)原则
1例(男/4岁)纵膈神母(骨Mstage IV)术后化疗后移植状态放疗-TOMO超分割放疗-南京返回
4岁男孩右侧纵膈神母(多发骨转移,stage IV)自体干细胞移植后-TOMO放疗-返回自-济南
1例(男/2岁)骶尾部神经母细胞瘤两次手术后化疗后放疗-TOMO放疗+深部热疗
复发性纵膈神母1例(女,2岁;初诊时29天,初始分期为:II期低危)报告并文献复习-TOMO放疗
复发性-左肾上腺-神经母细胞瘤-2岁11月龄(<3岁,小于3岁,神母)1例报告并文献复习-北京
1例IV期(男/5岁2月)右肾上腺神母(骨转移并骨髓侵犯)报告并文献复习-TOMO放疗-来自-荆州
穿潜水衣/1例(男/5岁)B系急淋-全皮肤+全骨髓+海马保护全中枢+全淋巴结+睾丸保护-TOMO放疗
神经母细胞瘤(Neuroblastoma,NB) 占儿童恶性肿瘤的 8-10%,死广率却达 15%,其生物学行为多样,病因复杂,尤其高危神经母细胞瘤,肿瘤异质性更为明显,制定多中心、多学科诊疗共识显得尤为重要。
国际上开展的多中心临床试验结果,逐步地改善了神经母细胞瘤预后,目前高危神经母细胞瘤治愈率也提高到 50%左右。但由于国际上各 NB 协作组织采用的危险度分层各有侧重,导致部分病例临床分析结果会存在差异。
国际神经母细胞瘤危险度分组(INRG) 组织制定的基于影像学定义的危险因子 (Image-defined risk factors,IDRFs)的治疗前分期和危险度分组方案,考虑到治疗前评估及手术策略的相关因素,有利于各分组间临床比较,目前被越来越多的临床及研究机构所采用。
高危组治疗方案
高危组治疗方案
推荐意见 5:
综合治疗是高危组治疗策略,随着干细胞移植、放疗、免疫治疗等治疗的不断成熟,依据 COG ANBL0532 等相关临床试验结果,CCCG-NB-2021 方案,同样将高危组诱导化疗疗程从 8 个疗程减至 6 个疗程,与 COG 诱导期化疗方案一致,CTX 剂量也依据 COG 方案进行调整。(证据等级: A;推荐强度:强)
治疗计划:
包括三个阶段,即:诱导期(包括化疗和手术)、巩固期(序贯移植及针对原发肿瘤以及残余转移部位的放疗) 和巩固期后维持治疗(免疫治疗和 13-cis-RA)。先化疗 2 周期后,进行自体外周血干细胞采集,后继续化疗2 周期后择期手术。术后化疗2 个疗程,总疗程不超过 6 个疗程。
常规化疗结束后自体干细胞移植和放疗剂量为 21.6Gy 的瘤床放疗(推荐行序贯自体干细胞移植,瘤床放疗在两次自体干细胞移植之间进行) 。后进行 GD2 单抗免疫治疗联合 GM-CSE 和 13-cis-RA 治疗。
2.巩固期(造血于细胞移植及针对原发肿瘤以及残余转移部位的放疗)
2.1 造血干细胞移植
推荐意见 7:
自体外周血造血干细胞移植可选择单次移植和序贯移植两种方案之一的方式进行,推荐具有较好疗效的国际多中心临床研究预处理化疗方案,单次移植 MM 方案,序贯移植 COG的 T/C (#1) & CEM (#2)方案。(证据等级: A; 推荐强度: 强)
放射治疗原则
2.2 放射治疗原则
推荐意见 8:
高危组患者原发灶放疗是必不可少的治疗手段,可提高局部控制率。放疗剂量为 21.6Gy 的瘤床放疗。 (证据等级: A;推荐强度: 强)
2.2.1 适应症
低危组
仅有极少数病例,当病变复发且无法行手术和化疗时,或者肝脾肿大抑制呼吸或脊髓压迫等急诊情况下可考虑放疗。
中危组
放疗仅限于手术或化疗后疾病进展或化疗后肿瘤持续残留患者。
高危组
原发灶瘤床和化疗后持续性转移灶应采用放疗提高局部控制率。
2.2.2 放疗靶区
1) 术区放疗
术后放疗靶区由术前影像学表现和手术医师术中描述共同决定。如影像学或手术病理证实的淋巴结转移,则照射野不仅包括原发病灶部分,还要包括引流的淋巴结区域,如照射野必须包括一部分椎体,则应将整个椎体包括在照射野内,以减少脊柱侧弯的可能
2)转移灶放疗
超过 50%新诊断患儿已发生,并可能发生急症状况如眼眶转移造成视力受损、硬膜外转移引起的髓压迫,或骨转移造成严重疼痛。放疗可有效缓解骨和软组织转移引起的症状。
2.2.3 放疗剂量
目前大对数研究机构认可 21.6Gy/14f BID 或21.6Gy/12f QD 的剂量分割模式,大体残留肿瘤局部可推量到 30~36Gy。
2.2.4 放疗技术
早期的研究结果都基于二维放疗技术,目前适形调强放疗(IMRT) 已经成为放射治疗的主流,IMRT、Proton 等放疗技术与二维技术比较,可提供更好的靶区适形度同时显著减低包括肾脏在内的危及器官受量。
2.2.5 放疗副反应
急性反应包括胃肠道系统、神经系统、泌尿系统和骨髓抑制等。远期毒性主要为对骨骼肌肉系统的生长抑制和第二肿瘤。


3.维持治疗(抗 GD2 免疫治疗和维甲酸治疗)
推荐意见 9:
免疫治疗是近年对高危疗效提升贡献很大的治疗手段,应该尽快利用已知的国外临床试验结果,开展国内临床研究,充分发挥免疫治疗药物的作用。(证据等级: A;推荐强度: 强)
GD2(双唾液酸神经节苷脂) 是一种在的细胞外膜中存在的表面抗原,是免疫治疗的理想靶点。GD2 单抗与其结合后,主要通过激活抗体依赖性细胞介导的细胞毒性(ADCC)和补体介导的细胞毒性(CDC),使肿瘤细胞裂解和死亡。
GD2 抗体是针对高危的免疫靶向药物,是近十年来高危神经母细胞瘤治疗的重要进展。GD2 抗体已经在美国以及欧盟等国家获批上市,成为高危多模式治疗中不可或缺的一部分。目前,国际已有三款获得FDA 批准的 GD2 抗体,分别是 Unituxin (dinutuximab)、Qarziba(dinutuximab beta),以及 Danyelza (naxitamab) 。
其中, Qarziba (dinutuximab beta)国内已获批上市,
其适应症为:
①治疗>12 月龄的高危患儿,这些患者既往接受过诱导化疗且至少获得部分缓解,并且随后进行过清髓性治疗和干细胞移植治疗:
②治疗伴或不伴有残留病灶的复发性或难治性。在治疗复发性之前,应采取适当措施使活动性进展性疾病保持稳定。
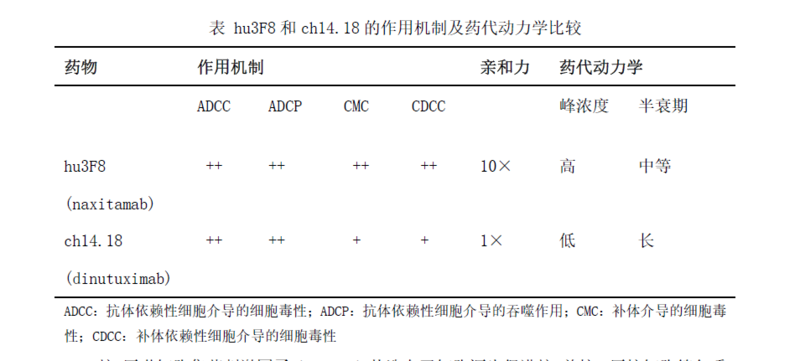
粒-巨噬细胞集落刺激因子(GM-CSF) 从造血干细胞源头促进粒-单核、巨核细胞等各系细胞生成,作用位点高且广。GM-CSF 能促进树突状细胞分化增殖,增强抗原提呈作用,放大机体免疫效应。同时单核细胞在 GM-CSF 作用下分化为M1 型巨细胞,从而抑制肿瘤,抵抗感染。因此 GM-CSF 作为免疫促进剂,可以提升患者体内的免疫细胞数量,增强其活性,进而发挥更强的攻击靶细胞作用。
国外文献报道,GD2 单抗联合 GM-CSF 应用能为高危患儿生存带来获益。另外,高危患儿自体干细胞移植后维持治疗,GD2 单抗联合 IL-2 应用并未改善疗效,且增加了毒副作用发生。
高危维持治疗阶段 GD2 抗体使用方法一般为每 35 天一疗程,计划应用5 疗程,并联合GM-CSF 及维用酸。

本文是曾辉版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论