 三甲
三甲
耿鑫
副主任医师
昆明医科大学第一附属医院
神经外科
糖尿病神经损伤的分子机制
190人已读
糖尿病神经病变(Diabetic Neuropathy, DN)是一种由糖尿病引起的常见并发症,主要表现为周围神经和自主神经的损伤。其发生机制复杂,受多种因素的影响,包括高血糖、氧化应激、缺氧、炎症反应等。以下将详细阐述糖尿病神经损伤的各种机制,尤其是缺氧机制。
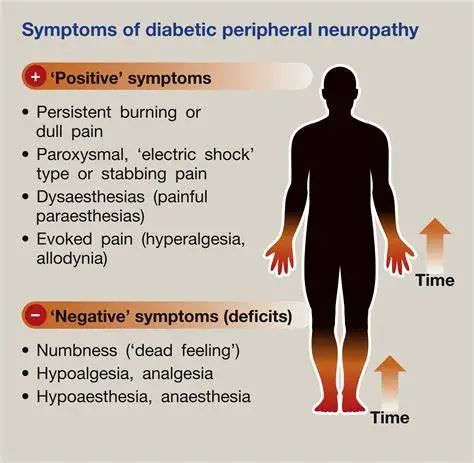
一、高血糖的影响
高血糖是糖尿病患者最明显的病理特征,长期的高血糖状态会导致多种代谢紊乱,进而引发神经损伤。
- 糖基化终末产物(AGEs)
- 高血糖会促进糖基化反应,生成AGEs。这些物质能够与细胞表面的受体结合,激活各种信号通路,如NF-κB通路,导致细胞的炎症反应增强,并造成神经细胞的毒性。
- 多元醇途径
- 在高血糖条件下,葡萄糖通过醛糖还原酶转化为甘露醇,从而促使神经细胞内多元醇累积,导致细胞功能障碍,并引发细胞凋亡。
- 氧化应激
- 高血糖状态会增强氧化应激,产生大量的活性氧(ROS),损伤神经细胞,导致细胞膜、蛋白质和DNA的氧化损伤。
- 微血管病变
- 糖尿病可导致微血管(如小动脉和小静脉)的损伤,影响血液流动。小血管的损伤会引起氧气和营养物质供应的不足,进而导致神经细胞缺氧。这种缺氧状态在糖尿病患者的周围神经组织中非常常见。
- 缺氧诱导因子(HIF)
- 缺氧时,缺氧诱导因子(HIF)表达上升,导致细胞产生一系列保护机制以应对缺氧。例如,HIF可诱导血管新生和耐缺氧基因的表达,帮助神经细胞适应缺氧环境。但在长期缺氧状态下,HIF的持续激活可能造成细胞的损伤和凋亡。
- 线粒体损伤
- 缺氧还会导致线粒体损伤,使能量产生下降,神经细胞的代谢能力降低。缺乏能量会使神经细胞对损伤的抵抗能力下降,进一步加重神经损伤。
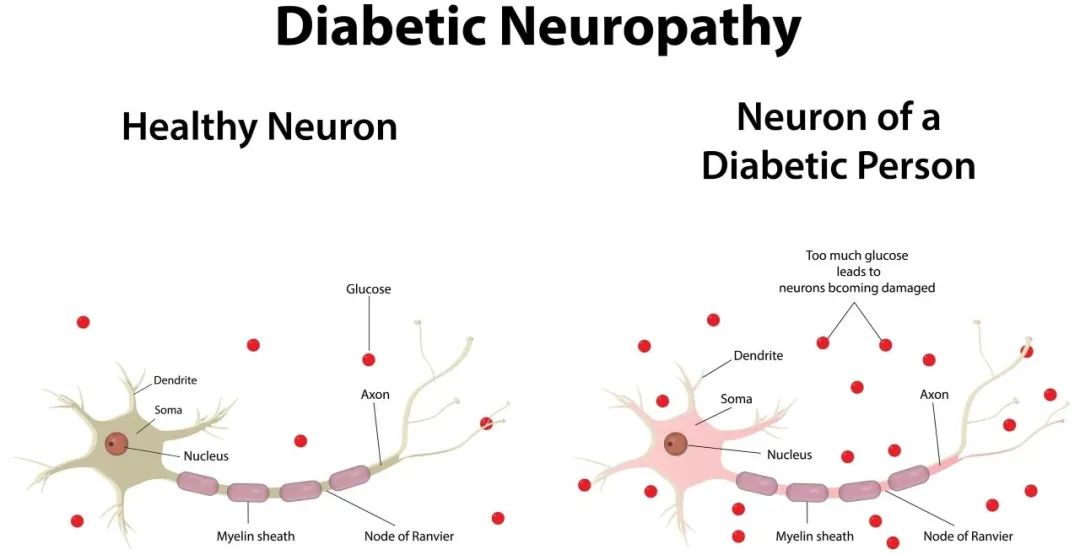
二、缺氧机制
缺氧可以视为糖尿病神经损伤的一个重要间接机制,尤其是在糖尿病导致的微血管病变中。
三、炎症反应
炎症反应在糖尿病神经损伤中起着重要的作用。
- 巨噬细胞活化
- 糖尿病引发的慢性低度炎症可激活神经系统中的巨噬细胞,释放多种促炎细胞因子,如TNF-α和IL-6。这些因子会导致神经细胞的损伤和功能障碍。
- 神经胶质细胞反应
- 神经胶质细胞在炎症反应中起重要作用。糖尿病时,神经胶质细胞的活性增加,但这种活化往往伴随有细胞的凋亡和功能异常,进一步加剧神经损伤。
- 活性氧(ROS)的产生
- 糖尿病患者的体内会产生大量的活性氧,超出机体的抗氧化能力,导致细胞损伤。ROS会通过氧化损伤脂质、蛋白质和DNA,最终导致细胞减弱或死亡。
- 抗氧化防御系统的失衡
- 在糖尿病情况下,抗氧化防御系统的功能下降,这包括抗氧化酶(如超氧化物歧化酶、过氧化氢酶等)的活性降低,导致细胞对氧化损伤的抵抗能力减弱。
- 甘油三酯和游离脂肪酸
- 糖尿病患者中,甘油三酯和游离脂肪酸水平往往升高,这些物质能够通过多种机制对神经细胞产生毒性作用,包括诱导细胞凋亡和促进炎症反应。
- 代谢产物累积
- 糖尿病引起的代谢紊乱会导致有毒代谢产物的累积,如疏水性氨基酸和胺,有可能对神经组织造成直接的损伤。
- Ziegler, D., et al. (2015). “Diabetic neuropathy: pathophysiology and clinical management.“ The Lancet Diabetes & Endocrinology, 3(10), 827-837.
- Tesfaye, S., et al. (2013). “Diabetic neuropathy: update on the management.“ The Lancet, 383(9923), 2127-2137.
- Sima, A. A. F., & Calhoun, M. (2010). “Diabetic neuropathy: mechanisms and therapeutic targets.“ Journal of Diabetes Science and Technology, 4(5), 1064-1074.
- Apfel, S. C., et al. (2003). “Diabetic neuropathy: mechanisms and management.“ Molecular Pain, 8(1), 10-16.
- Brownlee, M. (2005). “The pathobiology of diabetic complications: a unifying mechanism.“ Diabetes, 54(6), 1615-1625.
四、氧化应激
氧化应激是糖尿病神经损伤中的另一个重要机制。
五、神经毒性物质
高血糖状态下,体内的代谢产物也会增加,对神经细胞造成毒性。
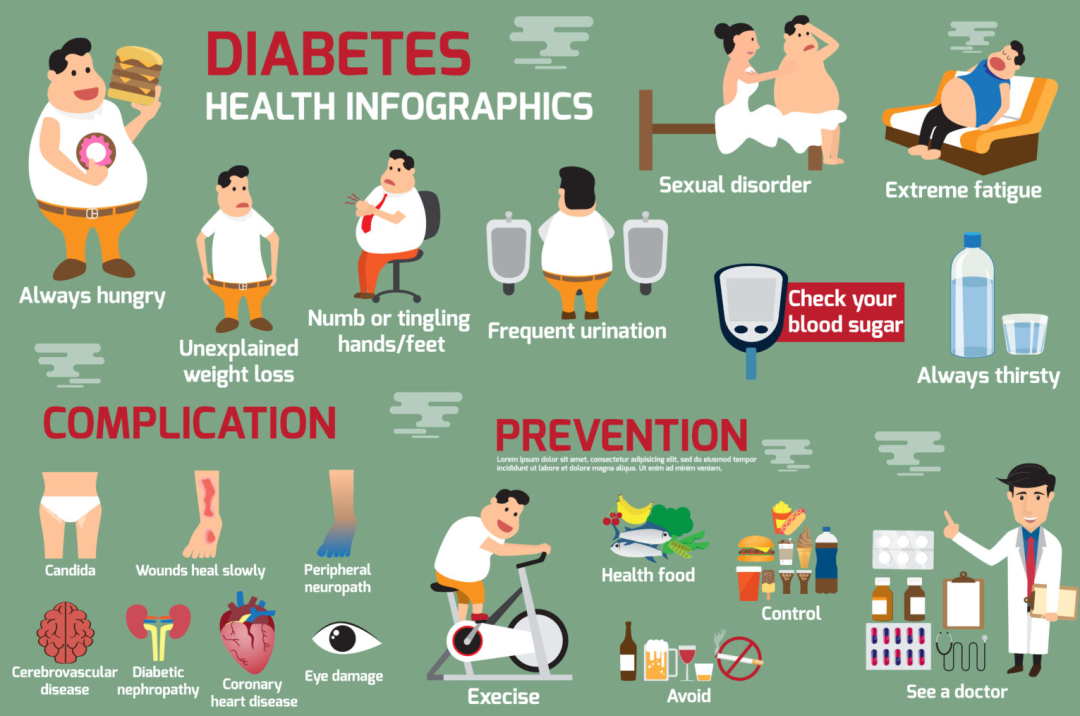
小结
糖尿病神经损伤的机制是多因素的,包括高血糖、缺氧、氧化应激、炎症反应、以及神经毒性物质等。缺氧在微血管病变的背景下,作为一种间接机制,加剧了神经的损伤。有效的干预措施应关注血糖控制、氧化应激的降低、炎症的抑制等,以期帮助糖尿病患者减轻神经损伤的风险。
参考文献
本文为转载文章,如有侵权请联系作者删除。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论