 三甲
三甲
免疫系统用药靶点梳理
免疫系统用药靶点梳理
01
T细胞重要靶点IL2R、IL6R、IL17、JAK1/TYK2是主要开发方向。
针对T细胞的靶点包括白细胞介素(IL)类、TNF-α、CD40/CD40L及JAK家族等。其中白细胞介素(IL)类靶点包括IL1、IL2、IL6、IL17及IL23等。
针对细胞表面受体及分泌性细胞因子(IL及其受体、TNF-α以及ITG等),通常开发抗体类药物作为治疗手段;而细胞内的蛋白靶点(JAK家族、PDE4以及AHR)通常以小分子抑制剂作为治疗手段。

图1 T细胞免疫靶点关系和抑制剂开发
02
体液免疫重要靶点针对B细胞的靶点包括CD20、补体系统以及FcRn等。其中CD20蛋白位于B细胞质膜表面,针对CD20的抗体能直接诱导免疫系统对于B细胞的杀伤,在血液瘤和自身免疫病治疗中有广泛应用。FcRn位于内皮细胞表面,能够结合并延长引起自身免疫性疾病的抗体的半衰期。通过单抗靶向补体系统的蛋白,可以减少补体系统对自身组织细胞的杀伤。

图3 B细胞免疫靶点关系和抑制剂开发
03
自身免疫疾病主流靶点表1 自身免疫疾病主流靶点

IL-1增强T细胞的局部再活化,提高效应功能发挥
自免性脑脊髓膜炎中,免疫细胞产生IL-1β,与其受体IL-1R1结合,促进可溶性趋化因子(CCL2,CXCL1,CXCL2,CXCL5)和细胞因子(IL-6,G-CSF和GM-CSF)表达,血脑屏障通透性增加,并刺激产生更多IL-1β,从而形成一个正反馈回路,可增强T细胞的局部再活化及其效应功能的发挥。
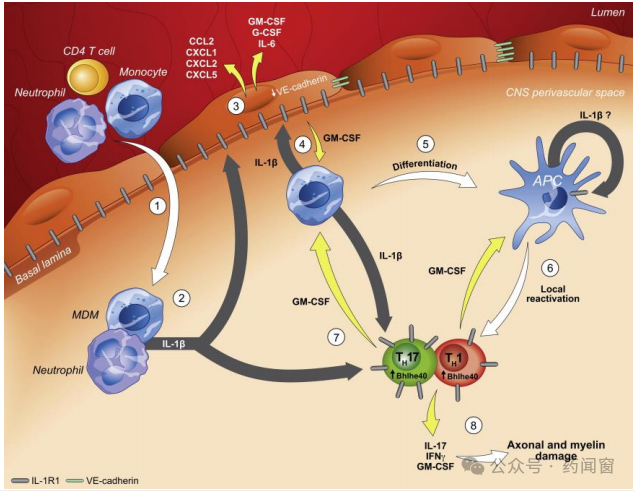
图1 IL-1β作为自免性疾病药物靶点的作用通路
IL-2对T细胞活化起双重作用
IL-2是第一个被分子克隆的细胞因子,对T细胞的增殖和效应细胞和记忆细胞的产生至关重要,其最早的治疗应用是增强癌症患者的免疫反应。近来,使用IL-2、针对IL-2的单克隆抗体或IL-2变体的疗法正在开发中,其通过增加Treg细胞的数量和功能以调节免疫细胞的数量和功能,从而治疗自身免疫性疾病。

图2 IL-2在自免性疾病中对T细胞活化的双重作用
IL-6、IL-6R多个药物上市,研究前景广泛
西鲁库单抗、司妥昔单抗、奥洛组单抗、克拉扎珠单抗通过与IL-6结合从而抑制其信号通路。而托珠单抗、沙利鲁单抗则直接作用于IL-6受体。

图3 IL-6、IL-6R作为自免性疾病药物靶点的作用机制
IL-4与IL13共享部分受体,相关抗体可同时抑制两者
IL-4Rα是IL-4与IL-13信号通路中的重要组成部分,参与这两种白细胞介素的受体组装(图中蓝色部分)。IL-4Rα在免疫反应中主要激活JAK-STAT通路,引起Th等的活化。1-3型IL-4受体以及1型IL-13受体均有IL-4Rα作为组分。在哮喘、系统性红斑狼疮以及特应性皮炎等多种免疫疾病中均有参与。同样,IL-13Rα1(图中红色部分)也参与多种受体装配。
一般而言,造血系统中的免疫细胞表达1型IL4受体较多,而血液循环细胞及组织驻留细胞主要表达2型IL4受体。IL-4更多地在造血系统中发挥作用,也促进Th2型免疫反应和B细胞的活化。而IL-13主要激活外周组织中的细胞,在调节上皮细胞和巨噬细胞的抗炎反应中起作用。这也是作用于游离IL-4药物较少的原因之一。
知名免疫类药物度普利尤单抗即是以IL-4Rα为靶点。同靶点药物还有司普奇拜单抗、曼多奇单抗和QX005N等。而来金珠单抗等特异性结合可溶性IL-13的药物,也是通过阻断IL-4Rα而抑制免疫反应,在治疗特应性皮炎等方面发挥作用。

图4 IL-4、IL-13及其受体作为自免性疾病药物靶点的作用机制
IL-12、IL-17、IL-23个药物上市,研究前景广泛
乌司奴单抗通过与IL-12、IL-23的p40蛋白结合,古塞奇尤单抗、替拉珠单抗、瑞莎珠单抗、布雷库单抗、米吉珠单抗通过与IL-23的p19蛋白结合,从而阻断其信号通路,抑制Th1、Th17细胞的分化。苏金单抗、依奇珠单抗与IL-17结合以阻止其与IL- 17R结合,布达鲁单抗则通过与IL-17竞争受体,从而抑制该信号通路下游。
从目前的药物临床开发成果来看,靶向p19的药物如匹康奇拜单抗和古塞奇尤单抗,效果好于靶向p40的乌司奴单抗。

图5 IL-12、IL-17、IL-23作为自免性疾病药物靶点的作用机制
TNF-α最早成药的靶点,市场潜力挖掘相对充分
α肿瘤坏死因子(TNF-α)是一种主要由单核-巨噬细胞产生的促炎细胞因子,广泛参与并激活机体的免疫反应。TNF-α不适当或过度激活与慢性炎症有关,并导致自身免疫性疾病的发展。针对TNF-α的药物主要为以阿达木单抗为首的各类单克隆抗体,广泛用于包括强直性脊柱、银屑病和炎症性肠病等自身免疫疾病的治疗。由于该类药物大部分开发时间较早,专利多已过期,市面上出现了大量仿制药竞争。

图6 TNF-α类药物作用机制
JAK新药研发不断加速,巨大潜力正在兑现
JAK家族激酶包括JAK1/2/3以及TYK2四位成员,主要通过激活下游STAT家族促进细胞存活与增殖。JAK家族能够刺激T细胞的存活与免疫功能,是自身免疫疾病治疗中的重要靶点。从十余年前首个JAK抑制剂托法替布开始,许多新药不断涌现,造就了百花齐放的竞争格局。其治疗领域包括斑秃、银屑病、特应性皮炎、炎症性肠病和类风湿关节炎等。

图7 JAK类抑制剂作用机制
ROCK2自免领域小众靶点,独具特色
ROCK2为Rho蛋白相关激酶的一种亚型。在T细胞中,与JAK家族成员类似地激活STAT3蛋白,刺激T细胞的增殖和免疫反应。
目前,ROCK2抑制剂在自身免疫病相关领域用于移植物抗宿主病的治疗。

图8 ROCK2抑制剂作用机制
CD20靶点常青树,广泛应用于免疫系统疾病治疗
CD20是一种在B细胞表面高度表达的糖蛋白。抗CD20抗体可通过抗体、T细胞或是程序性死亡等方式较为特异地杀伤B细胞,因此在血液瘤及自身免疫病等领域被广泛开发及应用。自1997年利妥昔单抗上市以来,已经出现了大量相关靶点的新药及仿制药。可用于天疱疮、狼疮肾炎和类风湿关节炎等疾病的治疗。

图9 CD20类药物作用机制
FcRn重症肌无力领域的新兴靶点
FcRn是一种位于细胞膜表面的IgG抗体受体,主要在内皮细胞中表达。FcRn通过结合IgG的Fc部分,阻止IgG在体内的自然代谢,延长了IgG的作用时间。通过靶向FcRn的药物可以促进IgG降解,起到治疗自身免疫疾病的效果。目前该类药物主要应用于重症肌无力治疗。

图10 FcRn类药物作用机制
C5前景广阔,自免领域应用有待发
补体系统是固有免疫的重要组成部分,参与人体免疫调节及免疫损伤性反应。补体成分5是补体系统级联反应的一环,激活后的C5可以促进炎症反应以及对于细胞的杀伤。目前,靶向C3、C5的药物已经在阵发性睡眠性血红蛋白尿、重症肌无力以及血管性水肿等疾病的治疗中得到了批准。

图11 抗C5类药物作用机制
IgE哮喘治疗成效显著,仿制药不断跟进
IgE是I型超敏反应中的关键性抗体,介导嗜碱性粒细胞和肥大细胞产生的免疫反应,也是哮喘和荨麻疹治疗中的关键靶点。
目前该领域唯一新药奥马珠单抗专利已经到期,大批仿制药厂商正在迅速跟进,也有部分新药正在进行关键性III期临床。

图12 抗IgE类药物作用机制
整联素组织差异性大,研发重点靶向肠道治疗
整合素是一类介导细胞粘附的受体超家族,与细胞外基质(ECM)配体和细胞表面配体结合以调控细胞生理活动。其中,α4亚基(又称ITGA4)与β7亚基(又称ITGB7)组成的α4β7整联素是负责肠道组织中淋巴细胞归巢的受体,淋巴细胞借助α4β7整联素进入肠道产生免疫反应。这两个亚基也因此成为了自身免疫性肠病治疗中的热门靶点。

图13 抗整联素类药物作用机制
PDE4银屑病领域重要靶点,适应症不断扩展
cAMP是细胞信号转导过程中重要的第二信使,负责在细胞内传递胞外信号,介导一系列生理过程。通常来说cAMP由G蛋白耦联受体激活产生,而被磷酸二酯酶(PDE)蛋白家族成员水解。在免疫细胞中,cAMP具有抑制细胞增殖和降低细胞因子分泌等作用。通过抑制水解cAMP的PDE4蛋白,可以增强免疫细胞内的cAMP浓度,治疗特应性皮炎、银屑病和银屑病关节炎。

图14 抗PDE4类药物作用机制
TSLP自免领域新兴靶点,前景可期
与IL-7在进化上具有同源关系,能够刺激T、B淋巴细胞的增殖与发育。该蛋白的基因在支气管上皮细胞、结肠上皮细胞以及肺成纤维细胞等中均有表达,是人类2型炎症的重要驱动因素。各种刺激因素如机械损伤、疾病和过敏原等都可能刺激上皮细胞释放TSLP,激活树突状细胞、肥大细胞或是辅助T细胞的免疫反应。目前相关药物主要用于特应性皮炎与哮喘治疗。

图15 抗TSLP类药物作用机制
自身免疫系统疾病靶点纷杂多样,除了TNF-a,其他靶点的市场应用价值尚未体现。
本文为转载文章,如有侵权请联系作者删除。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论