
光电与填充剂关系——文献与思考
光电设备与填充剂在医美治疗上是相辅相成的关系,在治疗上,先做光电治疗,再做各种填充,没有冲突。但是经常碰到做完填充后,再做光电,或者填充过度,或填充后有结节,需要用光电处理的,什么时候做光电,值得探讨的问题。本文就部分文献,做一点思考。
Jordan P. Farkas医生(1)选用6头母猪进行研究。每头小猪的腹部,在间隔1.5cm*1.5cm处,注射0.1-0.2ml的玻尿酸。用的品牌:铂金瑞蓝、瑞蓝丽瑅、乔雅登。两周后,小猪们注射过玻尿酸的地方再进行光电设备的治疗,具体的设备名称如下:
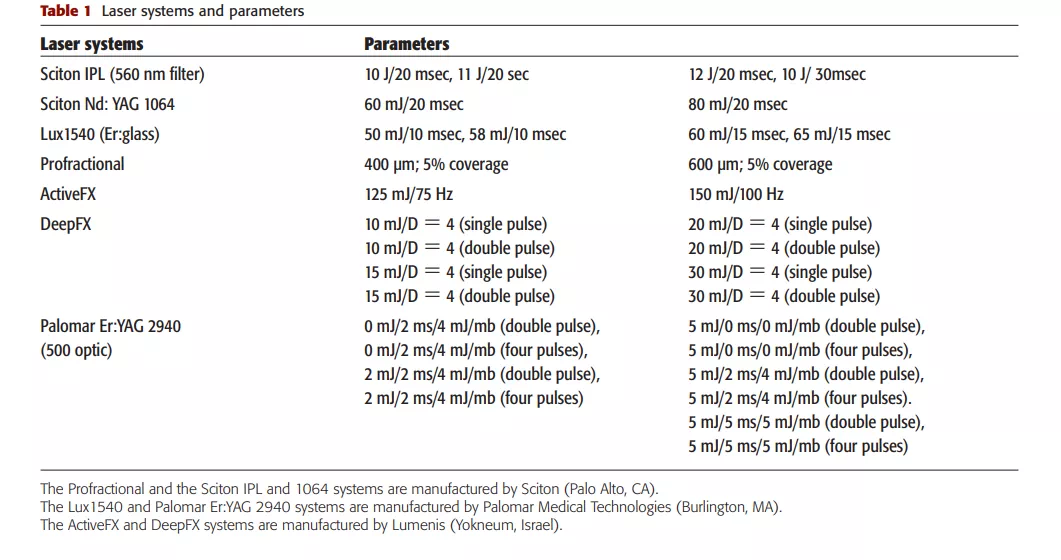
每个光电设备至少处理6个注射点。治疗结束后,立即对小猪实施安乐死,并对治疗区域进行组织学处理和评估。
最后的结果非常精彩。经激光治疗后,填充物无明显损伤、起泡、渗出或渗漏。此外,在组织学上,在任何预注射处理的标本中,没有观察到填充物周围有凝固或组织损伤的迹象。每一种不同的HA软组织填充物在每一个组织活检标本的真皮或皮下组织中都有被鉴定到。阿尔辛蓝染色有助于从周围真皮胶原和皮下脂肪细胞中清楚地识别填充物。每一个填充物都被鉴定为真皮或皮下组织内的一个离散的肿块,用阿尔辛蓝染上一个丰富的蓝色(如下图所示)。
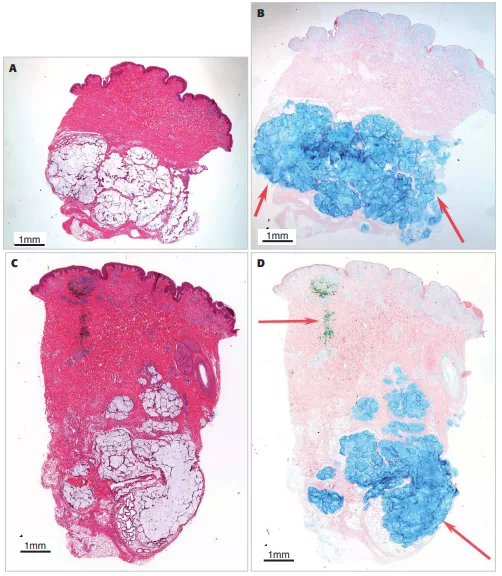
用Sciton IPL或1064处理的注射区域不会对软组织填充物造成任何形态学变化(见下图)。
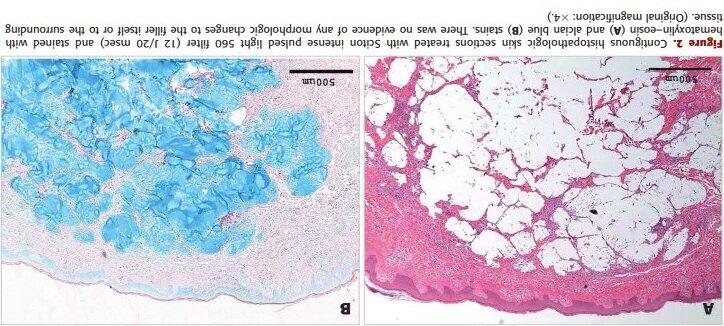
使用LUX154系统治疗后,观察到胶原的凝固微柱从表皮逐渐变细进入真皮乳头状。在使用ActiveFX设备治疗后,表面烧蚀坑明显,并从表皮延伸到真皮乳头状。在不同的能量设置下,这些装置对表皮和真皮乳头状的表面损伤和改变没有深入到真皮中,无法与填充物有接触(见下图)。
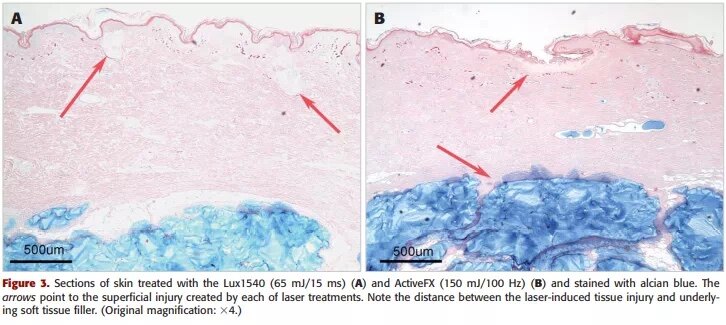
在用分次Er:YAG装置(Profraction,Palomar 2940)治疗后,观察到损伤的微清创柱从表皮穿透到真皮下的乳头状和网状真皮。部分微清管柱直接与真皮乳头状和网状真皮中的HAF相接触。一些微穿孔柱包围并困住了填充物(见下图)。
那我们来看看Lumenis出品的Deep FX CO2设备,深部皮肤损伤的证据明显,在某些活检标本中,微切削柱散布在填充物的注入池中,这些活检标本直接与填充物接触,并显示了填充物迁移到烧蚀微通道中的证据。在某些区域,HA被困在坍塌的微清根柱内(见下图)。
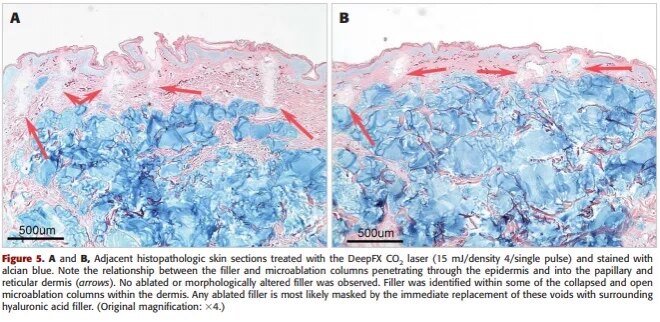
较高的能量设置会导致更深的组织损伤和增加对网状真皮的渗透,但没有显示出任何明显的形态学变化或预注射填充物的变性。填充物的烧蚀区域不明显(见下图)。
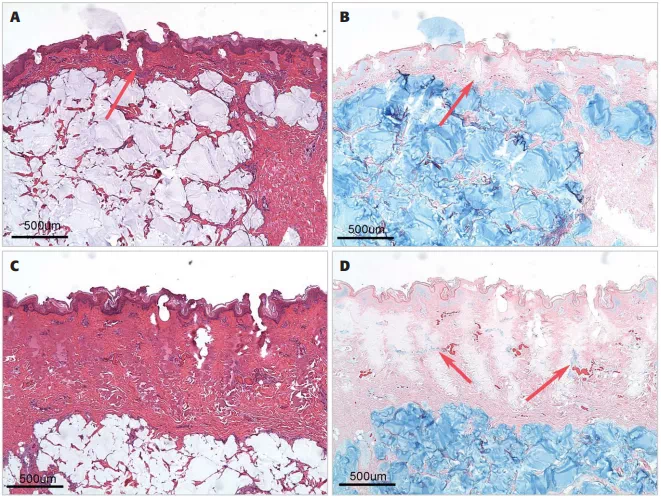
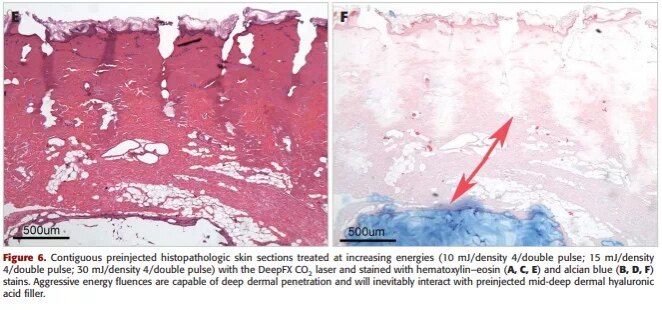
所以说,光电设备的能量越大,穿透力越强,就会侵蚀到玻尿酸注射的层次。
Sarah Hahn医生(2)将腹壁成形术皮肤分为8个区。经皮内注射透明质酸填充剂 7个区,1个区为对照。然后对7个注入区中的6个进行了以下设备的处理:1,540,1,550,1927和10,600nm分数激光,以及通过绝缘和非绝缘微针传输的分数双极射频。治疗后取组织切片进行H&E染色。

结果组织学检查显示真皮中部至深层有透明质酸填充剂的存在。用1,540-、1,550-、1927-和10,600 nm激光处理后,透明质酸填充剂的形态没有发生任何变化,尽管来自1,540和1,550 nm激光器的热变化使得与透明质酸填充剂非常接近。射频设备显示透明质酸填充剂沿微针轨道存在热损伤。
以上是点阵激光的实验结果。接下来我们来看射频类:
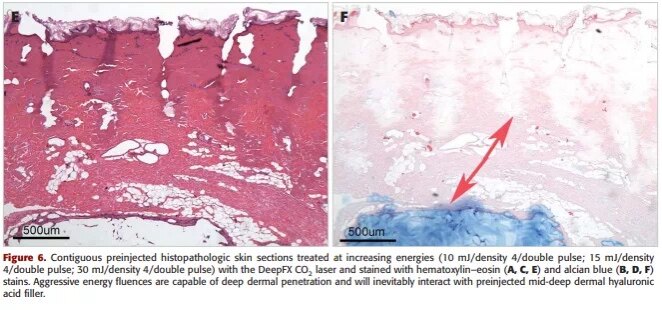
1,540 nm的Er激光,1,550 nm的Er激光和1,927 nm的thulium激光,形成了具有完整角质层的凝固胶原柱,边缘非常清楚。10,600 nm CO2分数激光造成真皮和表皮的锥形蒸发,周围的热损伤表现为退化的胶原束。测量了各个点阵激光的MTZ深度,分别为0.85、0.54、0.21和0.58 mm,颗粒层到皮肤表皮距离分别为0.78、0.44、0.10和0.54mm。
由1,927-和10,600 nm激光引起的损伤无法穿透到与填充剂直接接触的深度。
1,540 nm激光损伤的微柱支撑了填充剂的表面部分,没有显示出填充剂的任何明显的变化。从1,550 nm激光的热变化也发现非常接近填充剂 。
与点阵激光相比,微针双极射频产生了更深的真皮穿透。热损伤的最大深度为1.92毫米,带有绝缘的微针和1.38毫米的非绝缘微针。在这些深度,射频设备引起的损伤柱进入预先注入的填充剂,并有组织学证据显示填充剂沿微针轨迹受到热损伤。热损伤的证据显示,与周围组织相比,紫色退化胶原束之间的填充剂减少。在紧挨着微针轨道附近的地区似乎没有受到影响。
所以在Sarah Hahn医生的研究中,透明质酸填充剂不受点阵激光的影响。但是部分射频设备会产生更深的真皮穿透,从而导致填充剂的热损伤。因此建议在使用微针射频作用在注射过填充剂的区域时要小心。
Jurairattanaporn N等(3)做了一项前瞻性、单盲、试点研究,对14名参与者进行了研究。所有患者均获得知情同意。选择14名健康参与者入选。参与者年龄为18-65岁,排除了患有腹部皮肤疾病(如湿疹、皮肤感染、开放性伤口等)、结缔组织疾病、免疫抑制状态、凝血病、妊娠和哺乳期的参与者。有增生性瘢痕或瘢痕疙瘩病史、玻尿酸过敏史和永久性金属植入装置或起搏器的参与者。
所有参与者在四个干预部位(每个部位2 × 2 cm)(A、B、C和D)进行研究。在第一次就诊期间,在所有四个部位注射玻尿酸(Belotero Balance®,Merz)。在每个部位注射0.2毫升玻尿酸,将其分成16个小等分试样。轻轻按摩所有注射部位5分钟。注射后2小时在所有部位进行mm穿刺活检。在部位B,射频治疗(Minnie,Quanta System SpA,意大利)以单极模式进行治疗,60%的能量大约治疗30–60 秒后,直到表面皮肤温度达到42°C(通过红外温度计测量)。第14天,使用相同的设置在C部位进行射频治疗。第28天,再次使用相同的设置在D部位进行射频治疗。在最后一次就诊(第56天),由经验丰富的皮肤病理学家在所有四个部位(A、B、C和D)进行皮肤活检,并进行阿尔西安蓝(pH 2.5)染色,以评估组织中玻尿酸的残留量。
为了评估组织中残留HA的量,在载玻片上使用Alcian蓝(pH 2.5)观察突出显示的HA;HA分级评分由经验丰富的皮肤病理学家使用显微镜下拍摄的高分辨率照片进行分配。评分范围为0至4,如下:0级=无HA,1级=HA 1%–25%,2级=HA 26%–50%,3级=HA 51%–75%,4级=HA 76%–100%。评估者对每个组织切片的时间间隔不知情。
不良反应玻尿酸注射和RF治疗后的不良反应记录为二元结果(是或否),包括疼痛、瘙痒、红斑、可触及结节和炎后色素沉着(PIH)。还记录了组织学变化,包括炎症和肉芽肿。
HA丧失程度与对照组(第0天)相比,第56天HA退化的参与者百分比如表2所示。每个时间点射频治疗后的平均HA分级评分如图2所示,在玻尿酸注射后立即进行射频治疗的部位,5名参与者(35.71%)表现出HA部分丧失,与基线相比,平均HA分级评分显著降低(4.0比3.57,p ≤ 0.01)。组织学检查还显示,与对照部位相比,组织中HA显著流失(如下)。
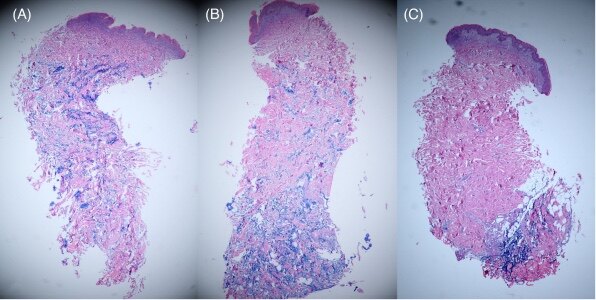
玻尿酸注射后,立即治疗区域,HA 流失明显。
在更长的时间间隔内,对于玻尿酸注射后第14天进行RF治疗的部位,一名参与者(7.14%)表现出HA流失;对于第28天进行射频治疗的部位,一名参与者(7.14%)在组织切片中显示HA流失。在第14天和第28天进行射频治疗的部位,平均HA分级评分在基线和第56天之间没有显著差异(4.0 vs 3.93,p=0.56)。在对照部位,在玻尿酸注射后未进行射频治疗,没有参与者表现出HA流失,平均HA评分为4(如下)。
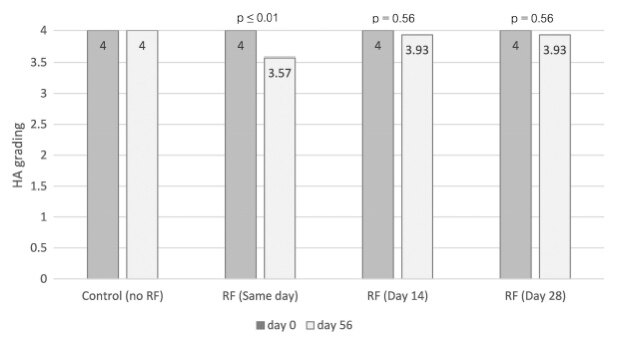
所有患者均耐受。治疗后未观察到可触及的结节、红斑或妊高征。两名参与者(14.28%)在注射HA后所有部位出现瘙痒,2小时内完全消退。未观察到严重不良反应。组织学检查显示,注射后第56天,任何活检标本均无炎症或肉芽肿。
为了延长玻尿酸的寿命,制造商开发了交联技术,将HA聚合物链相互结合,形成强大的聚合物网络,并将粘性溶液转化为硬凝胶颗粒。然而,一些因素可以加速HA的降解过程,如透明质酸酶、酸碱、超声波、热、自由基和紫外线。射频治疗目前正越来越流行于美容目的。它在组织中产生热量,以紧致皮肤,减少脂肪,并刺激新的胶原蛋白形成。目前可以使用三种类型的设备输送能量:双极、单极和单极设备。通常,与其他类型的射频设备相比,单极设备具有最深的穿透力。RF治疗的目标温度可以变化。理论上,当组织温度达到约47°C时,开始刺激成纤维细胞和新胶原蛋白生成。在60°C时,热量会导致胶原蛋白收缩。当皮下组织温度升至70°C时,脂肪细胞溶解开始。如果温度升高到85°C以上,可能会导致永久性组织和神经损伤。热可以加速HA降解的前提导致了通常的做法,即大多数医生避免使用在玻尿酸注射后立刻使用产生热量的设备或治疗。射频治疗可在组织中产生高达65°C的热量,以达到治疗的临床终点。通常,建议单独进行射频治疗和玻尿酸注射。然而,每种治疗方式之间的适当时间间隔仍不确定。此外,先前关于RF治疗对皮内玻尿酸的热影响的研究仍然模棱两可。
在本研究中,使用非烧蚀单极射频装置,其设置导致表面温度为42°C。根据制造商的信息,热量可以渗透到2.5厘米的深度。然而,皮下温度无法准确测量。研究发现,根据组织学切片,有5名参与者(35.71%)的HA水平明显下降,注射HA后立即进行RF治疗时,平均HA评分显著降低。注射后第14天和第28天进行射频治疗时,每组只有一名参与者(7.14%)表现出HA丧失,平均HA评分与基线相比没有显著降低。根据我们的结果,我们可以推断,早期射频治疗可能会导致微观玻尿酸损失。玻尿酸注射和RF治疗之间的更长时间可以减少微观HA降解的机会。
总之,建议在注射玻尿酸之前进行射频治疗。然而,如果首先注射玻尿酸,则不应在玻尿酸注射后14天内进行射频治疗。
Vachiramon V等(4)一项单中心、前瞻性的试点研究,招募了受试者14名18至65岁的健康受试者,在基线(第0天),受试者被告知研究方案并签署知情同意书,然后在4个方形实验点(测量2 × 2cm)(0.25 ml/位点)。使用30号、½英寸长的锐针通过漂白技术注射HA(这是Belotero的特定注射技术)。采用多次穿刺技术将HA注射于皮内。针的方向几乎平行于皮肤(即针的穿透角度不超过12度),并向上倾斜。针的轮廓被可视化,以确保材料的表面、皮内放置。在表面下方继续多次穿刺,直到整个区域注射完毕。注射区域的注射后成型是为了确保更均匀的皮肤沉积。在每次随访期间,用单独的绘图塑料模板标记每个位置,以提供相同的位置。所有14名患者都进行了3mm穿刺活检以进行组织病理学研究。活检在所有部位进行注射30 分钟后进行。部位A作为对照,而部位B、C、D用MFU(Ultherapy®,MerzAesthetics,Raleigh,NC)处理,每个部位10条,使用1.5 mm深度换能器和0.2J能量。部位B用MFU处理,(同一天)注射后60分钟进行,而C和D部位分别在注射后第14天和第28天用MFU处理。在第56天,所有部位均已通过塑料模板标测确定位置,并触诊皮肤硬结,然后重新活检以评估组织病理学特征。将所有代表性样品进行福尔马林固定、切片,并对苏木精-伊红和pH2.5的阿尔西安蓝进行染色,以确定保留的HA的数量。在研究结束之前,建议患者在实验部位避免剧烈按摩或使用其他局部治疗、热疗和其他基于能量的设备。研究流程图如下图所示:
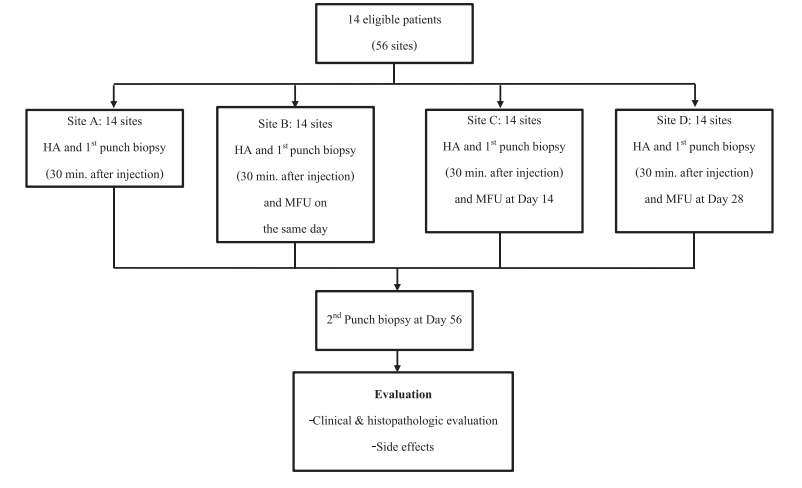
评估主要结果是保留HA的数量。皮肤病理学家通过光学显微镜(×100原始放大倍数)使用视觉HA分级评分盲评透明质酸的量。Alcian blue pH 2.5染色的蓝色从0到4分级,等级越高表示染色面积越大(等级0:无蓝色,等级1:1%–25%,等级2:26%–50%,等级3:51%–75%,等级4:76%–100%)。记录临床观察到的可能的不良反应,包括疼痛、瘙痒、红斑、瘀伤、炎性结节和炎后色素沉着。组织学观察炎症反应和肉芽肿。统计分析STATA/SE版本14.2(STATA Corp.,College Station,TX)用于进行统计分析。所有描述性统计数据使用分类变量的百分比。数值数据报告为平均值(SD)。使用估计量和线性混合效应模型的线性组合来确定结果的统计相关性。具有统计学意义的水平被视为p<0.05 。
所有部位的基线HA分级均无显著差异(A、B、C、D部位为3.7级)。在部位A(对照部位),第56天受试者(7.7%)的HA染色减少,另外12名受试者的HA分级得分相同。在第0天和第56天之间,对照部位的HA分级无统计学显著差异(3.7 vs 3.6,p=0.720)。关于MFU治疗部位,当在HA注射的同一天(部位B)和HA注射后第14天(部位C)进行MFU时,7名受试者(53.9%)和6名受试人员(46.2%)在第56天HA分级降低。基线和第56天的平均HA分级分别为B部位3.7 vs 2.8(p<0.001)和C部位3.7 vs 3.0(p=0.001)(下图)。
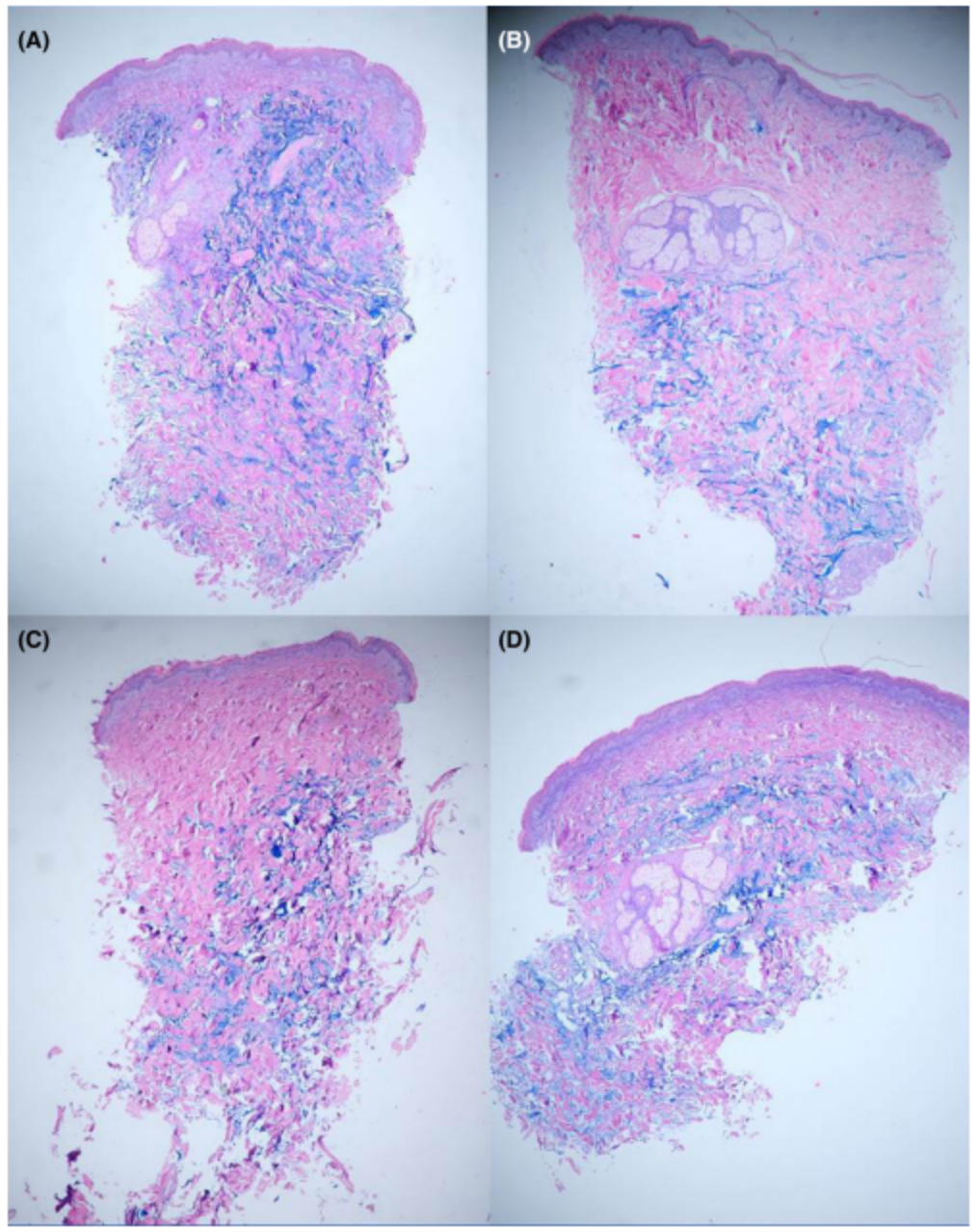
在D部位(注射HA后第28天进行MFU),有3名受试者(23.1%)在第56天HA分级降低。然而,基线和第56天的平均HA分级之间没有统计学显著差异(3.7 vs 3.3,p=0.073)(图2)。与位点B相比,位点D显示出显著更高的平均HA分级(3.3比2.8,p=0.012)。
关于组织学外观,在第56天,对照组和所有MFU治疗部位均无炎症反应或肉芽肿。所有患者都能耐受。MFU和HA注射的平均疼痛评分分别为3.6和2.9。在所有随访期间,临床上未观察到红斑、瘀伤或结节。三名患者因皮肤活检而出现增生性瘢痕,但在6个月的随访中自行好转。
MFU可以发射高频超声波,根据所用换能器的深度,在乳头状真皮和网状真皮或浅表肌筋膜系统中产生65–70°C的精确热凝固点。当HA被皮内注射时,理论上,加热可能导致填充剂性质的改变。然而,关于HA注射的MFU的数据仍然有限。根据Casabona等人的单例报告,HA注射后立即进行MFU时,临床上未观察到可见或可触及的结节。组织学上,在注射玻尿酸区域立即进行MFU治疗时,填充物外观无炎症反应、肉芽肿和组织学变化。此外,MFU促进术后新胶原和弹性纤维的增强和质量。根据本研究初步结果,大约一半的受试者在14天内进行MFU时出现了HA的流失,然而,如果MFU在注射后第28天进行,与对照组相比,HA流失没有显著差异。这可以解释为温度超过50°C会导致更高的HA降解。此外,超声功率的传播可通过高速振动和剪切力导致HA降解。根据Molliard等人的研究,注射后HA凝胶在体内的分布和整合到皮肤中需要几小时到注射后数周。同样,Tran等人的一项组织学研究也发现,8小时后,粘性聚致密基质填充剂(如Belotero Balance®)在皮肤中的分布与内源性HA非常相似。因此,我们假设注射后更长的MFU间隔时间可能允许填充物分布和组织整合,这有助于保护填充物免受MFU的热凝固。总之,HA注射后的MFU治疗似乎是安全的。HA流失的受试者百分比似乎随着HA注射和MFU治疗之间的时间间隔的延长而降低。为了避免HA流失,我们建议在注射HA后至少1个月进行MFU治疗,如果两种治疗方法是作用于组织的相同层次。
Hong JK等用“高强度聚焦超声+量子分子共振技术”治疗填充剂引发的肉芽肿。
这是一位52岁的女性,有4个月的皮肤色结节病史,双颊肿胀(如图)。1年前,她在双颊和鼻唇沟上注射聚乳酸填充剂,8个月前在同一部位接受透明质酸填充剂注射。患者报告说,结节形成于4个月前,她已经接受了透明质酸酶局部注射,也接受了全身抗生素治疗。尽管经过治疗,症状仍在继续。
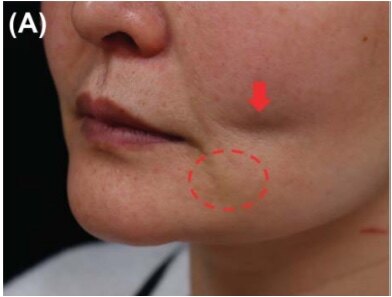
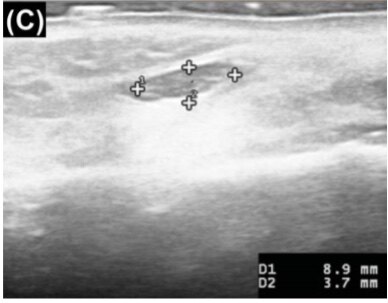
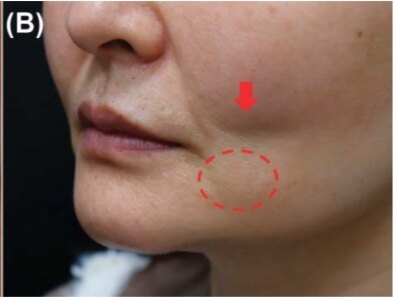
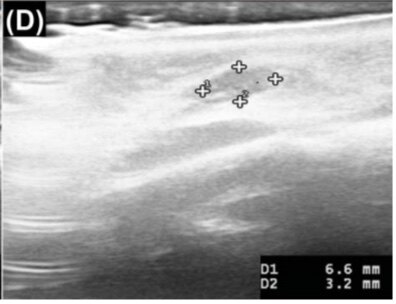
HIFU求美者的治疗面积为5.0×5.0cm。在每个脸颊上。应用局部麻醉剂后,我们使用两个不同的传感器(L4-4.5:4 MHz,4.5 mm探头,MF6:2 MHz,6.0 mm探头),治疗线包括L4-4.5(0.9J/次)和MF6(1.5J/次)共30次,每个病灶共分布72 J。(可选4.5mm探头)一周一次连续8次,QMR促进修复。
HIFU是利用高能超声波来提高病灶区的温度,导致组织破坏和凝血坏死。它还被用于实体肿瘤消融,包括前列腺癌和子宫肌瘤。通过选择合适的HIFU频率,可以方便地控制治疗区的焦深,这是HIFU系统的优点。在这种情况下,我们使用2兆赫和4兆赫换能器治疗浅层和小型填充肉芽肿。
与射频相比,HIFU在深网状真皮组织中具有高度聚焦,并表现出最高的新生期和新弹性生成。这表明HIFU对深部组织和病灶有一定的影响,而射频则对弥漫性区域有影响,在深层网状真皮中作用不如HIFU。因此,医生们推测与射频相比,HIFU能在不损伤表皮的情况下,通过聚焦胶原变性和新生胶原沉积,在不损伤表皮的情况下,对填充性肉芽肿患者产生类似但更有利的作用。
为了使治疗效果最大化,医生们还使用了一个qmr技术装置,它产生复杂的共振波,包括超过16个频率,从4兆赫到64兆赫,以产生电场治疗区。已经证明,QMR器件的辐射引起分子共振能,影响分子键,导致细胞在分子水平上再生。据报道,QMR装置减少了炎症细胞的数量,上调了血管内皮生长因子的表达,导致伤口愈合。在此基础上,医生们推测,通过胶原变性导致新生胶原生成,该装置可以改善炎症,加速HIFU所致坏死区的创面愈合过程。最后,QMR技术也显示出抗水肿作用,这对填充性肉芽肿患者尤其有益,因为填充剂肉芽肿常伴有注射部位的全身水肿。在这种情况下,病人明显地减少了面部肿胀。
思考:注射填充剂后的光电治疗分三种情况,一是为了更好的美容效果;二是为了纠正过度填充;三是为了纠正填充导致的肉芽肿或结节。光电是否影响填充剂,与光电穿透深度,能量等有关。为了获得更好的美容效果,在填充剂注射后导致的肿胀消退后即可做,热玛吉可以在填充后2周,超声刀最好是填充后1月。对于想纠正过度填充的,则是越早越好,填充后即刻治疗,有助于填充剂的代谢。纠正填充导致的肉芽肿和结节,聚焦超声有定位较准的优势。高能量长脉宽1064nm Nd:YAG激光对肉芽肿和结节是否有效,值得探究。
参考文献
- Farkas JP, Richardson JA, Brown S, Hoopman JE, Kenkel JM. Effects of common laser treatments on hyaluronic acid fillers in a porcine model. Aesthet. surg. j.. 2008;28(5):503-11. doi:10.1016/j.asj.2008.07.010, 10.1016/j.asj.2008.07.010
- Hsu, Sarah, Chung, Hye, Jin MD, MMS, Weiss, Robert. Histologic Effects of Fractional Laser and Radiofrequency Devices on Hyaluronic Acid Filler. Dermatol Surg. 2019;45(4):552-556.
- Jurairattanaporn N, Amornpetkul W, Rutnin S, Vachiramon V. The effect of combined hyaluronic acid filler injection and radiofrequency treatment: A clinic histological analysis. J Cosmet Dermatol. 2022 Nov 14. doi: 10.1111/jocd.15509. Epub ahead of print. PMID: 36374532.
- Vachiramon V, Rutnin S, Patcharapojanart C, Chittasirinuvat N. The effect of combined of hyaluronic acid dermal filler and microfocused ultrasound treatment: A clinicopathological study. J Cosmet Dermatol. 2022 Nov 14. doi: 10.1111/jocd.15498. Epub ahead of print. PMID: 36374232.
- Hong JK, Sun B, Shin SH, Kim BJ. Late-Onset Filler-Induced Granuloma After Polycaprolactone-Based Filler Treated With High-Intensity Focused Ultrasound and Quantum Molecular Resonance Technology. Dermatol Surg. 2022 Jun 1;48(6):693-694. doi: 10.1097/DSS.0000000000003424. Epub 2022 Mar 31.
本文是刘明章版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论