 三甲
三甲
肝癌“消融性”外照射放疗最新国际专家共识:BED10≥80 Gy是放疗剂量的最低要求
摘要
2022年版巴塞罗那肝癌指南没有在任何一种临床场景中包括肝癌外照射放疗,作为对这一荒唐行径的抗议,也是为了对肝癌患者中的消融性外照射放疗 EBRT 进行个体患者水平的荟萃分析,北美放疗界召集了一个国际专家小组,对肝细胞性肝癌的消融性外照射放疗(EBRT) 的参数达成了共识。
根据这一国际专家共识,肝癌的消融性外照射放疗(EBRT )被定义为:BED10 ≥80 Gy,使用多相影像进行靶区勾画,每日进行图像引导照射。允许放疗期间有时间中断,但总治疗疗程不超过6周。用质子治疗时的等效剂量应使用RBE=1.1的转换因子,碳离子没有单一的转换因子。
该共识发布于2024年1月份召开的ASCO 2024年胃肠道癌症研讨会上,文章同步发表于《Practical Radiation Oncology》杂志。
本文中HCC或肝癌均指肝细胞性肝癌。如无特殊说明,本文放疗一律指外照射放疗(EBRT)。
本文四部分内容如下:
- 介绍形成该共识的方法和内容
- 该共识对肝癌外照射放疗临床实施意味着什么?
- 增加肝癌的放疗剂量不会等比例的导致毒性增加
- 该共识的由来:肝癌外照射放疗面临的其他学科的竞争
1、形成该共识的方法和内容
1、为什么会在现在制定这样一个共识?
外照射放疗EBRT治疗肝癌业已百年,有很多前瞻性和回顾性研究证实其作为根治性治疗和姑息性治疗的安全性和有效性,为什么会在这个时间节点制定这一共识呢?因为在2022年巴萨罗纳肝癌指南中,任何临床场景都没有包括外照射放疗,理由是“外照射放疗临床证据不足“,但是”仅仅根据最近的一项回顾性研究,动脉放射栓塞(TARE,即钇90这类耗材)就已被纳入选择性BCLC 0-A 肝癌患者的一种选择?”。
欧美放疗医生对此提出严正抗议,巴萨罗纳委员会为了挽尊,同意和放疗医生一起,综合现有数据,通过对个体患者数据的荟萃分析为这些指南提供信息。由于即将进行的荟萃分析的结果在很大程度上取决于消融性EBRT的明确定义的技术和剂量参数。此外,美国肝病研究协会AASLD指南认可EBRT作为BCLC-A 肝癌消融性疗法的替代疗法,但没有定义消融性外照射放疗EBRT或以其他方式提供有关EBRT临床实践操作的具体信息(例如:处方剂量和技术细节)。因此,拟完成的荟萃分析的结果可用于将来更新美国肝病研究协会AASLD和欧洲肝脏研究协会EASL的治疗指南。
本文末对巴塞罗那委员会的荒唐做法和放疗医生的评论文章有详细说明,感兴趣的读者可以阅读。
1.1 形成该专家共识的方法和材料
指导委员会
一个由 7 名在治疗肝癌方面具有专业知识的放疗医生组成的委员会召开会议,以制定一份定义消融性放疗的关键标准 (KC) 清单。该委员会被指示确定消融性放疗的技术参数,而不是如何选择正确的患者群体进行治疗。
指导委员会由 10 人组成:7名放疗医生、2 名专门研究 肝癌的肝病学家和1名生物统计学家。初步关键标准KC代表了系统文献综述中确定的研究之间的共同差异领域,提供给指导委员会。
mDelphi委员会
加入 mDelphi 委员会的邀请被发送给由 40 名具有肝癌放疗专业知识的放疗医生组成的国际队列,该委员会的任务是为每个关键标准KC 选择答案。mDelphi委员会的候选人由指导委员会的每位成员提供,同时在已发表的系统文献综述较多的作者中选择其他候选人。与所有被提名的候选人联系,邀请他们加入,指导委员会的放疗医生也参加了mDelphi 委员会。
定义 mDelphi 调查的关键标准
经过两轮起草和独立匿名投票,确定了7个定义肝癌消融性放疗的关键标准(KC1-7),除了KC1(肝癌的α/β比)未达成共识外,其余6项均达成共识:
- KC1:肝癌的α/β比:未达成共识。
- KC2:肝癌消融性放疗最低的BED10:≥80Gy。
- KC3:质子使用相对生物学效应(RBE):1.1。
- KC4:碳离子使用RBE:由于碳离子的RBE因组织而异,因此不适合选择单个RBE来比较碳离子和光子研究之间的剂量和分割方案。
- KC5:放疗最长的总治疗持续时间:不超过6周。
- KC6:使用每日图像引导:同意。
- KC7:对靶区勾画使用多相成像(CT ± MRI):同意。
讨论:
迄今为止,在肝癌的治疗中,还没有被广泛接受的“消融性”外照射放疗EBRT的定义。消融性外照射放疗EBRT通常等同于立体定向放疗(SBRT),有时也称为立体定向消融放疗(SABR)。但术语“消融”意味着可以提供完全根除肿瘤的生物学效应,而SBRT和SABR指的是一种治疗技术。因此,使用这一技术本身并不意味着一定能达到消融这一治疗结果。此外,SBRT和SABR在全球范围内都有着不同的定义。在美国,保险支付方根据治疗次数限制该定义。即,一疗程照射5次或更少次数可被视为SBRT,6次就不被视为是SBRT。此外,SBRT通常仅用于基于光子的放疗,而不用于质子或碳离子。
在关键标准KC1-4 评估消融性外照射放疗EBRT 的生物学方面,回答中差异最大的问题是关于肝癌的α/β 比。使用这种mDelphi 方法无法就此问题达成共识。肝癌α/β比的文献很少,使用细胞培养系的实验揭示了一系列潜在值,而体内人体数据非常有限。鉴于肝癌α/β比的实际值存在很大的不确定性,委员会决定在BCLC荟萃分析中使用2到10的取值范围。
委员会选择将“剂量”定义为BED/生物等效剂量,因为这是比较不同剂量/分割方案之间生物剂量的最佳方法,这允许在不同研究中来统一放疗的等效生物学效应。在此定义中不要求剂量学参数(例如,最小计划目标体积PTV覆盖率、最低或平均目标剂量),因为放疗计划中剂量的处方和评估方式存在差异。预计不同研究的剂量学参数的差异不会对结果产生重大影响,但值得进一步研究。
BED是一个数学公式,可以近似地给出给定辐射剂量的生物有效性。BED取决于α/β、总的物理辐射剂量和基于以下公式的单次照射剂量:
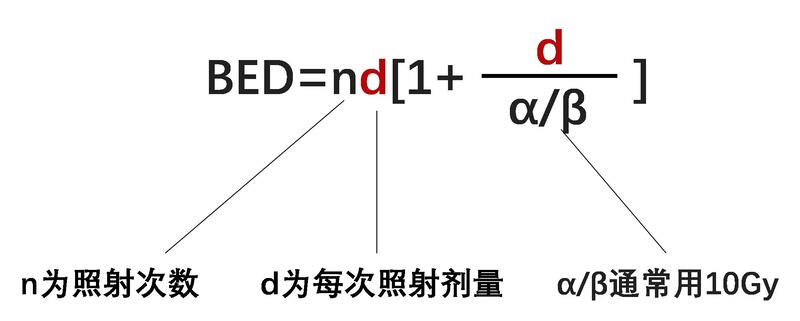
较高的BED值与更好的肿瘤控制有关。BED≥100 Gy 已被用作定义其他癌症组织类型消融的阈值。然而,临床数据表明,对比其他肿瘤类型,肝细胞性肝癌可能对辐射更为敏感。
值得注意的是,BED与肿瘤局控之间存在连续关系,没有明确的阈值剂量。尽管严格的阈值有些武断,但消融性外照射放疗EBRT必须定义最低剂量参数。最终,在第二轮mDelphi中,35名参与者中有26名(74%)同意80Gy(例如SBRT~43Gy/5次)是比较合适的肝癌消融性放疗的最低BED阈值。
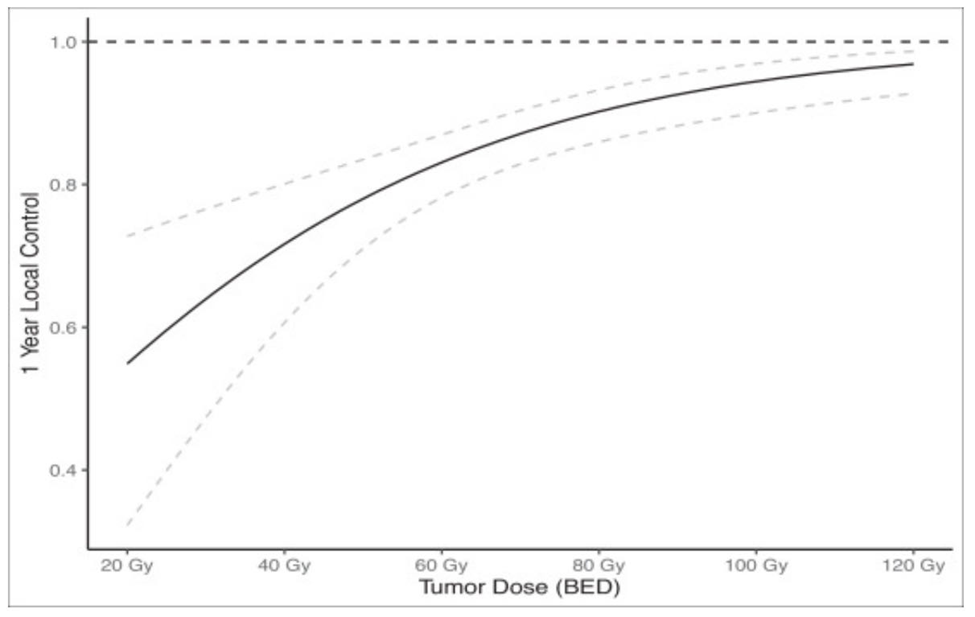
图 1.立体定向放疗SBRT后 1 年局控率和总剂量( BED Gy,α/β = 10Gy)的函数。
Chang Wang和Matthew Schipper分析了来自密歇根大学和玛格丽特公主癌症中心的先前参与临床试验的212名患者。该曲线代表剂量和1年局控的关系,当然了,时间维度越长,高BED对局控的正面影响越显著。虚线表示关系的 95% 置信区间。缩写:BED=生物有效剂量。
根据投票结果,委员会接受了质子的 RBE 为 1.1,并计划在未来的荟萃分析中使用该值;同意为碳离子选择单一 RBE 是不合适的。由于无法选择碳离子的 RBE,因此 BCLC 荟萃分析将检查单独使用碳离子的每篇文章。文章审稿人将审查每篇出版物的方法,以确定使用哪种生物等效模型来选择剂量,并考虑一系列RBE值,以确定质子重离子照射的BED是否为>80 GyE。
关键参数5-7 评估了消融性 EBRT 的技术方面 (KC5-7)
KC5的目的是为可称为消融性放疗的疗程总持续时间提供定义。该问题的提出是因为相对于传统的每日照射一次或隔天照射一次的时间表,肝癌的一些分割方案是在更长的时间内进行的,并且关于延长治疗间隔如何影响肿瘤控制概率的数据有限,尽管现有数据并未表明肿瘤控制会随着治疗时间的延长而下降。
KC6达成共识,即应使用每日成像进行目标配准,包括适当的替代物(例如,植入的标记点)。
KC7指出,靶区轮廓的勾画应依赖于多相增强对比成像。在多期成像中,病变最好在动脉、门静脉或延迟期上看到,并且被认为最准确地定义肿瘤范围的一个或多个时相被用作轮廓勾画的主要图像集。需要注意的是,在一些情况下,由于组织密度的固有差异,非造影成像也可以提供病变的适当解剖边界。尽管在一些独特的病例中,肿瘤可以与肝脏背景区分开来,例如在一些非酒精性脂肪肝患者中,但这并不能消除对多相成像的需要,以确保精准的靶区勾画。需要注意的是,如果不使用多相成像,血管浸润可能会被漏诊,尤其是在无法进行MRI检查的情况下。
根据这一国际专家共识,肝癌的消融性外照射放疗(EBRT )被定义为:BED10 ≥80 Gy,使用多相影像进行靶区勾画,每日进行图像引导照射。允许放疗期间有时间中断,但总治疗疗程不超过6周。用质子治疗时的等效剂量应使用RBE=1.1的转换因子,碳离子没有单一的转换因子。
2、该共识对肝癌放疗的临床实施(尤其剂量分割)意味着什么?
肝癌消融性外照射放疗EBRT的共识定义“BED10 ≥80 Gy,具有每日进行图像引导和使用多相影像进行靶区勾画。允许放疗期间有时间间隔,但总治疗时间应不超过6周……“满打满算照满6周,每工作日一次,最多30次照射。意味着需要在≤30次的照射中给予BED10≥80Gy的剂量。
根据对肝癌消融性放疗这一最低剂量要求,只有高剂量的大分割放疗和SBRT才有可能做到。因为常规分割(单次照射1.8Gy-2.2Gy)能给予的最高剂量(30次*2.2Gy/次=66Gy,其BED10=80.5Gy)也就刚刚能达到这一最低要求。

根据上述BED的计算公式,不超过6周照射BED10≥80Gy,意味着如下公式:

解这个方程式,很容易得到不同照射次数下,达到BED10 80Gy的最低剂量要求:
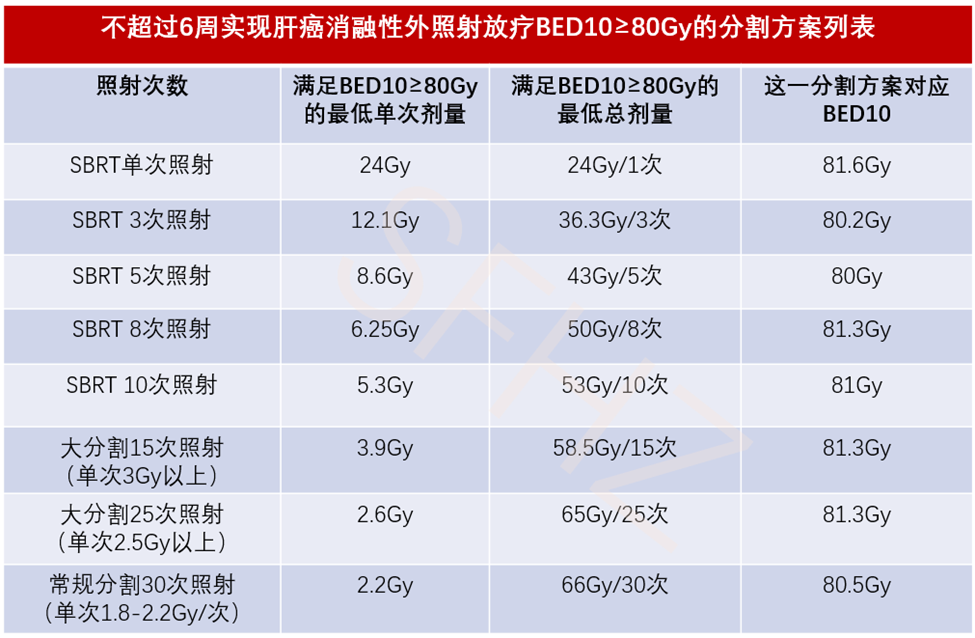
从理论上来讲,放疗技术上做到80Gy以上并非难事,尤其是SBRT技术。但是在真实世界里,原发性肝癌放疗都在二线、三线甚至四线,放疗前绝大多数患者都是在多个其他科室接受多线治疗后复发/进展的患者,大多数患者都伴有肝硬化、(手术切除后)正常肝体积小、肿瘤大等特点,放疗医生治疗的早期小肝癌非常少见(小肝癌SBRT比较容易实施高BED照射)。这种情况下,如何权衡肿瘤剂量和关键脏器OAR的剂量,是摆在放疗医生面前的一道难题。
而对于大肝癌来讲(例如直径大于15cm),可能上述技术都无法都实现消融性剂量的放疗,LATTICE/SBRT PATHY等技术,也许是潜在的解决方案。
3、该共识引申讨论:肝癌消融性放疗的剂量增加会导致毒性增加吗?
肝癌的消融性外照射放疗EBRT 被定义为 BED10 ≥80 Gy,这意味着低于这个阈值将不被认为是根治性/消融性放疗。那么,增加肝癌消融性剂量会导致毒性增加吗,尤其是放疗医生一直担忧的放射性肝炎等肝毒性?
根据2021年Shanker等人发表的肝癌立体定向消融放疗SABR的系统回顾和荟萃分析<Stereotactic ablative radiotherapy for hepatocellular carcinoma: A systematic review and meta-analysis of local control, survival and toxicity outcomes>,增加肝癌消融性剂量,对患者局控率和生存带来的正面影响,远远大于毒性的微小增幅。
根据这一荟萃分析:在EQD2 40–83.3Gy的范围内(相当于SBRT处方剂量30Gy/5次–50Gy/5次区间),放疗剂量每增加10Gy,1年局控率/2年局控率/3年局控率分别提升2.4%/1.4%/3.6%,1年OS%/2年OS%/3年OS%分别提升0.7%/1.4%/3.9%,但3级或以上的肝毒性/胃肠道毒性仅增加0.3%。
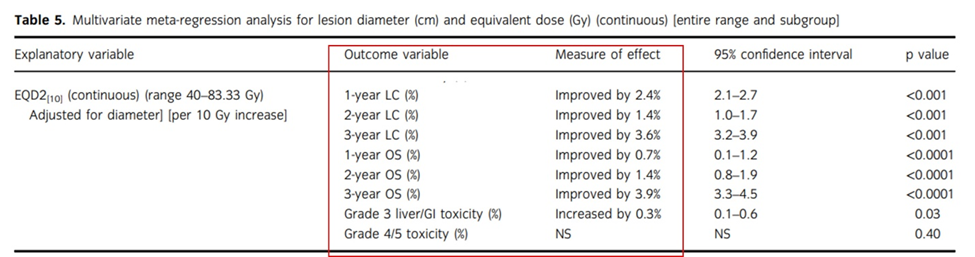
当SBRT的放疗剂量从30Gy/5次(EQD2剂量为40Gy)增加到50Gy/5次(EQD2剂量为83.3Gy)时,EQD2剂量增加了43.3Gy,即4.33个10Gy的增加。根据文中EQD2每增加10Gy剂量对局控、OS%和毒性增加的影响,进行换算,当SBRT的放疗剂量从30Gy/5次(EQD2剂量为40Gy)增加到50Gy/5次时:
- 1年局控率和3年局控率分别增加了10.4%和15.6%
- 1年OS%和3年OS%分别增加3.0%和16.9%
- 3级毒性的发生率仅仅增加了1.4%
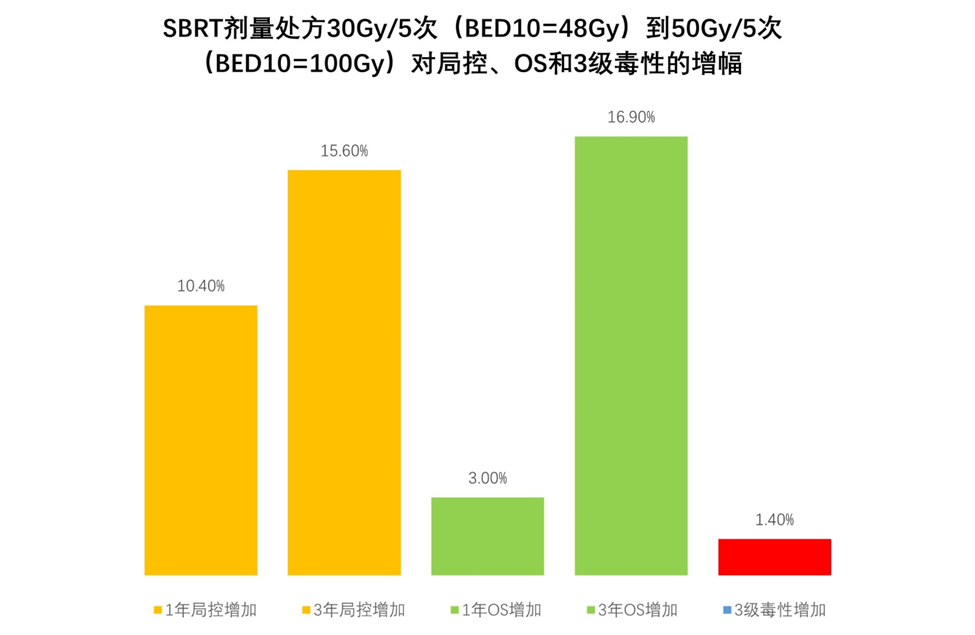
剂量增加对局控和OS的提升是惊人的(15.6%和16.9%), 而3级毒性仅增加了1.4%,这还不值得努力去增加剂量吗? 增加肝癌放疗剂量不会等比例增加、更加不会指数级别的增加毒性,否则谈论各种放疗技术就毫无意义了。安全的增加剂量依赖放疗医生使用合适的影像手段、呼吸运动管理、精准的靶区勾画、合理的剂量处方,以及和物理师的良好合作。
从根本上来看,无论是为了提升患者获益还是面对其他治疗方式的竞争,安全的提升放疗剂量是放疗发展的永恒主题和立足根本。不独肝癌放疗如此,其他癌症的放疗也是如此。近期发表的两项研究分别通过SBRT boost或SBRT联合IMRT来治疗局部晚期非小细胞肺癌前瞻性II期研究的阳性结果也证实了这一点:其目的都是通过各种技术手段安全地将局部晚期肺癌的放疗剂量增加到BED10≥100Gy这一阈值以上。
4、该共识的由来:背后的故事和肝癌放疗的竞争
肝细胞性肝癌(HCC)是全球第六大常见癌症,也是癌症死亡的第三大原因。有许多可用的局部/区域治疗方法,包括外照射放疗(EBRT)。巴塞罗那诊所肝癌(BCLC)分期系统是世界上用于选择患者首选治疗方案的最常用分期系统,并得到欧洲肝脏研究协会(EASL)和美国肝病研究协会(AASLD)的认可。
但是在最近的指南更新中(2021年11月份发布),2022版BCLC治疗指南没有提供任何有关使用外照射放疗EBRT的建议,理由是外照射放疗缺乏足够的前瞻性数据。放疗医生对于这个指南更新当然是大吃一惊的,因为外照射放疗用于肝癌的治疗已有近百年的历史,有很多回顾性和前瞻性的临床数据。美国梅奥诊所的Christopher Leigh Hallemeier医生,华盛顿大学附属医院的Smith Apisarnthanarax医生,以及加拿大玛格丽特公主癌症中心的Laura Ann Dawson医生在2022年1月联合就该指南更新发表文章评论:“巴塞罗那2022年更新:重要的进展,但是缺失了外照射放疗”。(“BCLC 2022 update: Important advances, but missing external beam radiotherapy”)

在这篇评论中,三位放疗医生指出,仅仅只是根据最近的一项回顾性研究,动脉放射栓塞(TARE)就已被纳入选择性BCLC 0-A HCC患者的一种选择,然而,值得注意的是,2022年更新的指南竟然没有将外照射放疗(EBRT)作为HCC指南中的一种治疗选择。除了许多回顾性研究外,来自多个大洲的多项前瞻性研究已经证明了外照射放疗EBRT的安全性和有效性,包括立体定向放疗SBRT和质子放疗,适用于所有BCLC分期。自2018年版BCLC指南更新以来,放疗学界已经发表了一些重要的外照射放疗的随机对照试验。例如,对于复发性BCLC A-B 肝癌患者,将质子放疗PBT与射频消融术(RFA)进行比较的III期非劣效性随机对照试验表明,质子放疗与较低的严重毒性和肝脏失代偿风险以及相似的局部无进展生存率和生存率(4年生存率约为75%)相关。对于有大血管浸润的肝癌患者,对比单独使用索拉非尼,经动脉化疗栓塞TACE+外照射放疗EBRT的III期随机对照试验显示出更高的生存率。对于可接受手术切除的大血管侵犯患者,III期随机对照试验显示,与单独切除相比,术前接受外照射放疗EBRT的患者生存率更高。这些2018年以来发表的III期随机对照试验的结果证实了此前非随机研究的结果,也证实了外照射放疗的安全性和有效性。
最后这三位医生在评论文章中指出,他们认为有足够的证据支持将外照射放疗(EBRT)纳入BCLC指南,特别是当肝癌患者“一线治疗方案”不可行或不合适时,或者在一线治疗后出现进展。对于BCLC指南的未来更新,他们建议根据ASTRO指南的建议纳入外照射放疗EBRT,具体建议如下:
- 对于BCLC 0-A 肝癌患者,应将外照射放疗EBRT和RFA消融或TACE栓塞一样被视为一种替代性非手术治疗,作为根治性治疗或移植前桥接治疗。
- 对于BCLC B-C肝癌患者,外照射放疗EBRT是一种治疗选择,结合或不结合TACE栓塞或全身治疗。
- 对于BCLC D 肝癌患者,外照射放疗EBRT应被视为肿瘤相关疼痛等的姑息治疗。
在上述荒唐背景下,BCLC和肝癌放疗领域的国际专家发起拟合力进行系统的文献综述,并从合格研究中获得个体患者水平的数据以进行荟萃分析,以更好地了解外照射放疗EBRT在肝癌治疗中的作用。对于这种类型的综述,首先需要达成共识来定义构成消融性EBRT的参数,消融性的治疗目的是在目标区域完全根除肿瘤。
在确定消融性放疗时,需要考虑EBRT的治疗意图、技术和质量。例如,外照射放疗的目的可能是根治性的,或者外照射放疗EBRT可以用作肝移植前的桥接治疗;放疗模式可以包括光子、质子或重离子;可以使用具有不同剂量学目标、靶区勾画和运动管理的各种剂量分割方案。为了获得评估EBRT在BCLC个体数据荟萃分析中有意义的信息,需要首先定义肝癌治疗环境中使用的放疗参数的最低技术要求。
为了制定消融性EBRT的定义,专家组遵循了用于生成EASL临床实践指南的做法。具体来说,专家组召集了具有肝癌治疗专业知识的国际委员会,并使用改进的Delphi(mDelphi)方法就EBRT被认为是消融所需的一组最低参数达成共识。这些信息对于BCLC个体数据荟萃分析至关重要,但也通用于所有考虑EBRT治疗HCC的场景。
这个关于肝癌消融性放疗的定义共识,是为了解决肝癌临床放疗的医疗竞争压力。对于肝癌放疗来说,这个共识也算开创风气之先,能起到正本清源的作用。无论是小同行(放疗医生)还是大同行(其他肿瘤医生),在沟通肝癌的根治性放疗/消融性放疗的时候,至少有了一个最低的标准,而不是各说各话,将肝癌姑息性放疗的结果/技术/剂量和根治性/消融性放疗混淆在一起。
参考文献:
1. MReig, A Forner, J Rimola, et al. BCLC strategy for prognosis prediction and treatment recommendation: The 2022 update. J Hepatol, 76 (2022), pp. 681-693
2. Hallemeier CL, Apisarnthanarax S, Dawson LA. BCLC 2022 update: Important advances, but missing external beam radiotherapy. J Hepatol. 2022 76(5):1237-1239
3. Yanagihara TK, et al. Defining Minimum Treatment Parameters of Ablative Radiation Therapy in Patients With Hepatocellular Carcinoma: An Expert Consensus. Pract Radiat Oncol. 2023 Nov 14:S1879-8500(23)00276-X
4.Shanker, M.D, et al. Stereotactic ablative radiotherapy for hepatocellular carcinoma: A systematic review and meta-analysis of local control, survival and toxicity outcomes. J. Med. Imaging Radiat. Oncol. 2021, 65, 956–968
本文为转载文章,如有侵权请联系作者删除。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论