 三甲
三甲
2023 ASCO-GI 胃癌相关研究
今年的ASCO GI大会于当地时间2023年1月19日至21日在旧金山召开。分享几篇关于胃癌/食管胃结合部癌药物治疗的摘要。
新辅助治疗
- Rapid Abstract 295:NEO-AEGIS研究最终结果初步分析
Neo-Aegis是比较同步放化疗(CROSS方案:卡铂/紫杉醇+41.4Gy放疗)与围术期MAGIC/ FLOT化疗治疗食管胃结合部腺癌的III期临床研究。
研究设计
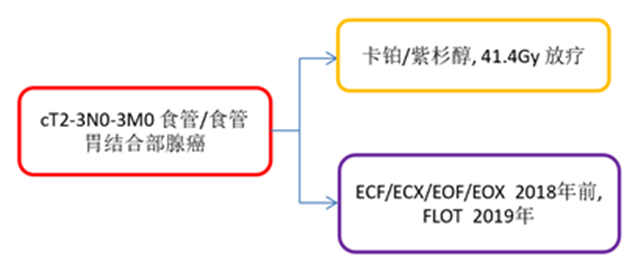
主要研究终点:总生存
结果:377例cT2-3N0-3M0 食管胃结合部腺癌患者随机分组为围手术期化疗组(184例)或CROSS治疗组(178例)。初始样本量计算是基于CROSS组疗效优于围手术期化疗10%。在第一次无效性分析后,主要研究终点被修改为围手术期化疗的疗效不劣于同步放化疗。2021 ASCO报道了该研究第二次无效性分析的结果,共有143例死亡,新辅助放化疗组70例,新辅助化疗组73例,估计3年生存率分别为56%和57%。基于此数据,数据和安全监察委员会建议结束招募。
今年的ASCO-GI上报道了中位随访34.2(0.43-111.8)个月的结果,共有186人死亡,CROSS 组91人,围手术期化疗组95人,估计的3年生存率分别为57%和55%,HR 1.03(95%可信区间0.77-1.38)。
食管胃结合部癌泛指发生于食管胃解剖交界线上下约5 cm 范围内的腺癌。食管胃结合部癌的最佳综合治疗模式尚不明确。FLOT4-AIO研究中有56%患者为食管胃结合部癌,提示食管胃结合部癌患者围手术期化疗是一种有效治疗方法。CROSS研究结果显示新辅助放化疗+手术与单纯手术相比提高了食管胃结合部癌患者的生存。
对于食管胃结合部癌,新辅助放化疗与围手术期化疗两种治疗模式的疗效是否有差异?与POET研究目的类似,Neo-AEGIS研究旨在比较新辅助放化疗与围手术期化疗治疗食管胃结合部癌的疗效。此次生存结果与既往报道一致,围手术期化疗在生存上不劣于术前放化疗,但在R0切除率和pCR率方面,同步放化疗优于围手术期化疗。
- Poster 354 JCOG1704研究:多西紫杉醇、奥沙利铂和S-1联合D2胃切除加腹主动脉旁淋巴结清扫术治疗有广泛淋巴结转移胃癌的II期研究
- Poster 308 化疗在临床T2N0M0胃癌中的作用
方法:研究纳入的是初治的胃腺癌,胃主要分支动脉周围肿大结节(肿大N)和/或腹主动脉旁转移(PAN);cM0(主动脉旁结节除外);灌洗液细胞学阴性。术前多西紫杉醇、奥沙利铂联合S-1化疗3周期,然后行D2+腹主动脉旁淋巴结清扫术。术后采用S-1辅助化疗1年。主要终点是主要病理缓解率(肿瘤消退超过三分之二)。主要病理反应率的期望值和阈值分别设定为40%和25%。
结果:共纳入47例患者,符合疗效分析的46位患者中,20例仅有块状N,17例仅有PAN,10例同时有块状N和PAN。临床分期:III期19例,IV期28例。46例完成了术前DOS。行胃切除术44例(94%),其中远端胃切除23例,全胃切除21例,R0切除43例(91%)。46例患者中,26例(57%)有明显病理反应,其中pCR 24%。按Becker分级标准,3级13例,2级12例,1b级7例,1a级11例。与手术相关的3/4级毒性反应为腹壁脓肿5例(12%),胰瘘3例(7%)。没有观察到与治疗相关的死亡。
目前,PAN转移在TNM分期中被归为M1期, 视为远处转移,不包括在标准的D2淋巴结清扫范围内。但也有研究者建议考虑将胃癌转移至 PAN视为可切除的病例而不是转移性肿瘤,因为与其他转移性胃癌相比,在此类患者中观察到的长期结局要好得多。JCOG0001、JCOG0405和JCOG1002三项研究均是针对腹主动脉旁淋巴结转移的胃癌患者,术前新辅助化疗联合腹主动脉旁淋巴清扫的Ⅱ期临床试验,结果表明术前化疗然后行D2+腹主动脉旁淋巴结清扫术可以改善患者生存。JCOG1704研究也提示胃癌术前DOS+D2+腹主动脉旁结节清扫术是一种安全、可行的治疗胃癌合并广泛淋巴结转移的方法。
辅 助
对于病理分期I期的胃癌患者是否可以从术后辅助化疗中获益尚不明确。
研究回顾性分析了2006至2017年美国国家肿瘤数据库中术后分期为T2N0M0的3142名胃腺癌患者。将这些患者分为3组:单纯手术组(S)2,090例(66.5%)、手术后辅助化疗组(AC) 360例(11.5%)和围手术期化疗组(POC)692例(22.0%)。采用单变量和多变量COX比例风险模型评价总生存率的差异。根据检查的区域淋巴结数量,患者被分为两个亚组,小于15个(RNE<15个)1526例(49.2%)和大于或等于15个(RNE≥15)1577例(50.8%)。在多变量模型中,手术后辅助性化疗(HR0.75,p=0.003)、RNE≥15(HR 0.73,p=0.001)、在学术机构接受治疗(HR0.84,p=0.005)、女性(HR0.84,p=0.004)和亚裔(HR0.69,p=0.002)的患者有更好的结果。亚组分析显示,围手术期化疗对RNE<15有利(HR0.74,p=0.029)。在多变量模型中,RNE≥15的患者,接受手术后辅助性化疗(HR0.72,p=0.017)的存活率有所提高。
结论:对于T2N0M0期胃癌患者,手术后辅以化疗是有益的。
- Poster 386 Ⅲ期胃腺癌根治性D2切除术后辅助nab-紫杉醇+S-1治疗的III期临床研究
研究旨在评价nab-紫杉醇联合S-1(AS)和奥沙利铂联合卡培他滨(CAPOX)治疗D2根治性胃切除术后III期胃腺癌(GAC)的疗效和安全性。
方法:本研究为3期开放随机研究,入组的是D2根治性胃切除术后病理分期为III期的胃癌患者。随机分为AS组(nab-紫杉醇100 mg/m2,第1、8天;S-1 40~60 mg,每日2次,第1~14天)或CAPOX,每3周重复,共8个周期。主要终点是意向治疗分析的3年无病生存率(DFS)。次要终点包括总体存活率(OS)和安全性。
结果:在2020年3月至2022年8月期间,233名患者被随机分配到研究治疗(AS,115例;CAPOX,118例)。AS的病理分期为IIIA期42.61%,IIIB期34.78%,IIIC期22.61%;CAPOX病理分期IIIA期47.46%,IIIB期30.51%,IIIC期22.03%。AS组1年DFS率为89.0%,CAPOX组为76.9%。AS组的1年OS率高于CAPOX组(100%比95.5%)。AS组复发7例(6.09%),CAPOX组复发11例(9.32%)。AS和CAPOX的复发部位涉及腹膜(1 vs 4)、局部复发(1 vs 2)和远处复发(5 vs 6)。AS(38.26%)和CAPOX(22.03%)患者出现3/4级不良事件(AEs)。AS和CAPOX最常见的不良反应包括贫血(20.96% vs 19.63%)、中性粒细胞减少症(30.70% vs 21.02%)和血小板减少症(1.10% vs 15.47%)。
结论:在这项研究中,AS显示了与CAPOX相比,根治性D2胃切除后III期GAC患者的DFS率、OS率有更长的趋势,有待于更长时间随访结果。
晚期一线(化疗)
- Poster 380 晚期胃癌转化治疗前瞻性多中心II期研究 CCOG1403的长期生存结果
- Poster 313 进展期胃食管腺癌一线两药化疗与三药化疗的真实世界研究
- Poster 347 泽尼达妥单抗+化疗一线治疗HER-2阳性转移性胃食管腺癌的II期临床研究
- Oral Abstract 289 HERIZON:HER2靶向多肽疫苗HER-Vaxx(IMU-131)联合标准化疗治疗HER2过表达的转移性或晚期胃/食管胃结合部腺癌患者的Ⅱ期研究
- Poster 342 应用JCOG1013的资料研究进展期胃癌的预后指标
方法:研究纳入的是初诊不可切除治愈的胃癌患者,1个疗程以上化疗后,行诊断性腹腔镜术或开腹手术。对于可治愈的病例行胃切除术。主要终点是从一线化疗开始算起的3年生存率。
结果:从2014年4月至2019年3月,共纳入30名患者。不可治愈因素包括淋巴结转移,腹膜转移,肝转移等。Yoshida’s的分类:I类 3例,II类16例,III类8例,IV类2例。化疗方案包括SOX(11例)、SP(8例)、XP+HER(8例)、PTX 腹腔灌注方案(6例)和其他方案(12例)。术前化疗疗效评价:PR 24例,SD 6例。手术方式:全胃切除(18例)、远端胃切除(7例)、近端胃切除(1例)。80%(24例)获得R0切除。病理结果显示26.7% (8/30)的患者出现主要反应。在30例患者中,66.3%的患者一线化疗后存活3年以上。
胃癌的转化治疗是针对初始部分不可切除,但有潜在手术切除机会的胃癌患者,接受全身系统化疗后,其不可切除因素出现部分或完全缓解,行R0 切除,从而获得相对较长的术后生存时间和(或)无复发生存时间。目前初始不可切除胃癌转化治疗尚处于探索阶段, 相关研究主要为一些单中心、小样本、回顾性的报道。CCOG1403是小样本前瞻性研究,对于初始不可手术的胃癌患者,经过转化治疗,3年生存率达到66.3%,有待开展随机试验进行验证。
方法:研究分析了美国一电子健康记录(EHR)数据库,比较在一线两药化疗和三药化疗的疗效。研究回顾2011至2022年间接受一线细胞毒性两药或三药治疗的胃及食管胃结合部癌(AGEA)患者。使用Kaplan Meier和Cox比例风险模型比较两组间的生存结果。
结果:5375例符合纳入标准的AGEA患者中,4415例(82%)接受了两药化疗,960例(17%)接受了三药化疗。接受两药化疗患者的中位OS为11个月,与接受三药化疗患者的中位OS(11个月,95%可信区间10-12)相似。控制了性别、种族、吸烟状况、发病地点以及HER2和PD-L1状态等潜在混杂变量的Cox比例风险模型显示,两组的预后没有显著差异(HR 0.9,95%CI 0.8-1)。亚组分析比较FLOT和FOLFOX/CapeOx方案疗效显示,FLOT的mOS改善优于FOLFOX/CapeOx方案(13m vs 10m)。多变量分析中得到一致的结果,与FLOT相比,FOLFOX/CapeOX的死亡风险增加(HR 1.2,95%CI 1-1.4)。
结论:与既往研究一致,这项真实世界的研究没有发现在AGEA中一线使用三药化疗与两药化疗的生存差异。然而,当将分析局限于现代化疗方案时,结果表明,与FOFOX/CapeOX相比,使用FLOT可能存在生存益处。
晚期一线(免疫)
· General Session 286 Rationale 305:替雷利珠联合化疗一线治疗进展期胃或食管胃交界部腺癌的III期临床研究
研究设计
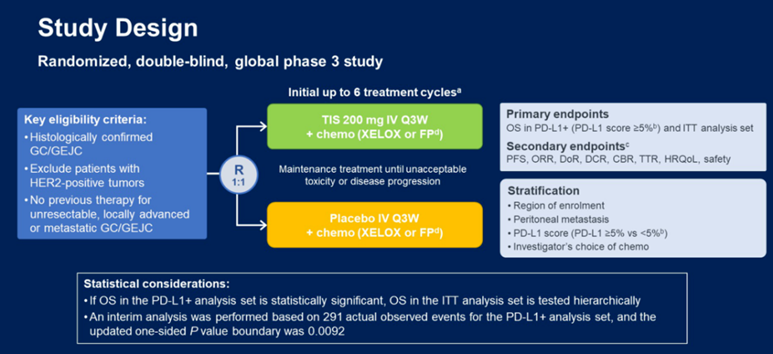
(引自ASCO GI 2023幻灯)
结果:546名PD-L1+患者中,274名患者随机接受替雷利珠联合化疗,272名患者接受安慰剂+化疗治疗。替雷利珠单抗+化疗显示出具有统计学意义和临床意义的OS改善(HR 0.74[95%CI:0.59-0.94],mOS 17.2 vs 12.6个月;单侧P=0.056)。与安慰剂+化疗相比,替雷利珠单抗+化疗的PFS也更长(mPFS 7.2 vs 5.9个月;HR 0.67[95%CI=0.55-0.83]),ORR更高(50.4%vs 43.0%),反应更持久(mDoR 9.0 vs 7.1个月)。
结论:在RATIONALE 305中,替雷利珠+化疗与安慰剂+化疗相比,在OS方面有显著且有临床意义的改善。
· Oral Abstract 325 CheckMate 649研究的3年随访结果
CheckMate 649研究是评估NIVO+化疗一线治疗晚期胃癌/食管胃交界处癌/食管腺癌的III期临床研究。此次会议报道了CheckMate 649的3年随访结果。
结果:581例患者同时随机接受NIVO+化疗或化疗。在至少36个月的随访中,NIVO+化疗继续显示PD-L1 CPS≥5患者和所有随机患者的OS和PFS优于化疗。PD-L1 CPS≥5患者在基线时有可测量病变的客观有效率NIVO+化疗组为60%,化疗组为45%。在所有随机患者中,NIVO+化疗组的ORR为58%(95%CI 54–62),化疗组为46%(95%CI 42–50)。在PD-L1 CPS≥5的患者中,NIVO+化疗组比化疗组的反应更持久,反应中位持续时间分别胃9.6个月 vs 7.0个月,在所有随机患者中(mDOR]8.5个月[9%可信区间7.7-9.9]vs 6.9个月[995%可信区间5.8-7.2])。在大多数预先指定的亚组中观察到NIVO+化疗对OS的益处。
结论:经过3年的随访,NIVO+化疗继续显示出具有临床意义的长期生存益处,具有可接受的安全性,进一步支持其作为先前未经治疗的晚期GC/GEQC/EAC患者的标准1L治疗。
晚期一线(靶向)
· Oral Abstract LBA292 Spotlight研究:佐妥昔单抗+mFOLFOX6一线治疗CLDN18.2+/HER2-局部晚期无法切除或转移性胃或胃食道交界处腺癌的3期研究
方法:初治CLDN18.2+/HER2-不可切除局部晚期或转移性胃或胃食管交界处腺癌患者1:1随机分为佐妥昔单抗+mFOLFOX6或安慰剂+mFOLVOX6。主要终点为PFS。次要终点包括OS、ORR和安全性。
结果:565名患者被1:1随机分为佐妥昔单抗+mFOLFOX6(N=283)或安慰剂+mFORFOX6组(N=282)。佐妥昔单抗+mFOLFOX6显著改善PFS(中位数10.61 vs 8.67个月,HR 0.751,P=0.0066)和OS(中位数18.23 vs 15.54个月,HR 0.750,P=0.0053,)。两组ORR分别为53.8% vs 48.8%。佐妥昔单抗+mFOLFOX6最常见的TEAE为恶心(佐妥昔单抗组与安慰剂组分别为82.4%与60.8%)、呕吐(67.4%与35.6%)和食欲下降(47.0%与33.5%);
结论:佐妥昔单抗+mFOLFOX6显著延长CLDN18.2+/HER2-局部晚期无法切除或转移性胃或胃食道交界处腺癌患者的PFS和OS。
方法:入组的是晚期初治Her-2阳性胃食管腺癌患者,给予泽尼达妥单抗(一种针对ECD4和ECD2的抗HER2双特异性抗体)+化疗的治疗(mFOLFOX6、CAPOX或FP)。
结果:46名接受泽尼达妥单抗+化疗治疗的患者中位随访时间为21.5个月,20名患者(43%)仍在接受治疗。确认的客观缓解率(cORR)为79%,疾病控制率为92%;3名患者获得完全缓解。在所有42例患者中,中位无进展生存期(PFS)为12.5个月,中位总生存期(OS)尚未达到。18个月的生存率估计为87.3%。所有患者中最常见的治疗相关不良事件是腹泻、恶心、周围感觉神经病变、食欲下降、疲劳、呕吐和低钾血症。
结论:对于HER2阳性晚期食管胃腺癌患者,泽尼达妥单抗+化疗是一种高度有效的治疗方案,具有可控的安全性。
Toga研究确立了曲妥珠单抗+化疗一线治疗Her-2阳性胃癌的地位,研究显示,曲妥珠单抗组的中位 PFS 为 6.7个月,中位总生存期为13.8个月,客观有效率达到47.8%。此II期研究结果显示泽尼达妥单抗+化疗有更好的PFS, OS和客观有效率。期待III期研究的结果。
晚期二线及以后
研究设计
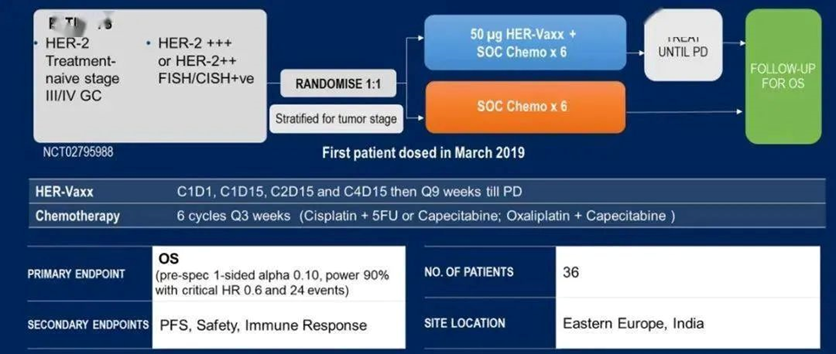
(引自大会讲者报告幻灯)
结果:在36例随机分组的患者中(19例接受HER-Vaxx联合化疗,17例单独化疗),32例患者在最终分析时出现生存事件(分别为15例和17例)。所有患者均接受奥沙利铂+卡培他滨化疗。与单纯化疗相比,HER Vaxx联合化疗的患者存活获益为42%。这转化为HR为0.580(80%双侧CI:0.362,0.927),p值为0.066,有统计学意义。接受HER Vaxx联合化疗的患者的中位OS为14.0个月,而仅接受化疗的患者为8.3个月。HER Vaxx组的中位反应持续时间为30周,单纯化疗组为19周。两个治疗组的安全性没有差异。
结论:这些数据表明,在HER2过度表达的胃/食管胃结合部癌症患者中,HER2主动免疫HER Vaxx是安全的,并提供了超过标准化疗的临床益处。
研究者既往报告过,PS评分≥1,未行胃切除术,转移部位数量≥2,和血清ALP水平高是进展期胃癌不良预后因素,并通过分析JCOG9912研究中的晚期胃癌患者的数据,提出了JCOG预后指数。
方法:使用Cox比例回归模型,回顾性分析预后因素对JCOG1013研究中纳入的的进展期胃癌患者生存的预测价值。
结果:在741名患者中,选择了730名具有本分析所需数据的患者。根据既往JCOG指数,将患者分为良好(n=233)、中等(n=444)和较差(n=53)风险组,三组的中位OS分别为19.0、14.2和9.1个月。与良好组相比,中等组的HR为1.59[95%CI,1.33–1.89;p<0.0001],差组为2.47[95%CI;1.81–3.38;p<0.001]。在7个因素的多变量分析中,单变量分析显示:PS≥1,弥漫型,转移部位数量≥2,NLR(中性粒细胞/淋巴细胞数比值)≥3.1与预后差显著相关,而之前没有胃切除、腹膜转移和血清ALP水平高则无相关性。根据四个新确定的预后危险因素提出改良JCOG预后指数。基于改良JCOG预后指数,患者被分为三组:良好(无危险因素)、中等(1或2)和较差(3或4)三组。良好(n=221)、中等(n=441)和较差(n=68)风险组的中位OS分别为20.6、13.7和9.4个月。与良好组相比,中等组的HR为1.70[95%CI,1.42–2.03;p < 0.0001],差组为3.11[95%CI;2.33–4.14;p <0.001] 。
结论:改良的JCOG预后指数可以将JCOG1013研究中患者的OS明显分层。
本文是蒲汪旸版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论