 三甲
三甲
2023 ESMO 胃癌治疗进展
2023年ESMO年会于10月20日-10月24日在西班牙马德里召开。下面就本次会上胃癌治疗相关研究进展做一梳理。
新辅助
免疫+化疗是近几年胃癌新辅治疗研究的热点,已有多个II期临床研究结果显示免疫+化疗新辅助治疗胃癌有较高的病理完全缓解率(pCR)和主要病理缓解率(MPR)。今年ESMO上报道了MATTERHORN研究、KEYNOTE-585研究和Dragon IV 3项关于免疫联合化疗新辅助治疗胃癌的III期研究的结果。
MATTERHORN研究中期结果:度伐利尤单抗+FLOT治疗可切除的胃和胃食管交界癌的III期临床研究
研究设计
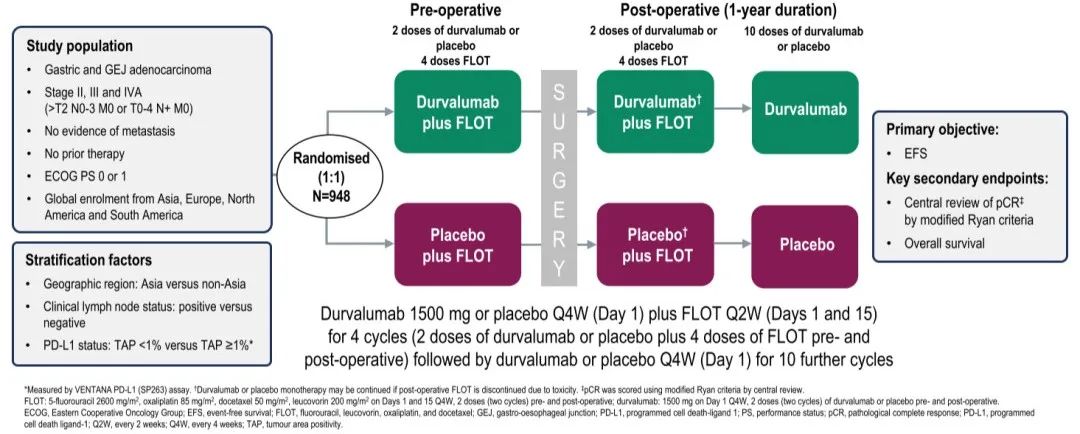
结果:474名患者随机分配到每个治疗组。两组基线特征平衡。患者中,胃癌比例68%、cT3:66%;cT4,25%;cLN+:70%。度伐利尤单抗组的pCR率较安慰剂组有显著改善(19% vs 7%);pCR+接近完全病理反应(pnCR)率在度伐利尤单抗组为27%,在安慰剂组为14%。度伐利尤单抗组的手术率和R0切除率(分别为87%和86%)与安慰剂组(分别为84%和86%)相似。两组之间的不良事件发生率相似。
在围手术期FLOT治疗中添加度伐利尤单抗可以提高pCR率。无事件生存(EFS)情况待后续随访结果。
KEYNOTE-585研究
KEYNOTE-585研究是评估帕博利珠单抗联合化疗新辅助/辅助治疗局部晚期,可切除的胃或胃食管交界处(G/GEJ)癌症疗效的III期临床研究。研究分为两个队列,主队列评估帕博利珠单抗联合顺铂+卡陪他滨/顺铂+5-Fu,FLOT队列评估帕博利珠单抗+FLOT新辅助治疗进展期胃癌的疗效。此次会议报道了主队列第三次中期分析的结果。
研究设计

主要研究终点:BICR评估的pCR、研究者评估的EFS、OS(主队列)、安全性(FLOT队列)
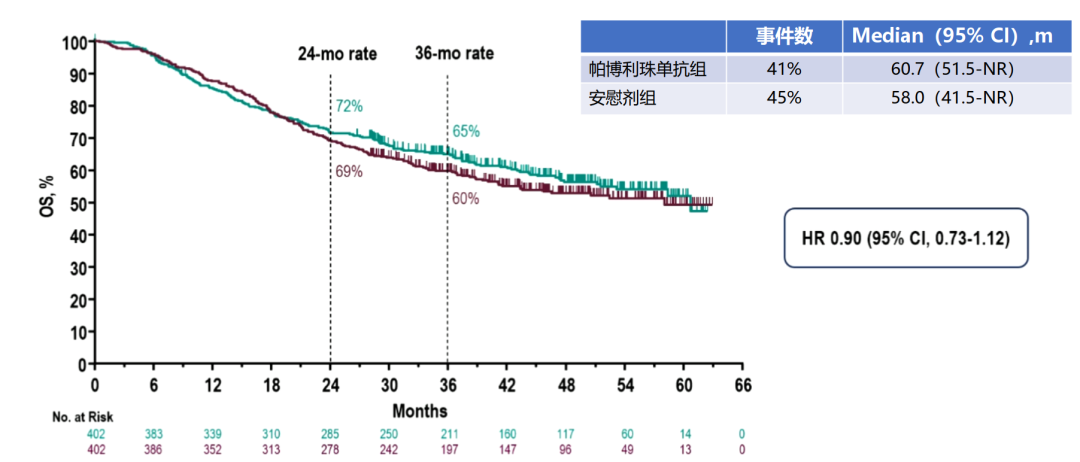
结果:两队列共纳入1007名患者,主队列中帕博利珠单抗组和安慰剂组各402名患者。FLOT队列帕博利珠单抗组100名,安慰剂组103名患者。主队列中,与安慰剂组相比,帕博利珠单抗组的pCR率(12.9% vs 2%,P<0.00001)明显提高; EFS有延长趋势(44.4 vs 25.3 m;P=0.0198),但统计学差异不显着。两组中位OS分别为60.7 vs 58.0 m(HR 0.90;95%CI,0.73-1.12)。由于EFS的改善无统计学意义,研究没有正式评估OS主要终点。
EFS亚组分析
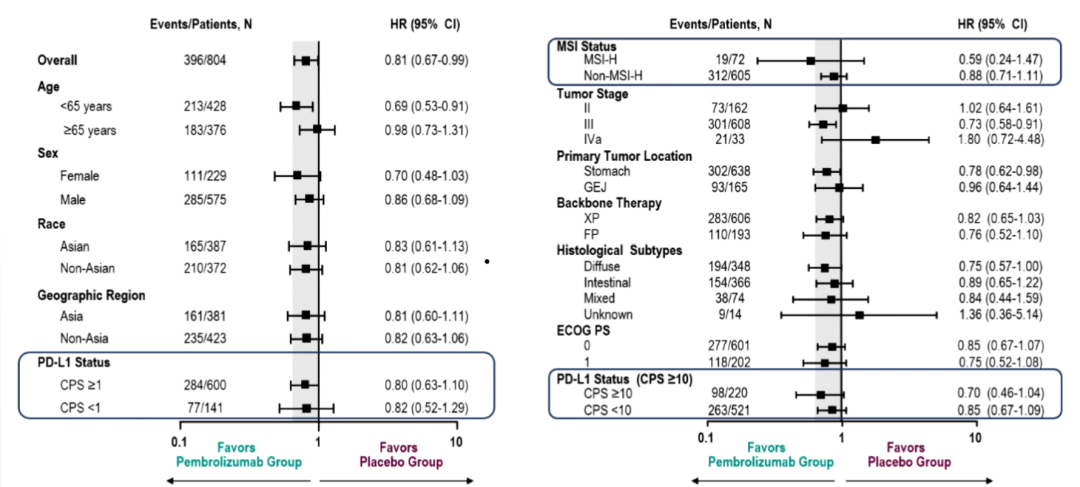
主队列组的OS
Dragon IV 研究中期分析:卡瑞利珠联合阿帕替尼和化疗治疗局部晚期可切除胃或胃食道交界部(G/GEJ)腺癌的III临床研究
研究设计
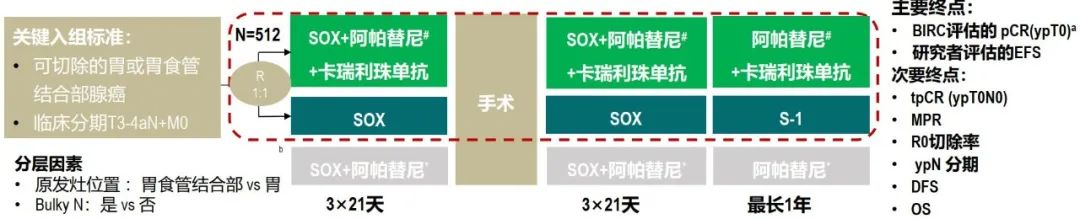
结果:SOX+阿帕替尼+卡瑞利珠组和SOX组各入组180例患者。两组患者的新辅助完成率为分别为91.1% vs.93.9%;手术完成率为86.1% vs.86.7%。
SOX+阿帕替尼+卡瑞利珠组与SOX组相比,pCR率提高了13.7%(95% CI 7.2-20.1,p<0.0001),两组的pCR率分别为18.3%(95% CI 13.0-24.8)和5.0%(95% CI 2.3-9.3);两组患者MPR率为51.1%和37.8%。
整个治疗期间,SOX+阿帕替尼+卡瑞利珠组与SOX组对比,≥10%的治疗相关不良事件(TRAEs)包括中性粒细胞减少、白细胞计数降低和血小板减少等,其中≥3级以上TRAEs包括:中性粒细胞减少(19 % vs. 10.1%),白细胞计数降低(8.4% vs 3.9%)、血小板减少(11.7% vs. 10.7%)、体重减轻(5.6% vs. 2.8%)、高血压(5.6% vs. 0)、γ-谷氨酰转移酶升高(6.7% vs. 0)等。
SOX+阿帕替尼+卡瑞利珠与单纯化疗相比明显提高pCR率,期待EFS的结果。
RESOLVE研究结果更新
RESOLVE研究是比较奥沙利铂联合S-1(SOX)的围手术期化疗与SOX或奥沙利铂联合卡培他滨(XELOX)的术后化疗治疗局部进展期胃腺癌疗效的III期临床研究。2019年的ESMO大会上报告了研究结果,与术后XELOX方案辅助化疗(B组)相比,围手术期SOX方案化疗(C组)提高了3年无病生存率(59.4%)。术后SOX(A组)3年DFS率为56.5%,不劣于术后XELOX(51.1%)。今年ESMO大会上,张小田教授公布了RESOLVE研究5年生存结果。
研究设计
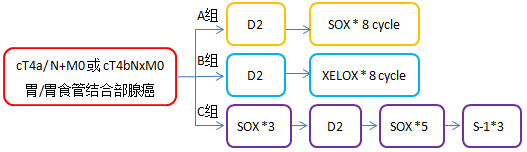
主要研究终点3年DFS,次要研究终点5年总体生存率和安全性
结果:SOX围手术期治疗与CapOx相比改善患者5年OS% (60.0% vs 52.1%;HR 0.79,95%CI [0.62-1.00],p=0.049),SOX围手术期治疗较CapOx显著降低21%的死亡风险;SOX术后辅助治疗非劣于CapOx(61.0% vs 52.1%;HR 0.77,95%CI [0.61-0.98], p=0.033)。SOX围手术期治疗与CapOx相比显著改善患者5年DFS% (53.2% vs 45.8%;HR 0.79,95% CI[0.63-0.98];p=0.034)。
晚期一线
Keynote-811:帕博利珠单抗联合曲妥珠单抗和化疗治疗Her-2阳性转移性胃或胃食道交界部腺癌的III临床研究
研究设计
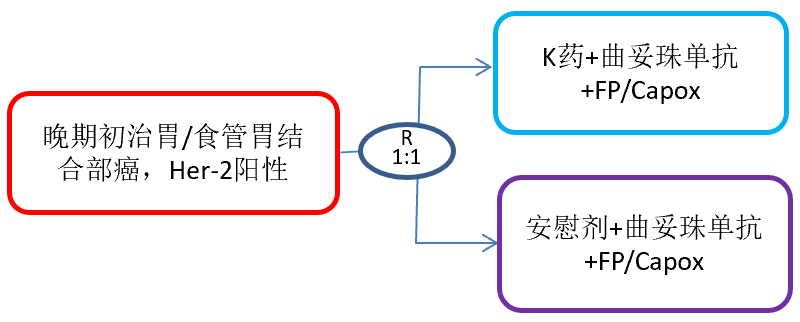
研究主要终点:PFS和OS;关键次要终点:ORR和DOR
结果:共纳入698例患者,帕博利珠单抗组350例,对照组348例,两组的PFS分别是10.0和8.1m;HR 0.72;95%CI 0.60~0.87;p=0.0002)。在PD-L1 CPS≥1患者中,两组的中位PFS分别为10.8mo和7.2mo(HR 0.70;95%CI,0.58~0.85)。
OS 仍在随访中。目前两组的OS分别为20和16.8m。
帕博利珠单抗组和对照组的ORR分别为73%和58%,在 PD-L1 CPS≥1 的患者中,ORR 分别为 73.2% 和58.4%。中位缓解持续时间(DOR)分别为 11.2 个月和 9.0 个月。大约 31% 和 19%的应答者的应答持续时间 ≥24 个月。
Her-2阳性晚期胃癌帕博利珠单抗+曲妥珠单抗+化疗明显提高客观有效率,延长PFS。
NO LIMIT研究的初步结果(WJOG13320G/CA209-7W7):纳武利尤单抗加低剂量伊匹单抗一线治疗进展期胃或食道胃交界处MSI-H腺癌患者的II期研究
研究设计:纳入MSI-H、不能切除的晚期、复发或转移性、初治胃腺癌患者,给予纳武利尤单抗 240 mg q2w,伊匹单抗 1 mg/kg q6w,直至病情进展或出现不可接受的毒性。主要终点为客观有效率(ORR)。
结果:2020年11月至2022年8月,从935例筛查病例中纳入29例患者。中位年龄为75岁(54-84岁),其中44.8%为男性。ORR为62.1%(95%CI:42.3-79.3),其中3名患者(10%)完全缓解。DCR为79.3%(95%CI,60.3~92.0)。中位PFS为13.8(95%可信区间,13.7-NR)个月,中位DOR和OS尚未达到。停止治疗的最常见原因是不良事件。安全性与已知的nivolumab加小剂量ipilimumab的不良反应一致。
结论:在MSI-H GC患者中,联合应用nivolumab和小剂量ipilimumab的非化疗策略显示出高而稳健的疗效和良好的耐受性。
RATIONALE-305研究结果更新
RATIONAL-305是评估铂/氟嘧啶联合替雷利珠单抗一线治疗局部晚期或转移性胃/胃食管结合部腺癌患者的安全性和有效性的III期临床研究。2023年ASCO-GI上报道了研究结果,与安慰剂相比,替雷利珠单抗能够明显延长患者中位OS(17.2m vs 12.6m)。替雷利珠单抗与安慰剂组的PFS分别胃 7.2 vs 5.9个月;ORR分别为50.4%vs 43.0%。本次会议上公布了RATIONALE-305试验的最终分析结果。
研究设计

结果:997名患者被随机分配至试验组(n=501)或安慰剂组(n=496)。与ITT人群中安慰剂组相比,试验组的OS显著改善,两组中位OS分别为15.0个月和12.9个月。其它主要疗效结果见下表:
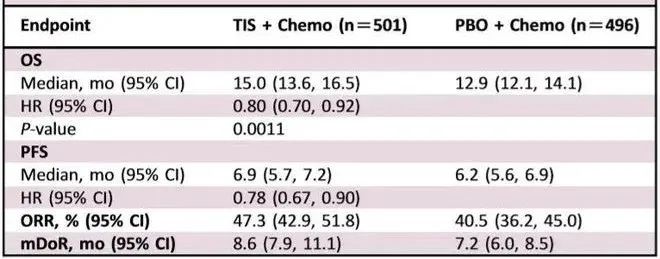
GLOW研究数据更新
GLOW研究是评估Zolbetuximab联合CAPOX用于治疗Claudin18.2阳性胃或食管胃结合部腺癌的随机对照III期研究。2023年ASCO大会上报道了GLOW研究的结果,Zolbetuximab组对比安慰剂组延长了PFS(8.21 vs 6.8m,P=0.0007)和OS(14.39 vs 12.16m,P=0.0118)。试验组和对照组的ORR分别为42.5% VS 40.3%。本次ESMO会议上更新了疗效和安全性数据。
研究设计
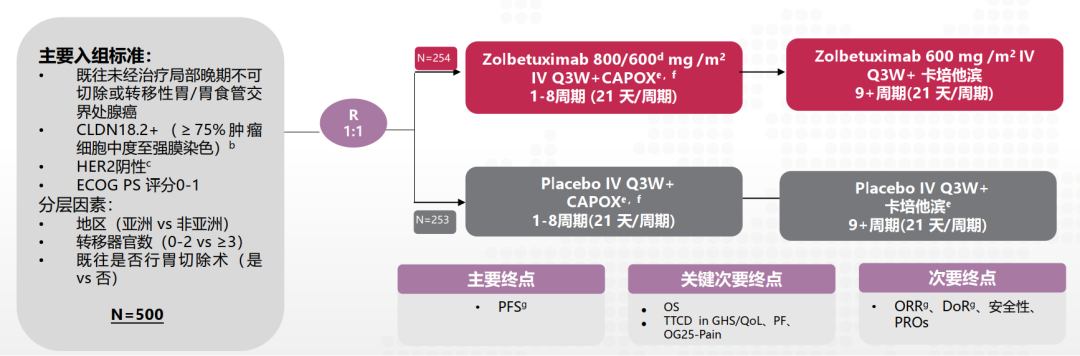
结果:在数据截止点(2023年6月29日),507名患者被分配到Zolbetuximab+CAPOX(n=254)或PBO+CAPOX(n=253)。zolbetuximab组与安慰剂组的中位PFS分别为8.3和6.8个月(HR 0.68[95%CI 0.55,0.85])。
Zolbetuximab组和安慰剂组中位OS分别为14.3和12.2个月(HR0.77[95%CI 0.62,0.95]);24个月OS发生率为28.3%对18.8%.
对可测量病灶的患者中进行事后分析,Zolbetuximab组和安慰剂组的ORR分别为54.1% vs 48.5%。
Zolbetuximab组最常见的治疗相关不良反应是恶心(Zolbetuximab组:68.9% vs PBO组:50.2%)、呕吐(66.1%vs 31.3%)和食欲下降(41.3%vs 34.5%);两组之间严重不良反应发生率相似(48.0%对50.6%)。
Spotlight研究结果更新
Spotlight是评估佐妥昔单抗+mFOLFOX6一线治疗CLDN18.2+/HER2-局部晚期无法切除或转移性胃或胃食道交界处腺癌的3期研究,今年ASCO-GI上公布了研究结果结果,与安慰剂相比,佐妥昔单抗+mFOLFOX6显著改善PFS(10.61 vs 8.67个月)和OS(18.23 vs 15.54个月)。两组ORR分别为53.8% vs 48.8%。此次会议更新了疗效和安全性数据。
研究设计
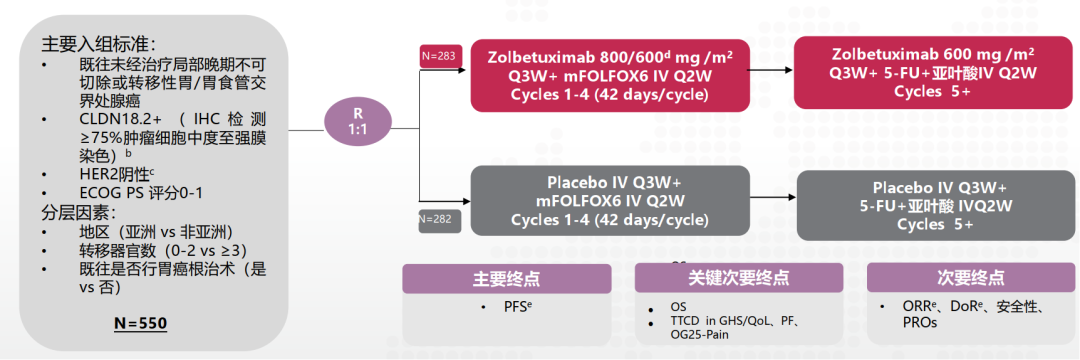
结果:在数据截止日期(2023年6月29日),佐妥昔单抗组(n=283)与安慰剂组(n=282)的中位PFS分别为11.0 vs 8.9个月(HR 0.73[95%CI 0.59,0.91],P=0.0022);中位OS为18.2 vs 15.6个月(HR0.78[95%CI 0.64,0.95],P=0.0067);独立评审委员会评估的ORR分别为61.1% vs 62.4%。
恶心、呕吐、食欲减退是Zolbetuximab联合mFOLFOX6最常见的治疗相关不良事件 ,这与GOLOW研究(Zolbetuximab联合CAPOX)最新的分析结果一致。
晚期二线及以后
RINDBeRG试验: 雷莫西尤单抗联合伊立替康对比伊立替康三线或后线治疗雷莫西尤单抗治疗过的晚期胃癌的III期临床研究
研究设计
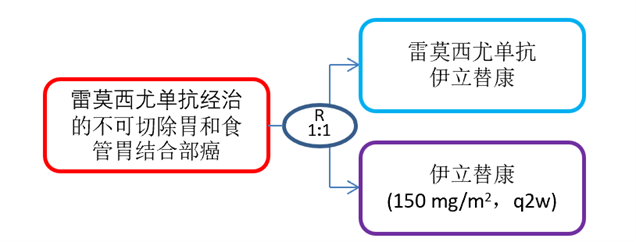
主要终点是总生存期
结果:共纳入402名患者,雷莫西尤单抗组202名,伊立替康组200名。两组的中位OS分别为9.4个月和8.5个月(校正HR 0.909,95%置信区间0.738-1.119;p=0.369)。中位PFS分别为3.8个月和2.8个月(HR 0.722,95%CI 0.590-0.884;p=0.001),ORR分别为22.1%(33/149)和15.0%(25/167)。
雷莫西尤单抗耐药后,在伊立替康中加入雷莫西尤单抗可改善PFS和ORR,毒性可控,但未达到OS的主要终点。
Infigratinib治疗FGFR2基因扩增的局部进展期或转移性胃癌或胃-食管交界腺癌患者的疗效和安全性
FIGHT研究结果显示评价贝马妥珠单抗(bema)联合mFOLFOX6一线治疗FGFR2b+晚期胃/胃食管交界处腺癌与单纯化疗相比,显著改善无进展生存期(中位PFS:9.5个月 vs 7.4个月;HR=0.68)和总缓解率(ORR:46.8% vs 33.3%)。Infigratinib是一种口服的、ATP竞争性的成纤维细胞生长因子受体酪氨酸激酶抑制剂(TKI),靶向纤维细胞生长因子受体(FGFR)蛋白,阻断下游活性。
LB1001-201试验(NCT05019794)队列1评估infigratinib在既往二线或以上系统治疗失败的、伴有FGFR2基因扩增(FISH检测)的局部进展期或转移性胃癌或胃食管结合部腺癌的疗效和安全性。ORR为25.0%,DCR为80.0%,mDOR为3.8个月,mPFS 3.3m,mOS 8.0m。15/19例肿瘤缩小,最大缩小幅度达78.5%。≥三级TRAE占42.9%。
本文是蒲汪旸版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论