 三甲
三甲
2024 ASCO-GI 胃癌研究进展
新辅助治疗
MATTERHORN研究:度伐利尤单抗+FLOT治疗可切除的胃和胃食管交界癌病理完全缓解的地区亚组分析结果
研究设计
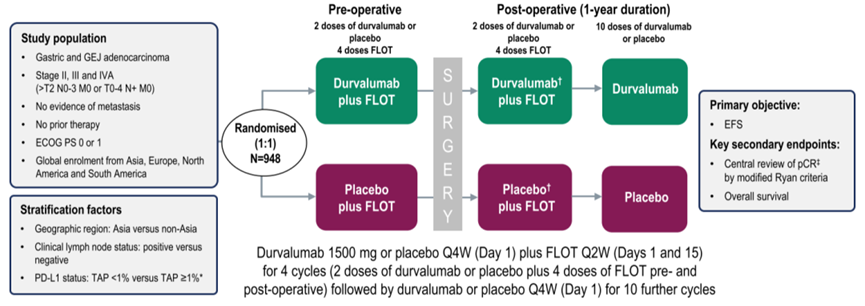
MATTERHORN研究旨在评估度伐利尤单抗+FLOT治疗可切除的胃和胃食管交界癌的III期临床研究。2023年ESMO会议上报道了中期分析结果。研究共纳入948例患者中,度伐利尤单抗组的pCR率较安慰剂组有显著改善(19% vs 7%)。pCR+接近完全病理反应(pnCR)率在度伐利尤单抗组为27%,安慰剂组为14%。
今年ASCO-GI上,公布了地区亚组分析结果。所有患者中,180例(19%)来自亚洲。在不同国家的亚组中,观察到与安慰剂联合FLOT相比度伐利尤单抗联合FLOT治疗的pCR均有改善。
KEYNOTE-585研究中FLOT队列列第三次中期分析的结果
KEYNOTE-585研究评估帕博利珠单抗联合化疗新辅助/辅助治疗局部晚期可切除的胃或胃食管交界处(G/GEJ)腺癌的疗效。研究分为两个队列,主队列评估帕博利珠单抗联合顺铂+卡陪他滨/顺铂+5-Fu,FLOT队列评估帕博利珠单抗+FLOT的疗效。
研究设计

主要终点:BICR评估的pCR、研究者评估的无事件生存期(EFS)、OS(主队列)、安全性(FLOT队列)
2023年ESMO大会上报道了主队列的结果。帕博利珠单抗组pCR率(12.9% vs 2%,P<0.00001)明显提高; EFS有延长趋势(44.4 vs 25.3 m;P=0.0198),但统计学差异不显着。
此次ASCO-GI会议上报道了FLOT队列结果。FLOT队列共有203 名患者,帕博利珠单抗组100 名,安慰剂组 103 名。140人(69%)为淋巴结阳性(N+),79人(39%)基线时患有胃食管腺癌。帕博利珠单抗组和安慰剂组的 R0切除率分别为 79% 和 80%。CR率分布为17.0%(95% CI,10.2-25.8)和6.8%(95% CI,2.8~13.5)。帕博利珠单抗组中位 EFS未达到,安慰剂组为 30.9 个月。两组患者均未达到中位 OS,两组患者24个月的OS率分别为72%和73%。
MATTERHORN和KEYNOT-585都是关于免疫联合化疗应用于胃癌围手术期治疗的III期临床研究。两个研究入组的都是T≥3或N+性的患者。研究结果上看,杜伐利尤单抗/帕博利珠单抗联合FLOT方案的pCR率非常接近,期待EFS和PD-L1表达亚组的结果。
晚期一线
比较多西他赛-奥沙利铂-卡培他滨/5-氟尿嘧啶(DOC/F)然后多西他赛维持与CAPOX/mFOLFOX-7治疗晚期胃癌的疗效随机开放标签前瞻性III期临床研究(DOC-GC研究)
研究设计
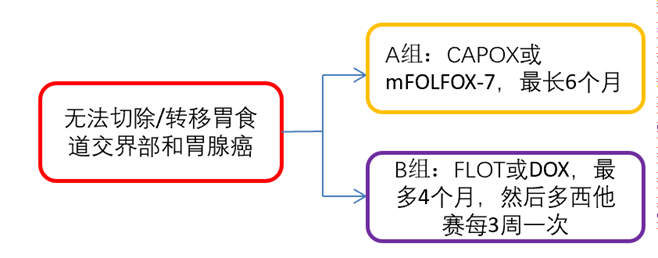
主要终点:OS;次要终点包括无进展生存率和不良事件发生率
结果:在2020年7月至2022年11月期间入组的324名患者中,305名患者可进行评估分析(A组:156例;B组:149例)。A组和B组的中位OS分别为10.1个月(95%:9.2-10.9)和8.9个月(95%可信区间:7.3-10.5),差异无统计学意义[p=0.70]。两组中位PFS差异无统计学意义[A组:7.1个月(95%CI:6.1-8.1);B组:6.2个月(95%CI:5.7-6.8);P=0.39]。B组患者出现3/4级中性粒细胞减少症的比例高于A组(21%比5.1%;p<0.001),其他与治疗相关的副作用在两组患者中相似。与B组相比,A组患者倾向于接受二线治疗的比例更大(38%比26%;p=0.07)。
晚期胃癌一线的化疗方案是选择两药,还是三药,争论由来已久。三药方案 DCF 虽然在III期研究中达到了研究终点,但不良反应亦有明显增加,限制了它的临床运用。JCOG1013研究显示在CS的基础上加上多西他赛(DCS方案)并未改善生存期。此次会议报告的DOC-GC研究也显示由5-氟尿嘧啶/卡培他滨和奥沙利铂组成的双重方案中增加多西紫杉醇并不能改善晚期GEJ/G癌症患者的生存。JCOG1013和DOC-GC研究探索增加一个药物的疗效,可能考虑到不良反应,对其他两药的剂量强度也进行了变更。其次,后线的治疗可能会影响OS的结果。
晚期后线
NIVOFGFR2研究:纳武利尤单抗联合 CapeOX 对既往未经治疗的 FGFR2 阳性、PD-L1 阳性晚期胃癌患者的疗效和安全性:单臂、多中心、2 期研究
方法:入组初治、转移性、HER2 阴性、PD-L1 CPS≥5(DAKO 28-8)、FGFR2 2+或3+(Abcam EPR24075-418)胃腺癌患者。患者接受纳武利尤单抗联合 CapeOX治疗。主要终点是1年PFS率。
结果 纳入23名患者,78%患者有≥2个转移灶;CPS(5-9)22%,(≥10)78% 。1年PFS率为30.4%。中位PFS为 6.2 个月(95% CI 4.4-7.6)。ORR为21.7%,其中有1例完全应答。数据截止时的中位随访时间为11.8个月,未达到中位OS。9例(39.1%)患者出现了3级治疗相关不良反应。
纳武利尤单抗联合化疗已被批准用于PD-L1阳性转移性胃癌的一线治疗。FGFR2在 30% 的胃癌患者中过表达。FIGHT研究显示bemarituzumab+mFOLFOX6一线治疗FGFR2阳性的不可切除胃癌的能够延长PFS,客观缓解率为57.9%。对于PD-L1 CPS≥5同时FGFR2阳性患者是选择免疫联合化疗还是bemarituzumab联合化疗?NIVOFGFR2研究中期分析表明,nivolumabin与化疗联合治疗FGFR2阳性、PD-L1阳性转移性GC患者疗效一般, 安全性可接受。
德曲妥珠单抗作为新辅助治疗 HER2 阳性胃癌和胃食管交界腺癌的II期研究(EPOC2003)。
方法 纳入符合条件的患者为临床分期为T2-4和/或N+、无远处转移、既往未经治疗的局部进展期胃癌或胃食管结合部腺癌。研究包括主队列和探索性队列。主要队列是HER2阳性的患者,定义为IHC 3+或IHC 2+,局部评估为ISH+。探索性队列是HER2低表达(IHC1+或2+,ISH阴性)且血清HER2-ECD超过11.6 ng/ml的患者。术前德曲妥珠单抗治疗3个周期,然后手术。主要终点是中央评估的主要病理反应(MPR)率,预期为45%,无效阈值为20%。主队列的计划样本量为27例,单侧α为10%,功率为90%,另外10例纳入探索性队列。
结果 2021年11月至2022年11月,27名患者被纳入主队列。大多数患者的 IHC3+(24 人)。临床分期从 II/III/IVa分别为2/21/4 例。其中,26 人完成了计划的 3 个疗程的T-DXd,1人因毒性中止治疗。25名患者完成了R0切除术,1名患者进行了R1切除术。MPR率为14.8%,未超过预定的20%。pCR率为3.7%。
结论 在这项 2 期研究中,德曲妥珠单抗对晚期 HER2 阳性胃癌或胃食管腺癌具有适度的单药活性。计划在围手术期将T-DXd与卡培他滨和durvalumab联合使用,以评估是否能提高疗效和预后。
输注氟尿嘧啶和每周多西他赛一线治疗骨髓转移(BMM)和弥散性血管内凝血(DIC)胃癌的多中心 II 期试验
方法:这是一项单臂试验。采用西蒙两阶段优化设计。符合条件的病例包括年龄18- 75岁,组织学确诊为胃癌,已有BMM,明显DIC,血小板≤50*109/L,ECOG评分≤3。氟尿嘧啶 200 mg/㎡,d1-21;多西他赛 25 mg/㎡,d 1、8、15,q4w。血液学反应(HeR)的定义是血小板恢复到正常范围。主要终点为HeR率。次要终点是达到HeR的时间(TTHeR)、一个月死亡率(OMM)、OS、不良事件(AE)和生活质量( QoL)。
结果:2021 年 1 月至 2022 年 9 月,来自中国三个中心的 24 例HAGC病例入选(详见下表)。共完成 20 例 HeR,HeR 率为 83.3%。中位TTHeR 为 13 天,OMM 为 12.5%。中位 OS 为 242 天。7名患者(29.2%)发生了3级不良反应,其中最常见的是口腔炎(4例,16.7%)和转氨酶升高(3例,12.5%)。治疗期间和治疗后的生活质量均有明显改善。
伴有骨髓转移和弥散性血管内凝血的胃癌预后很差。由于血小板减少,这类患者能否从细胞毒性药物治疗中获益不清楚。本研究中氟尿嘧啶+多西他赛方案耐受性良好,在1线治疗中显示出良好的疗效。
胃癌伴巨大淋巴结转移的新辅助化疗后预防性主动脉旁淋巴结清扫术
在日本,广泛淋巴结转移包括沿腹腔动脉及其分支的巨大淋巴结转移(巨大N2)和主动脉旁淋巴结转移(PAN)。新辅助化疗(Noadjuvant chemotherapy,NAC)后进行D2胃切除术和主动脉旁淋巴结清扫术(PAND)是广泛淋巴结转移( ELM)胃癌的标准治疗。然而,PAND 对有 Bulky N2 但无PAN 受累的胃癌的益处尚不清楚。本研究旨在评估NAC 后预防性 PAND 对这部分患者的疗效。
方法 回顾性研究了 2008 年至 2019 年期间因Bulky N2(+)但 PAN(-)胃癌接受新辅助化疗后进行R0胃切除术的 21 例患者。肿大淋巴结的定义为一个淋巴结 3厘米或两个相邻淋巴结各 1.5 厘米。患者分为两组:D2+PAND 组(11 例)和D2 组( 10 例)。我们比较了两组患者的临床病理特征、复发模式和生存结果。
结果:与D2组相比,D2+PAND组的手术时间更长(p=0. 006),组织学类型倾向于未分化(p=0.063),病理反应更好(p=0.086),辅助化疗率更高( p=0.090)。两组患者的 yp 分期相似。D2+PAND组有两名患者(18%)发现病理 PAN转移。D2组有7例(70%)患者复发,D2+PAND组有3例( 27%)患者复发。两组复发患者中,分别有4例(40%)和1例(10%)患者出现淋巴结复发。D2+PAND组的总生存期、无复发生存期和疾病特异性生存期明显优于D2组( P分别为0.008、0.008和0.020)。
结论 NAC后预防性PAND可降低Bulky N2但未累及PAN的局部晚期胃癌的复发风险。
特瑞普利单抗联合CAPOX新辅助治疗dMMR/MSI-H局部进展期胃癌或食管胃交界腺癌的临床研究:NICE II期试验C组的结果。
方法:NICE试验是一项多中心、多队列II期试验,队列C评估特瑞普利单抗联合CapeOX方案作为围手术期治疗dMMR/MSI-H的局部GC或EGJC的安全性和有效性。纳入影像学和腹腔镜分期cT3-4aNxM0 或 cT2N+M0患者。患者(pts)在手术前后接受了特瑞普利单抗240mg联合标准剂量CapeOX方案。主要终点是主要病理反应率。
结果:14名患者术前完成了全部4个周期的治疗,1名患者因AEs完成了2个周期的治疗。无一人出现疾病进展,1名患者在放射学和内镜检查中获得完全临床反应并拒绝手术,其他14名患者均接受手术治疗,R0切除率为100%(14/14)。pCR率为78.6%( 11/14)。5例患者(15例)发生了与治疗相关的3/4级AE。一名患者在两个周期治疗后出现了3级免疫相关肝毒性,在接受类固醇治疗后痊愈。没有患者在围手术期死亡,一名患者在术后238天死于COVID-19,且未复发。所有患者均未发现疾病复发。mIHC显示,达到pCR的患者治疗后肿瘤区域内的CD20+ B细胞、CD3+ T细胞、NK dim细胞和M1巨噬细胞明显减少。
目前,dMMR/MSI-H 是公认的胃癌免疫治疗疗效预测标志物。Keynote-059、Keynote-061和Keynote-062研究中的MSI-H胃癌患者,帕博利珠单抗的ORR分别未为57.1%,46.7%和57.1%,Keynote-062研究中帕博利珠单抗加化疗的ORR为64.7%,单纯化疗的ORR为36.8%。2023年ESMO公布的NO LIMIT研究的初步结果显示纳武利尤单抗加低剂量伊匹单抗一线治疗进展期胃或食道胃交界处MSI-H腺癌患者ORR为62.1%(95%CI:42.3-79.3),中位PFS为13.8。
卡瑞利珠单抗联合阿帕替尼和SOX一线治疗产甲胎蛋白胃或胃食管交界处腺癌患者:一项单臂、多中心、II期试验
方法:纳入初治不可切除/复发或转移性G/GEJ腺癌、血清AFP>2ÍULN或IHC染色法AFP阳性。患者接受 4 个周期的标准 S-1 加奥沙利铂和卡瑞利珠单抗加阿帕替尼(250毫克,每天 1 次)治疗。随后卡瑞珠单抗加阿帕替尼治疗达24个月或疾病进展或不可接受的毒性反应。主要终点是ORR。
结果:共有36名患者入组并接受治疗。35例患者可评估肿瘤反应。中位年龄为63岁,其中30名患者为男性。94.5%的患者为IV 期。血清AFP水平中位数为 739.8 ng/ml。疗效在FAS 群体(n = 36)中进行了评估。2例完全应答(CR,全部确认),22例部分应答(P R,18例确认),7例病情稳定(SD)。因此,未经证实的ORR为66.7%(24/36),DCR为 86.1%(31/36),证实的ORR为55.6%( 20/36)。中位PFS 和OS 尚不成熟。13名患者(36.1%)发生了3级不良事件。最常见的3级TRAE是中性粒细胞计数下降(13.9%)、高血压(8.3%)和腹泻(5.6%)。
结论 在既往未接受过系统治疗的AFP生成型G/GEJ腺癌患者中,卡瑞利珠单抗联合阿帕替尼与SOX联合治疗后,再用卡瑞利珠单抗联合阿帕替尼治疗,显示出良好的抗肿瘤活性和可接受的安全性。
本文是蒲汪旸版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论