
纳武利尤单抗树立尿路上皮癌术后辅助治疗新标准
免疫治疗的发展为恶性肿瘤的诊疗带来了全新的思路,已成为泌尿肿瘤不可或缺的治疗手段。随着CheckMate-274研究取得突破性进展,尿路上皮癌辅助治疗免疫时代的大门已然打开。2023年1月,纳武利尤单抗成为我国首个且目前唯一获批用于尿路上皮癌辅助治疗的PD-1抑制剂。随后,在2023年美国临床肿瘤学会泌尿生殖系统肿瘤研讨会(ASCO-GU)和美国泌尿外科协会年会(AUA)上,CheckMate-274研究3年随访数据的更新更是给学界带来极大的惊喜,为尿路上皮癌辅助免疫治疗树立了新标准。
本辑由南京医科大学第一附属医院吕强教授、中国医科大学附属第一医院刘涛教授、青岛大学附属医院王科教授 专家访谈系列节目,大咖同道共话尿路上皮癌术后辅助治疗格局的改变以及新标准的建立。
有的放矢
辅助免疫治疗成为高复发风险尿路上皮癌治疗优选
尿路上皮癌是泌尿系统的常见肿瘤之一,其中膀胱尿路上皮癌占比为90%-95%。根治性切除术是尿路上皮癌的主要治疗方式之一,但尿路上皮癌术后出现复发或转移的患者比例较高且预后较差。数据显示,肌层浸润性膀胱癌(MIBC)患者术后5年复发率约30%,近80%复发患者在1年内死亡。因此,存在高复发风险的尿路上皮癌患者仍存在很大未被满足的临床需求。刘涛教授表示,手术切缘阳性的患者¹、行新辅助化疗术后且病理分期≥ypT2的患者²、未行新辅助化疗且术后病理分期≥pT3的患者³以及淋巴结阳性的患者⁴,都是尿路上皮癌高复发风险人群。积极进行术后辅助治疗,可以显著改善这部分人群的生存获益。
对于术后辅助治疗方案的选择,刘涛教授指出,对根治性切除术后的高复发风险患者,通常选择含铂类联合化疗。但是患者是否愿意接受化疗、是否耐受化疗、化疗可能导致的过度治疗以及化疗易受术后并发症影响导致治疗延迟等情况限制了化疗的使用。因此,辅助化疗的应用并不广泛。中国临床肿瘤学会(CSCO)尿路上皮癌指南⁵提及术后辅助放疗可能可以提高部分患者的局部肿瘤控制率,但是证据等级并不高。同时,放疗方案和疗效的难以统一、放疗导致的放射性不良反应也限制了辅助放疗的应用。
免疫时代的到来,无疑是尿路上皮癌的福音,刘涛教授补充道。在尿路上皮癌辅助免疫治疗领域的探索中,虽然IMvigor010试验⁶最终只取得阴性结果,但CheckMate-274研究⁷达到了主要研究终点,纳武利尤单抗组的中位无病生存期(DFS)较对照组翻倍,为患者带来了深入、持久的获益。可以说CheckMate-274研究的成功,开启了尿路上皮癌辅助治疗的免疫新时代,并成功改写了国家综合癌症网络(NCCN)和CSCO等一众国内外权威指南。纳武利尤单抗在国内获批此适应症,将造福更多中国尿路上皮癌患者。
吕强教授总结道,既往高复发风险尿路上皮癌患者的常规选择是化疗,但患者可能无法耐受全剂量化疗以及化疗的副作用等都为患者治疗的依从性和完整性带来局限。想要真正提高患者的长期生存获益,综合治疗非常关键。CheckMate-274研究达到了阳性结果,在尿路上皮癌辅助治疗领域取得重大突破,打开尿路上皮癌辅助治疗免疫时代的大门,为患者带来了切实的临床获益。
一枝独秀
纳武利尤单抗辅助治疗为患者带来长期获益
基于顺铂的化疗方案,特别是新辅助化疗可以改善尿路上皮癌患者的预后,但术后辅助化疗作用仍存在一定争议。随着治疗方式的不断拓展,辅助免疫治疗的探索逐渐丰富,并取得惊艳成绩。王科教授表示,CheckMate-274研究⁷是全球首个证实免疫疗法辅助治疗肌层浸润性尿路上皮癌,可显著降低患者疾病复发风险的多中心全球III期研究。2023 ASCO-GU和AUA年会上最新公布的36.1个月随访数据⁸显示:在所有随机(ITT)人群中,纳武利尤单抗组的DFS是对照组两倍以上(22.0个月 vs. 10.9个月),复发或死亡风险降低29%。

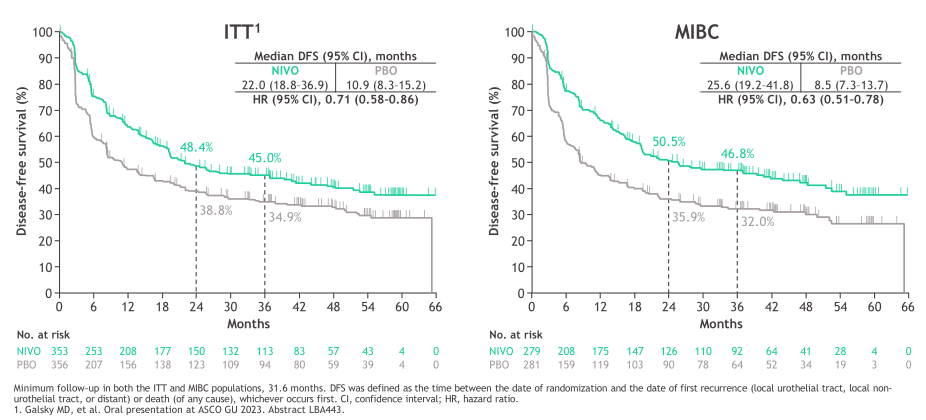
图1 与安慰剂相比,纳武利尤单抗在ITT人群和MIBC亚组人群的DFS获益
在肿瘤细胞PD-L1表达≥1%的患者中,纳武利尤单抗组的中位DFS甚至达到对照组的6倍以上(52.6个月 vs 8.4个月),复发或死亡风险降低48%。此外,纳武利尤单抗组的尿路外无复发生存期(NUTRFS)、无远处转移生存期(DMFS)和PFS2结果均具有优势。同时,在MIBC亚组中,纳武利尤单抗组的DFS是对照组的近3倍(25.6个月 vs 8.5个月),疾病复发或死亡风险降低37%;NUTRFS、DMFS等结果均与所有随机人群保持一致。

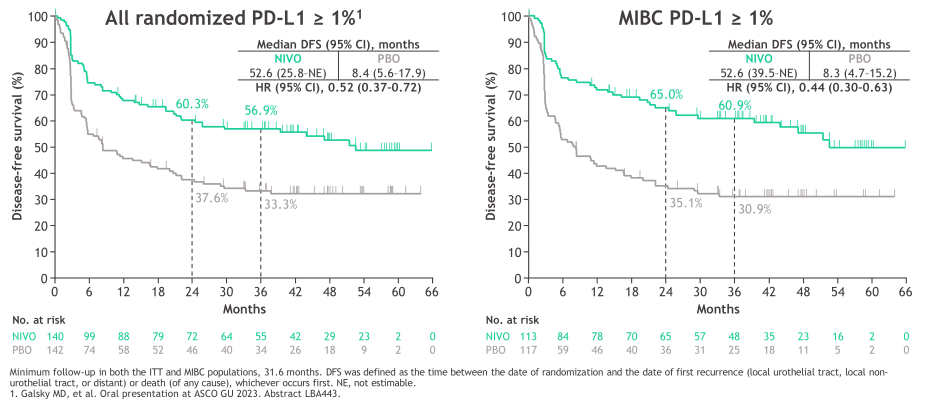
图2 PD-L1表达≥1%时,与安慰剂相比,纳武利尤单抗在所有随机人群和MIBC亚组人群的DFS获益
王科教授表示,CheckMate-274研究的数据一经公布就引起全世界的广泛关注,随着随访时间延长至36.1个月,纳武利尤单抗在所有随机人群的获益始终如一。同时,MIBC人群的获益与所有随机人群保持一致。无论患者PD-L1表达情况如何,纳武利尤单抗组的NUTRFS与DMFS、PFS2结果均具有优势,研究中也未观察到明显的安全性事件。“此次3年随访数据的更新进一步为纳武利尤单抗辅助治疗作为高复发风险尿路上皮癌术后的标准治疗提供了有力的循证医学证据。”
吕强教授同样认为CheckMate-274研究取得了令人惊喜的长期随访结果,并期待后续OS数据的公布。同时,吕强教授提到,CheckMate-274研究有多个国内医疗中心参与,纳入了为数不少的中国尿路上皮癌患者,他们也从中获益,为中国尿路上皮癌患者带来了更多的选择。
另开生面
纳武利尤单抗树立尿路上皮癌辅助治疗新标准
基于辅助化疗EORTC 30994⁹、POUT¹⁰等研究结果,CSCO指南对尿路上皮癌进行了术后辅助化疗的推荐,不过刘涛教授表示,这些研究结果不甚理想,患者长期获益并不明确,缺乏高质量、高级别的循证医学证据;加之患者对化疗的抗拒或不耐受,导致辅助化疗的地位十分尴尬,无法很好地满足临床需求。而CheckMate-274研究证实,无论患者PD-L1表达状况如何,纳武利尤单抗组的DFS获益均十分显著。如此高级别循证医学证据的出现,给了临床医生和患者极大的信心。作为国内首个且目前唯一获批用于尿路上皮癌术后辅助治疗的PD-1的抑制剂,纳武利尤单抗革新了尿路上皮癌术后辅助治疗的格局,树立了尿路上皮癌辅助治疗的新标准。刘涛教授认为,随着纳武利尤单抗临床使用经验的不断丰富,成功病例的不断增多,其在真实世界中的表现可能会更加亮眼,迈向尿路上皮癌治疗的新高峰。
吕强教授补充道,对于高复发风险尿路上皮癌患者,术后是否需要辅助治疗、辅助治疗如何开展始终是困扰泌尿外科医生的一大难题。CheckMate-274研究的成功带来了很好的循证医学证据,临床医生有了治疗依据,患者也可以从辅助免疫治疗中获益,让我们期待后续研究数据的披露以及各中心小样本研究的总结带来更多的惊喜。
方兴未艾
免疫治疗引领尿路上皮癌治疗新风向
在尿路上皮癌领域,以纳武利尤单抗为代表的免疫治疗已实现从晚期二线、晚期一线到术后辅助治疗的全面探索,展示出了良好的应用前景。王科教授表示,CheckMate-274研究的成功,为尿路上皮癌的辅助治疗提供了指导作用。随着免疫治疗的探索从晚期后线向局部晚期围术期治疗甚至疾病更早期覆盖,极大改变了尿路上皮癌的治疗格局。同时,免疫治疗的前移、与靶向和ADC等药物的联合使用,也是对现有保膀胱策略的有益补充与探索。王科教授谈到,免疫治疗已成为尿路上皮癌治疗领域的研究热点和关键一环。未来尿路上皮癌的治疗,也会与前列腺癌和肾癌一样,向着全程化、多元化、分阶梯的治疗方式转变。我们需要开展多层次、多学科的MDT综合诊疗,完善患者的全程管理,以最大化患者的临床获益。
吕强教授指出,免疫治疗前移的策略非常正确。因为在疾病早期阶段,患者自身免疫状态较好,此时免疫治疗的疗效更好。像纳武利尤单抗这样有着充分临床证据获益的药物,通过不同方案的联合使用,可以为临床医生带来更丰富的治疗选择。随着未来研究的不断深入,相信我国尿路上皮癌的诊疗将会迎来全新的发展,尿路上皮癌患者的生存获益和生活质量都会得到进一步的提高。
参考文献:
1. Xylinas E, et al. Predictors of survival in patients with soft tissue surgical margin involvement at radical cystectomy. Ann Surg Oncol. 2013;20(3):1027-1034.
2. lver G, et al. Neoadjuvant Gemcitabine-Cisplatin Plus Radical Cystectomy-Pelvic Lymph Node Dissection for Muscle-invasive Bladder Cancer: A 12-year Experience. Clin Genitourin Cancer. 2020:18(5):387-394.
3. Madersbacher S, et al. Radical cystectomy for bladder cancer today-a homogeneous series without neoadjuvant therapy. J Clin Oncol. 2003:21:690-696.
4. Hautmann RE, et al. Radical cystectomy for urothelial carcinoma of the bladder without neoadjuvant or adjuvant therapy: long-term results in 1100 patients. Eur Urol. 2012;61(5):1039-1047.
5. 2022版CSCO尿路上皮癌诊疗指南.
6. Bellmunt J, et al. IMvigor010 Study Group. Adjuvant atezolizumab versus observation in muscle-invasive urothelial carcinoma (IMvigor010): a multicentre, open-label, randomised, phase 3 trial. Lancet Oncol. 2021 Apr;22(4):525-537.
7. Dean F. Bajorin, et al. First results from the phase 3 CheckMate 274 trial of adjuvant nivolumab vs placebo in patients who underwent radical surgery for high-risk muscle-invasive urothelial carcinoma (MIUC). Journal of Clinical Oncology. 2021 39:6_suppl, 391-391.
8. Matthew I. Milowsky, et al. Results from the extended follow-up in patients with
muscle-invasive bladder cancer in the CheckMate 274 trial. 2023 AUA. Abstract number 23-9988.
9. Ohlmann CH, et al. Immediate Versus Deferred Chemotherapy After Radical Cystectomy in Patients with pT3-pT4 or N+ M0 Urothelial Carcinoma of the Bladder (EORTC 30994): An Intergroup, Open-label, Randomised Phase 3 Trial. Lancet Oncol 2015;16:76-86. Eur Urol. 2015 Dec;68(6):1104-5.
10. Birtle A, et al. Adjuvant chemotherapy in upper tract urothelial carcinoma (the POUT trial): A phase 3, open-label, randomized controlled trial. Lancet 2020 Apr 18;395(10232):1268-1277.
原文转自公众号:医脉通肿瘤科
https://mp.weixin.qq.com/s/MzCThn57D3KYiDunE_VhIQ
本文为转载文章,如有侵权请联系作者删除。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论