 三甲
三甲
国外非典型畸胎样/横纹肌样瘤(AT/RT)的化疗方案选择
目前,国内外对于 AT/RT 尚无统一的治疗方案。在2016年欧洲开展的一项深入研究中,针对AR/RT患儿的治疗策略展现出了显著进展。除了传统的放射治疗外,该方案还融入了大剂量化学疗法,辅以多次造血干细胞移植支持,这一综合疗法成功地将患儿的六年总体生存率(OS)提升至约46%,实现了相较于十年前数据近乎翻倍的显著改善。广大学术界普遍认为,通过综合运用包括外科手术、精准化疗以及放射治疗在内的多元化治疗手段,能够有效优化此类患儿的病情预后。
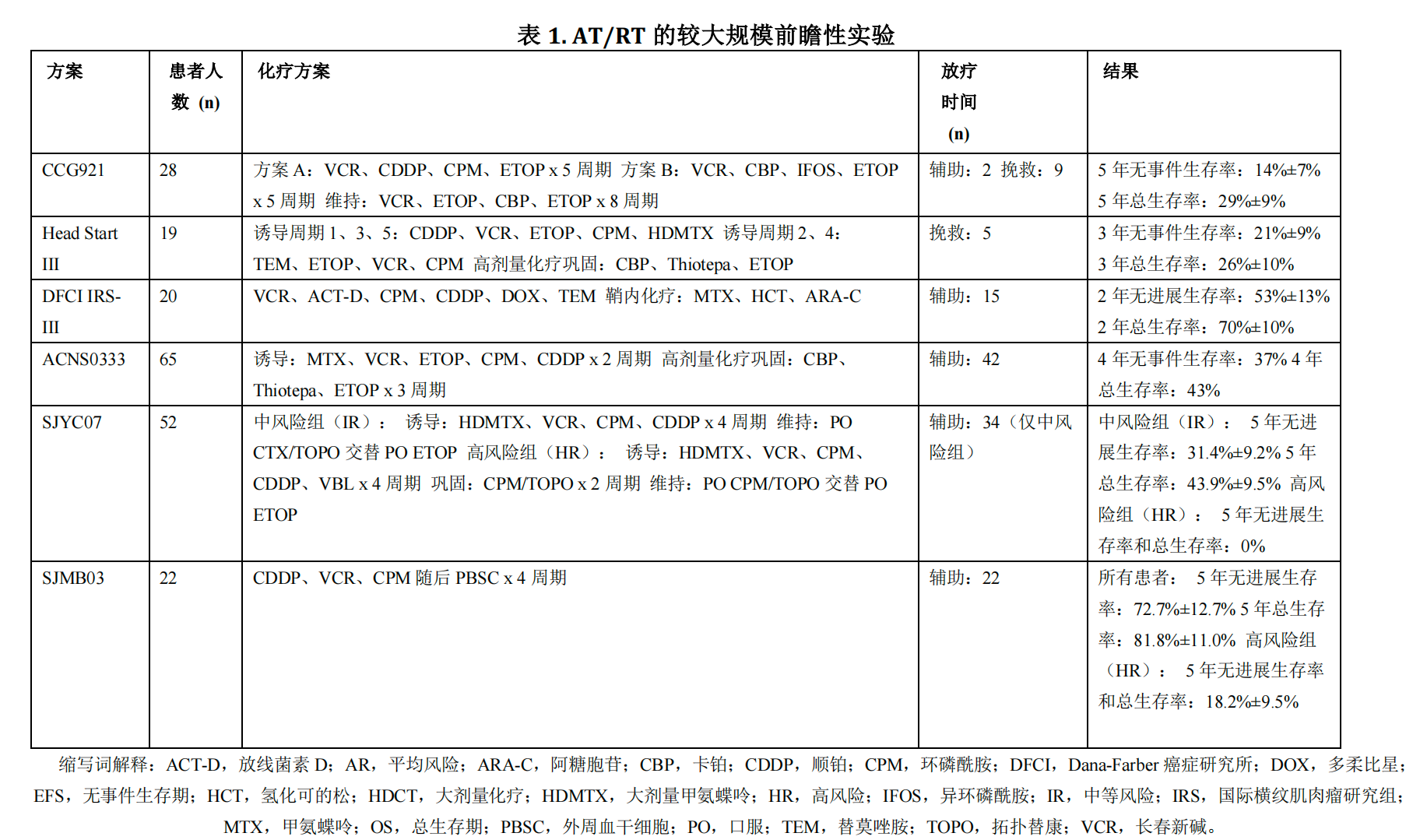
化疗是AT/RT治疗中重要的组成部分,近年关于AT/RT的较大规模前瞻性实验相继完成。
CCG-9921 方案
CCG-9921方案中,涉及28名AT/RT患儿,他们被分配接受两种不同的化疗方案:一组采用长春新碱、顺铂、环磷酰胺、依托泊苷进行5轮化疗,另一组则使用长春新碱、卡铂、异环磷酰胺、依托泊苷同样进行5个周期的化疗。紧接着,所有患儿均接受了由长春新碱、依托泊苷、卡铂组成的8周期维持化疗。在此过程中,有11名患儿接受了放射治疗。该方案实施后,患儿的5年无病生存率达到了14%,而总生存率则为29%。
Head Start III方案
在Head Start III计划中,针对19名AT/RT患儿实施了一项化疗方案,该方案包含五个周期的治疗:第1、3、5周期采用顺铂、长春新碱、依托泊苷、环磷酰胺和甲氨蝶呤的组合;而第2、4周期则替换为替莫唑胺、依托泊苷、长春新碱和环磷酰胺。完成这五个周期后,患儿需进一步接受一个周期的大剂量化疗(HDC)及自体干细胞治疗(ASCT)。然而,由于化疗诱导期间出现的毒副反应和疾病本身的进展,这19名患儿中仅有4名能够完成全部五个周期的化疗,另有3名患儿成功进行了HDC和ASCT。研究结果显示,此治疗方案下的3年无事件生存率(EFS)为21%,而总生存率(OS)则为26%。
ACNS0333 方案
在 ACNS0333 方案中,65 例 AT/RT 患儿进行包括高剂量甲氨蝶呤的两个周期强化多药化疗和 3个串联周期大剂量化疗联合自体干细胞治疗。在此方案中,研究表明 4 年EFS和OS分别为37%和43%。
SJYC07方案
SJYC07方案中,将 52 例患儿根据是否存在转移分为中等风险和高风险。34例中等风险患儿接受4个周期多药诱导化疗,随后接受24周期局部放疗和维持化疗。18例高风险患儿则接受添加长春新碱的4个周期诱导化疗,随后接受 2个周期环磷酰胺和托泊替康巩固治疗,并口服维持。对于诱导结束时年龄≥3岁患儿,进行全脑全脊髓照射(CSI)。研究表明中等风险患儿的5年无进展生 存率和 OS分别为31%和44%。但高风险患儿5年PFS和OS均为0。
SJMB 03方案
在SJMB 03方案中,22例患儿均接受CSI。CSI之后是4个周期多药化疗和外周血干细胞支持治疗。研究表明无远处转移(M0)和肿瘤残留<1.5cm2的平均风险患儿 5 年 PFS 和 OS 分别为 73% 和 82%;有远处转移(M+)或肿瘤残留≥1.5cm2的高风险患儿 5 年 PFS 和 OS 均为18%。
尽管上述试验已表明对于AT/RT患者,其治疗效果有所改善,但这些试验采用了不同的方法。对于新确诊的AT/RT患者,尚未建立统一的治疗标准。国外学者建议,接受ACNS0333和DFCI方案治疗的患者具有相似的特征和治疗效果。对于年龄<3岁的儿童,国外建议根据ACNS0333或DFCI方案进行治疗。对于年龄≥3岁且无残留或转移性疾病的患者,考虑SJMB03方案。关于治疗方案的决定,必须考虑患者的年龄、肿瘤的大小和位置、治疗机构的资源以及家庭因素等。
参考文献:
1、Saunders J, Ingley K, Wang XQ, et al. Loss of BRG1 (SMARCA4) Immunoexpression in a Pediatric Non-Central Nervous System Tumor Cohort. Pediatr Dev Pathol. 2020;23(2):132-138. doi:10.1177/1093526619869154
2、Haberler C, Laggner U, Slavc I, et al. Immunohistochemical analysis of INI1 protein in malignant pediatric CNS tumors: Lack of INI1 in atypical teratoid/rhabdoid tumors and in a fraction of primitive neuroectodermal tumors without rhabdoid phenotype. Am J Surg Pathol. 2006;30(11):1462-1468. doi:10.1097/01.pas.0000213329.71745.ef
3、Bartelheim K, Nemes K, Seeringer A, et al. Improved 6-year overall survival in AT/RT - results of the registry study Rhabdoid 2007. Cancer Med. 2016;5(8):1765-1775. doi:10.1002/cam4.741
4、Upadhyaya SA, Robinson GW, Onar-Thomas A, et al. Relevance of Molecular Groups in Children with Newly Diagnosed Atypical Teratoid Rhabdoid Tumor: Results from Prospective St. Jude Multi-institutional Trials. Clin Cancer Res. 2021;27(10):2879-2889. doi:10.1158/1078-0432.CCR-20-4731
5、Geyer JR, Sposto R, Jennings M, et al. Multiagent chemotherapy and deferred radiotherapy in infants with malignant brain tumors: a report from the Children‘s Cancer Group. J Clin Oncol. 2005;23(30):7621-7631. doi:10.1200/JCO.2005.09.095
6、Alva E, Rubens J, Chi S, et al. Recent progress and novel approaches to treating atypical teratoid rhabdoid tumor. Neoplasia. 2023;37:100880. doi:10.1016/j.neo.2023.100880
7、Bartelheim K, Nemes K, Seeringer A, et al. Improved 6-year overall survival in AT/RT - results of the registry study Rhabdoid 2007. Cancer Med. 2016;5(8):1765-1775. doi:10.1002/cam4.741
本文是阙旖版权所有,未经授权请勿转载。本文仅供健康科普使用,不能做为诊断、治疗的依据,请谨慎参阅





评论